【Sci. Adv.】东北大学王丁意/徐赵东/哥大Lutz Ackermann: 光/镍协同催化的不对称C(sp³)−C(sp)交叉亲电偶联:手性β-炔基乙胺的高效构建
手性炔烃结构单元广泛存在于天然产物、药物分子以及功能材料中。特别是带有手性中心的炔基胺类化合物,因其兼具炔烃的多样转化能力和胺基的生物活性,成为有机合成与药物化学领域研究的热点。因此如何高效、高对映选择性地构建C(sp³)−C(sp)键进而合成手性炔基乙胺类化合物具有重要意义。
近期,东北大学王丁意教授、徐赵东教授与哥大Lutz Ackermann教授合作首次实现了镍/光氧化还原协同催化的不对称交叉亲电偶联反应,成功将外消旋的苄基氮杂环丙烷与炔基溴化物转化为手性β-炔基乙胺。该方法不仅具有优异的区域选择性和对映选择性,还展现了广泛的底物适应性和良好的官能团兼容性,为手性炔基胺类化合物的合成提供了新的策略(图1, DOI: 10.1126/sciadv.aef4526)。
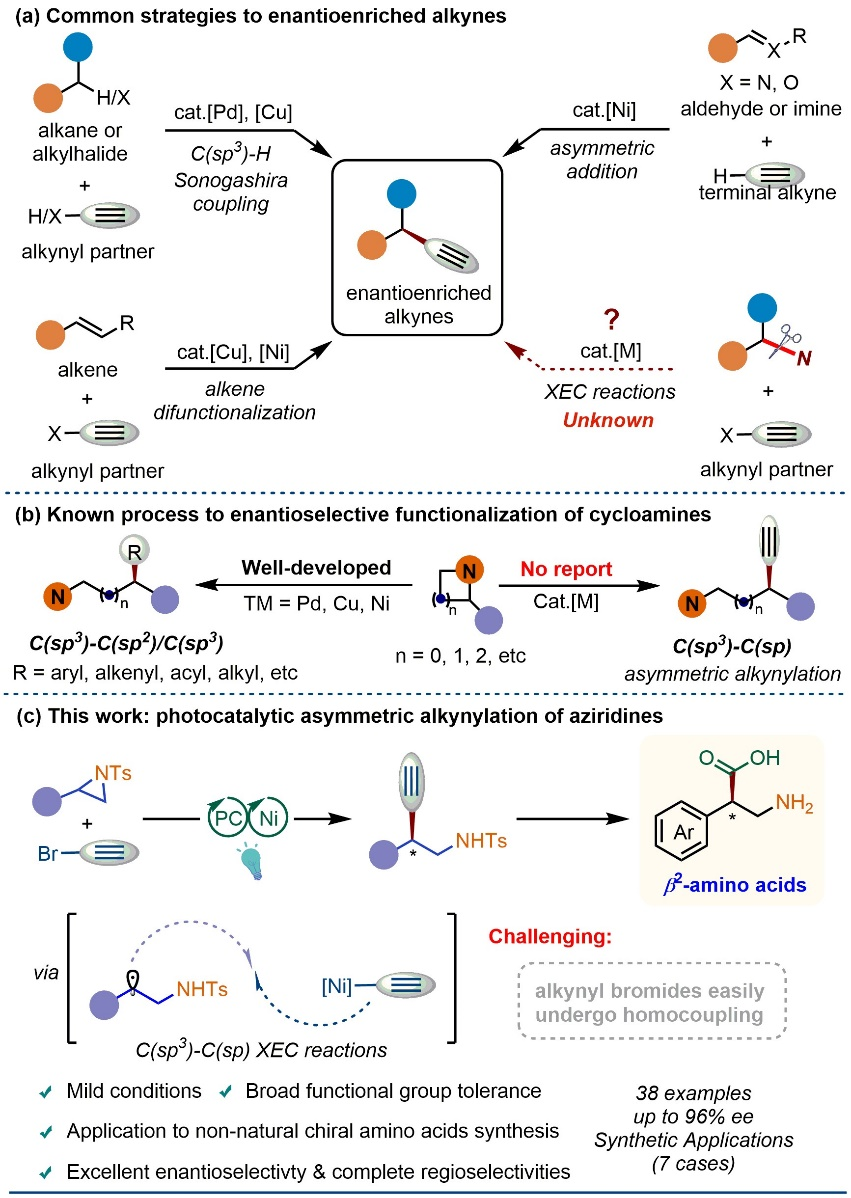
本研究采用镍/光氧化还原双催化体系,以Ir[dF(CF₃)ppy]₂(dtbbpy)PF₆为光催化剂,NiBr₂·DME为镍源,手性双咪唑啉(BiIM)L1为配体,在MgI₂和Et₃N存在下,于390 nm蓝光LED照射下,成功实现了氮杂环丙烷与炔基溴化物的对映收敛性交叉偶联。MgI₂在该体系中扮演关键角色,其促进氮杂环丙烷的区域选择性开环生成β-碘代磺酰胺中间体,该中间体更易被Ni⁰物种还原,从而避免了直接还原炔基溴化物导致的副反应(图2)。
在获得了最优反应条件后,作者对反应的底物范围进行了探究。结果表明该催化体系展现出优异的底物普适性。无论是带有电子给体、电子受体还是卤素取代的芳基氮杂环丙烷,均能以中等到良好的产率(最高>80%)和高对映选择性(最高>95% ee)得到目标产物。位阻较大的邻位取代底物仍能保持中等的对映控制。值得注意的是,含吲哚、萘等稠环或杂环结构的底物同样兼容。炔基溴方面,多种硅基保护基、烷基、芳基以及源自天然产物(如薄荷酮、雌酮、维生素E)的炔基溴均能顺利反应,体现了该方法在复杂分子后期修饰中的潜力(图3)。
在合成应用方面,所得β-炔基乙胺可进一步转化为多种高附加值化合物。例如,通过N-甲基化、环化反应获得手性含氮杂环、半氢化生成(Z)-烯胺、点击化学构建三唑及Ru催化氧化三键生成手性β²-氨基酸等。特别是后者,为合成非天然氨基酸及其相关药物(如Akt抑制剂)提供了新路径(图4)。
通过一系列控制实验与循环伏安分析,作者提出了此反应可能的反应机理:炔基溴化物与Ni⁰发生氧化加成生成NiII中间体;与此同时,氮杂环丙烷在MgI₂和NiII作用下开环生成β-碘代或溴代磺酰胺;该中间体经单电子还原生成苄基自由基,随后被NiII−炔基中间体捕获,形成NiIII物种,经还原消除得到目标产物。光催化剂通过还原淬灭循环再生Ni⁰,完成催化循环(图5)。
综上所述,本研究实现了镍/光氧化还原协同催化的C(sp³)−C(sp)不对称交叉亲电偶联反应,为手性β-炔基乙胺类化合物的合成提供了高效、温和、高选择性的新方法。该方法不仅拓展了氮杂环丙烷在不对称合成中的应用范围,也为金属/光氧化还原协同催化体系的底物设计提供了新的途径。
论文信息:
Hongyan Lan, Zhao-Dong Xu*, Zhuangzhi Shi, Lutz Ackermann*, Dingyi Wang*
Enantio- and regioselective nickel/photoredox-catalyzed cross-electrophile coupling of benzylic aziridines with alkynyl bromides
Sci. Adv. 2026, 12, eaef4526. DOI:10.1126/sciadv.aef4526.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




