JACS:光催化烯烃参与[2+1]和[2+1+1]环化发散性合成环丙烷和环丁烷

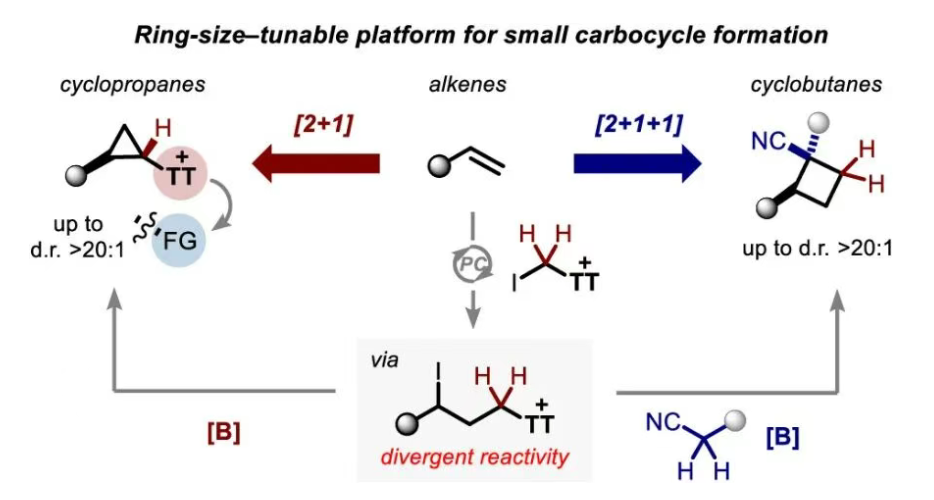
最近,韩国首尔大学Seung Youn Hong课题组,以烯烃和碘甲基噻蒽鎓盐为原料,经光催化[2+1]和[2+1+1]环化反应,实现环丙烷和环丁烷的非对映选择性发散性合成。此方法中,烯烃和碘甲基噻蒽鎓盐可经光催化反应生成3-碘代烷基噻蒽鎓中间体。此1,3-双亲电试剂具有双重反应性,可发生可调成环环化和衍生化,具体包括:1)1,3-双亲电试剂在适当碱作用下转化成噻蒽鎓叶立德中间体,然后发生[2+1]环化得到环丙基噻蒽鎓盐。所得产物可通过非对映选择性C(sp³)–N交叉偶联,和多种自由基介导官能团化反应实现衍生化,得到多种1,2-双官能团化环丙烷产物;2)1,3-双亲电试剂在更温和碱作用下,可与亚甲基化前亲核试剂发生[2+1+1]环化,得到1,2-双官能团化环丁烷产物。相关研究成果于近期在线发表在《美国化学会志》杂志上(J. Am. Chem. Soc. DOI: 10.1021/jacs.5c21279)。
环丙烷和环丁烷是具有重要价值的小碳环化合物,广泛应用于药物、农用化学品和功能材料领域(Figure 1A)。在合成化学和药物化学中,此类小碳环所具有的刚性构象特征可以施加几何约束,从而在三维空间中精确限制官能团的出口向量(exit vectors)。此外也常用作偕二甲基或sp²杂化芳基的生物电子等排体,可以降低分子平面性并通常能显著提高代谢稳定性。因此,在构效关系研究中,将此类刚性小碳环引入生物活性先导化合物,已成为一种重要的药物设计原则。
此工作简介:Seung Youn Hong课题组最近报道过一种以烯烃和碘甲基噻蒽鎓盐为原料,经3-碘代烷基噻蒽鎓中间体得到1,3-双官能团化产物的烯烃同系化反应(Nat. Chem. 2026, 1−9)。此文中,作者进一步利用3-碘代烷基噻蒽鎓中间体所具有的双重反应性,分别经光催化[2+1]环化和[2+1+1]环化反应,发散性得到1,2-双官能团化环丙烷和环丁烷产物(Figure 1C)。
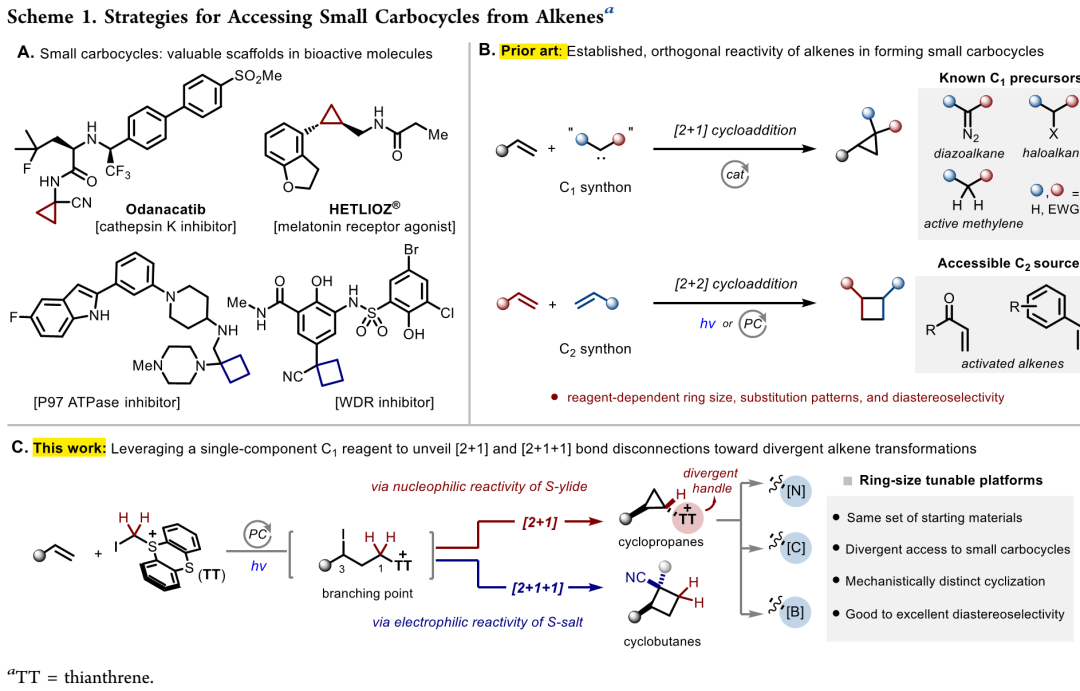
(Scheme 1,来源:J. Am. Chem. Soc.)
可调环化反应发现:如Figure 1A所示,烯烃2、碘甲基噻蒽鎓盐1和亚甲基类前亲核试剂4(pronucleophile),在组内已报道光催化反应条件下(Nat. Chem. 2026, 1−9),能同时得到[2+1]环化产物环丙基噻蒽鎓盐5和[2+1+1]环化产物环丁烷6,验证可调环化反应可行性。基于此,作者进一步优化碱,得出如Figure 1B所示两种优选反应条件和发散性机理:1)烯烃2和碘甲基噻蒽鎓盐1反应所得1,3-双亲电试剂3-碘代烷基噻蒽鎓3,在LDA作碱时(条件A),会脱质子转化成噻蒽鎓叶立德7,7发生[2+1]环化得到环丙基噻蒽鎓盐5;2)在更温和的碳酸铯作碱时(条件B),3可与亚甲基化前亲核试剂4发生单选择性置换得到中间体8,然后发生[2+1+1]环化得到1,2-双官能团化环丁烷6。
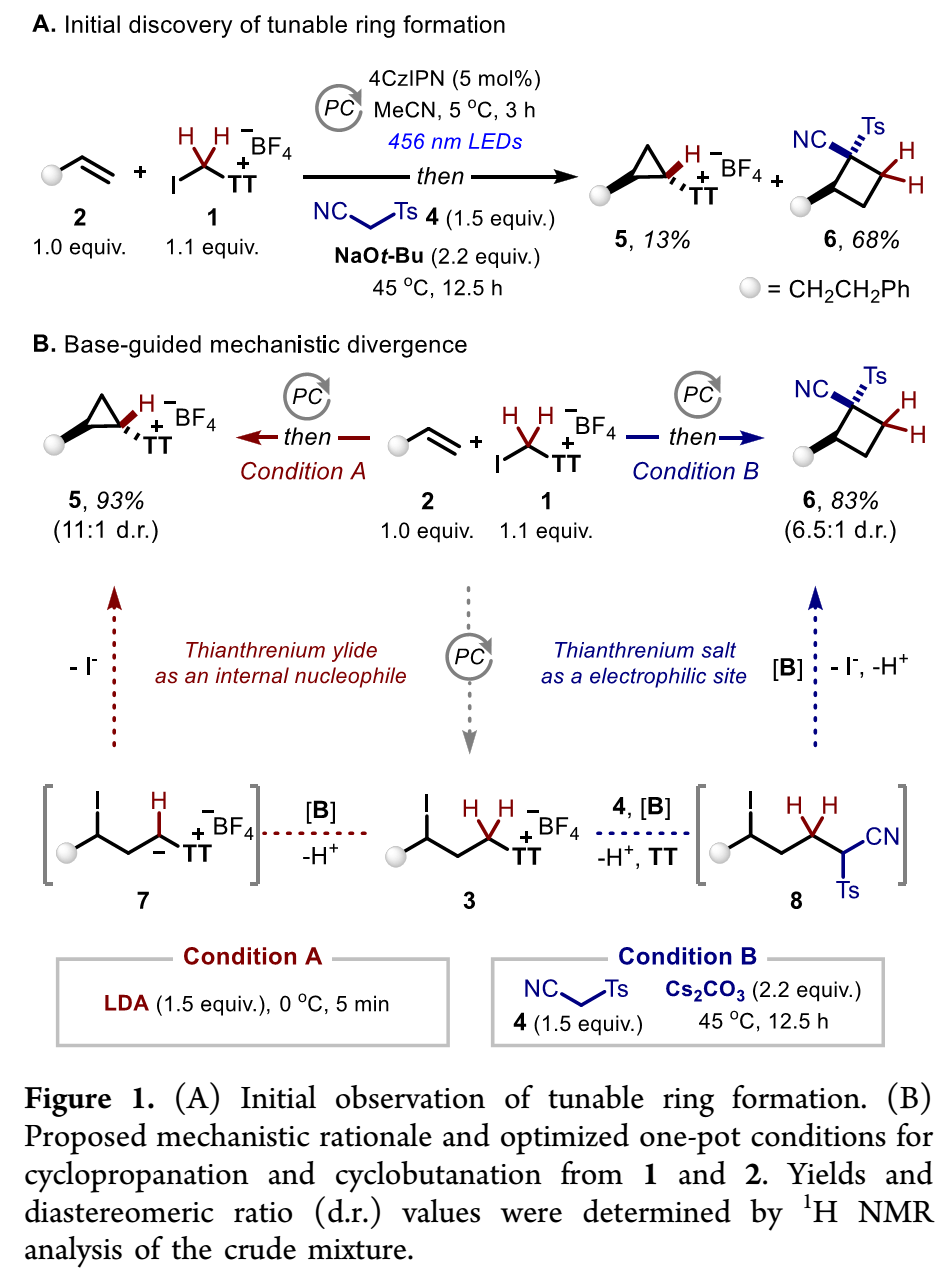
(Figure 1,来源:J. Am. Chem. Soc.)
环丙基噻蒽鎓盐合成:如Table 1所示,在[2+1]环化优选反应条件下,多种非活性末端烯烃可以和碘甲基噻蒽鎓盐发生理想反应,以可观收率和非对映选择性得到反式环丙基噻蒽鎓盐。反应兼容带苯基、苄醚、磺酰胺、酯基等多种末端烯烃,以及含各种基团苯乙烯。但对于缺电子分子间烯烃,仅会得到3-碘代烷基噻蒽鎓中间体,而不会发生后续环化。
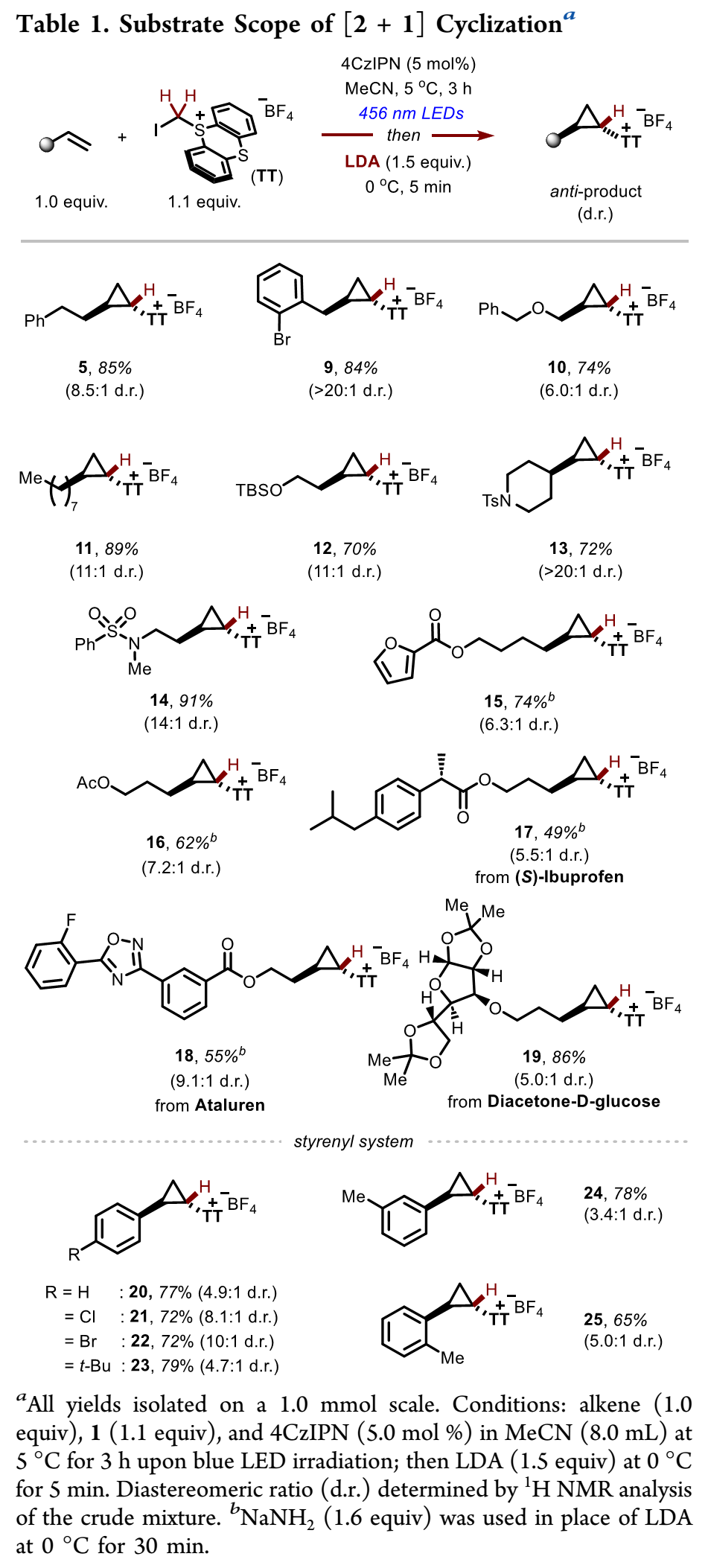
(Table 1,来源:J. Am. Chem. Soc.)
环丙基噻蒽鎓盐衍生:所得噻蒽鎓盐是稳定固体,可分离纯化用于后续衍生化。作者通过Figure 2所示反应设计和条件筛选研究,得出非对映选择性C(sp³)–N交叉偶联反应优选条件。在优选条件下,能将[2+1]环化所得多种环丙基噻蒽鎓盐,和各种氮亲核试剂包括吲哚、吲唑、吡咯、酰胺等,偶联成反式1.2-双取代环丙烷产物(Table 2)。此外,[2+1]环化所得环丙基噻蒽鎓盐,也可通过多种已报道自由基介导官能团化反应构建C(sp³)–X(X=H、C、B)键,进一步实现多样化衍生(Figure 3)。
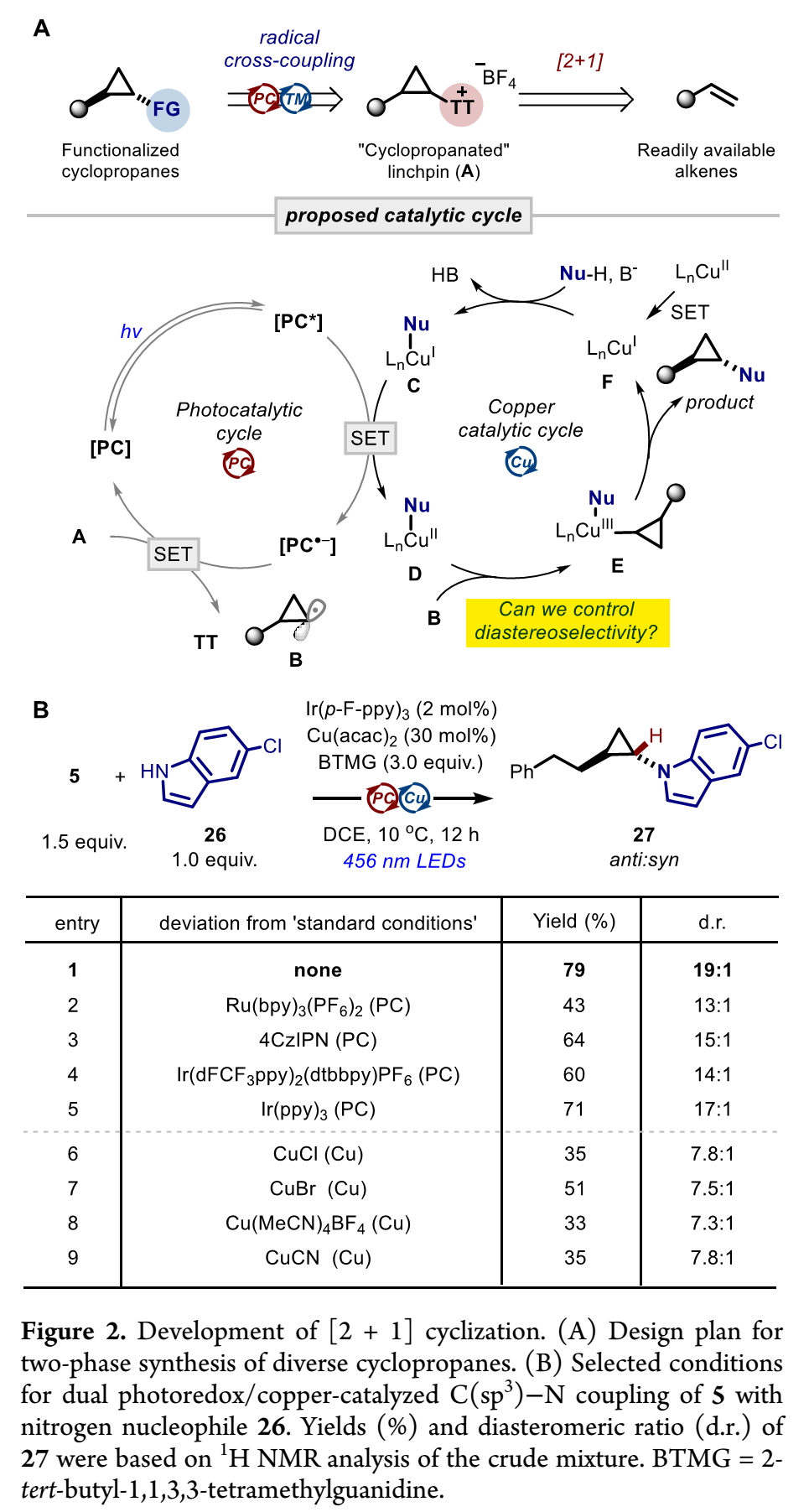
(Figure 2,来源:J. Am. Chem. Soc.)
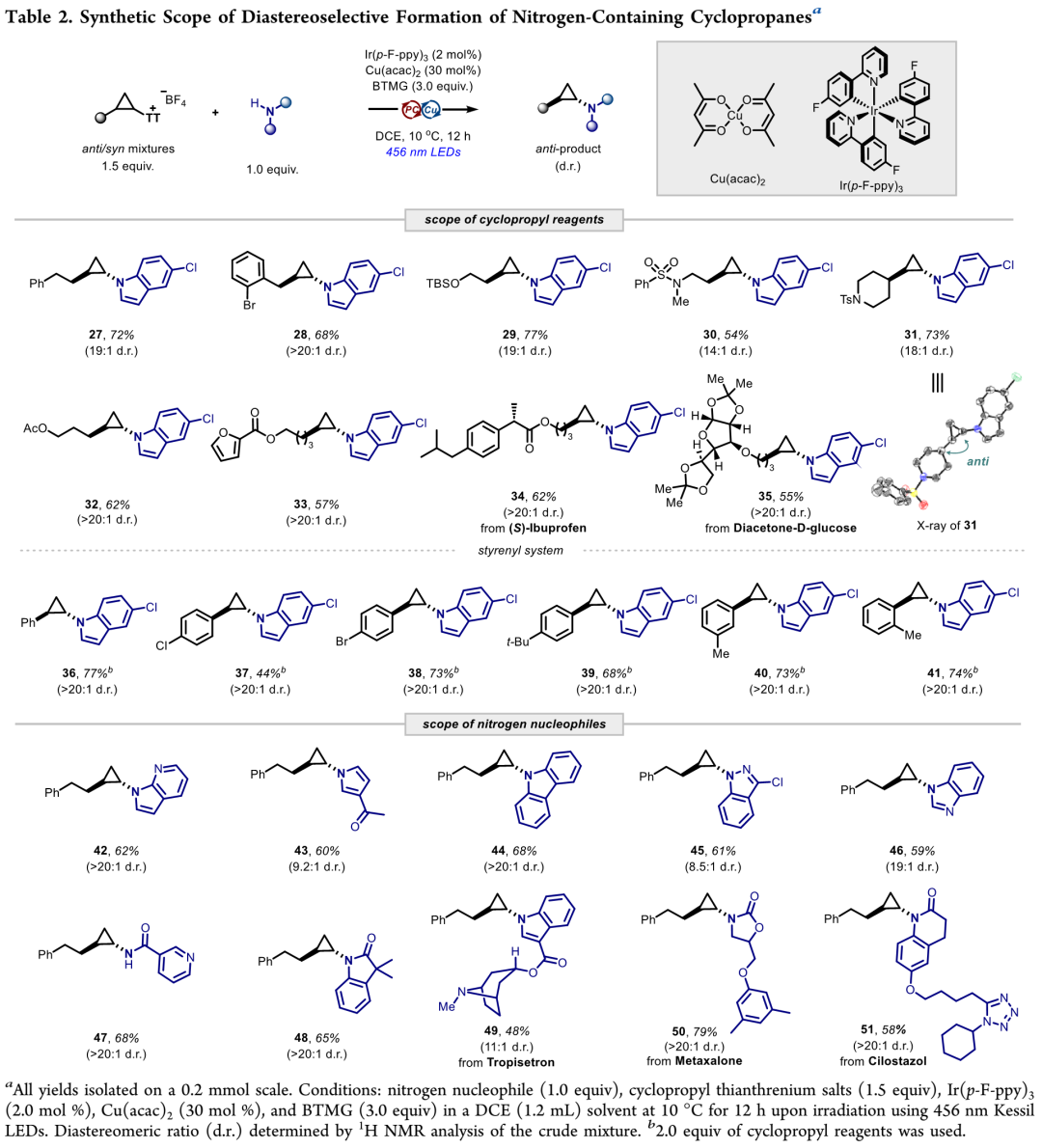
(Table 2,来源:J. Am. Chem. Soc.)
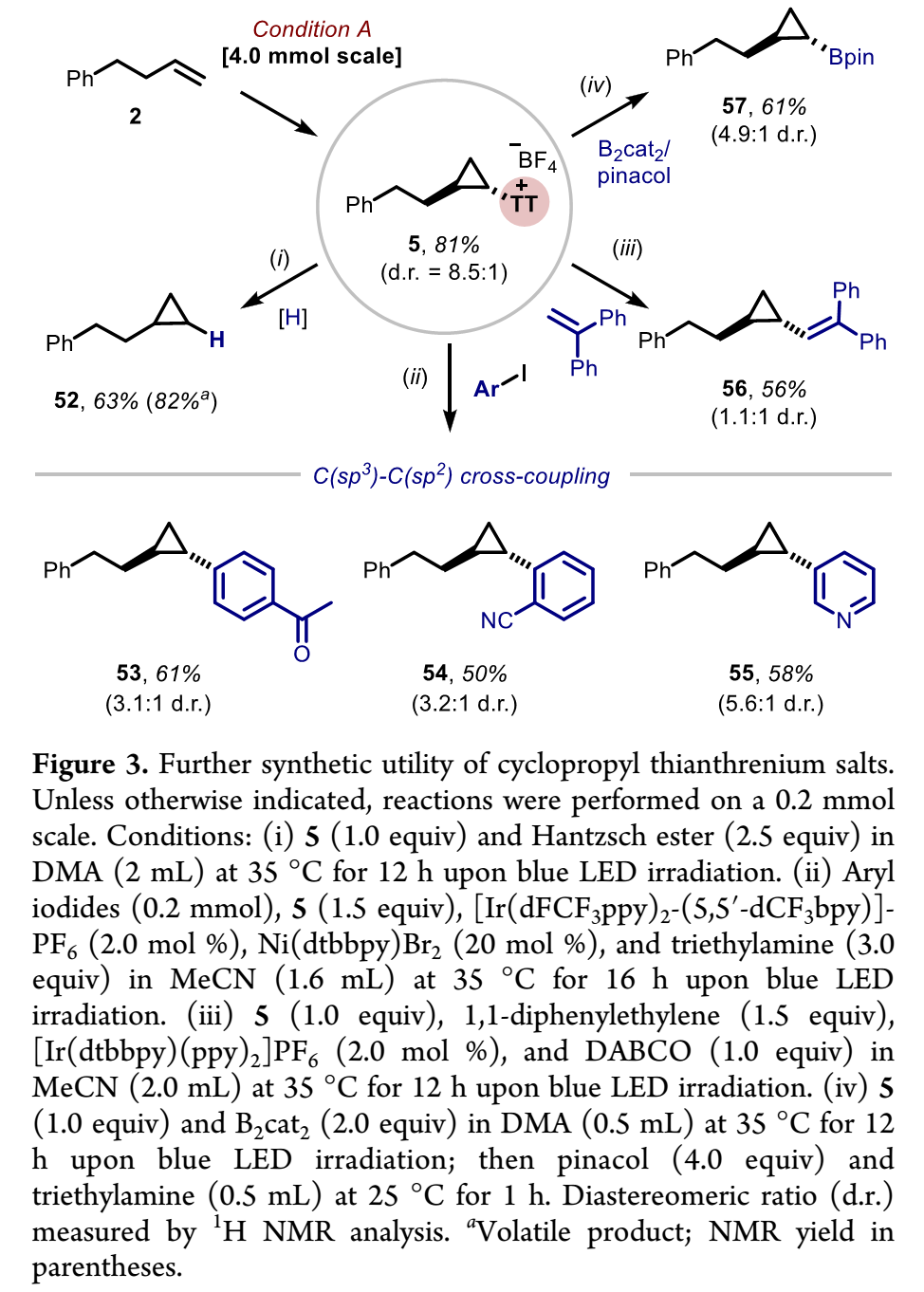
(Figure 3,来源:J. Am. Chem. Soc.)
环丁烷合成机理研究:如Figure 4所示,作者通过反应进程监控得出[2+1+1]环化反应可能中间体是8而不是58。并进一步通过8参与环化反应条件筛选得出碳酸铯是最优碱,可能原因是铯离子作为路易斯酸可以通过与前亲核试剂形成双齿螯合发挥旁观者作用,从而增强金属腈化物动力学活性。
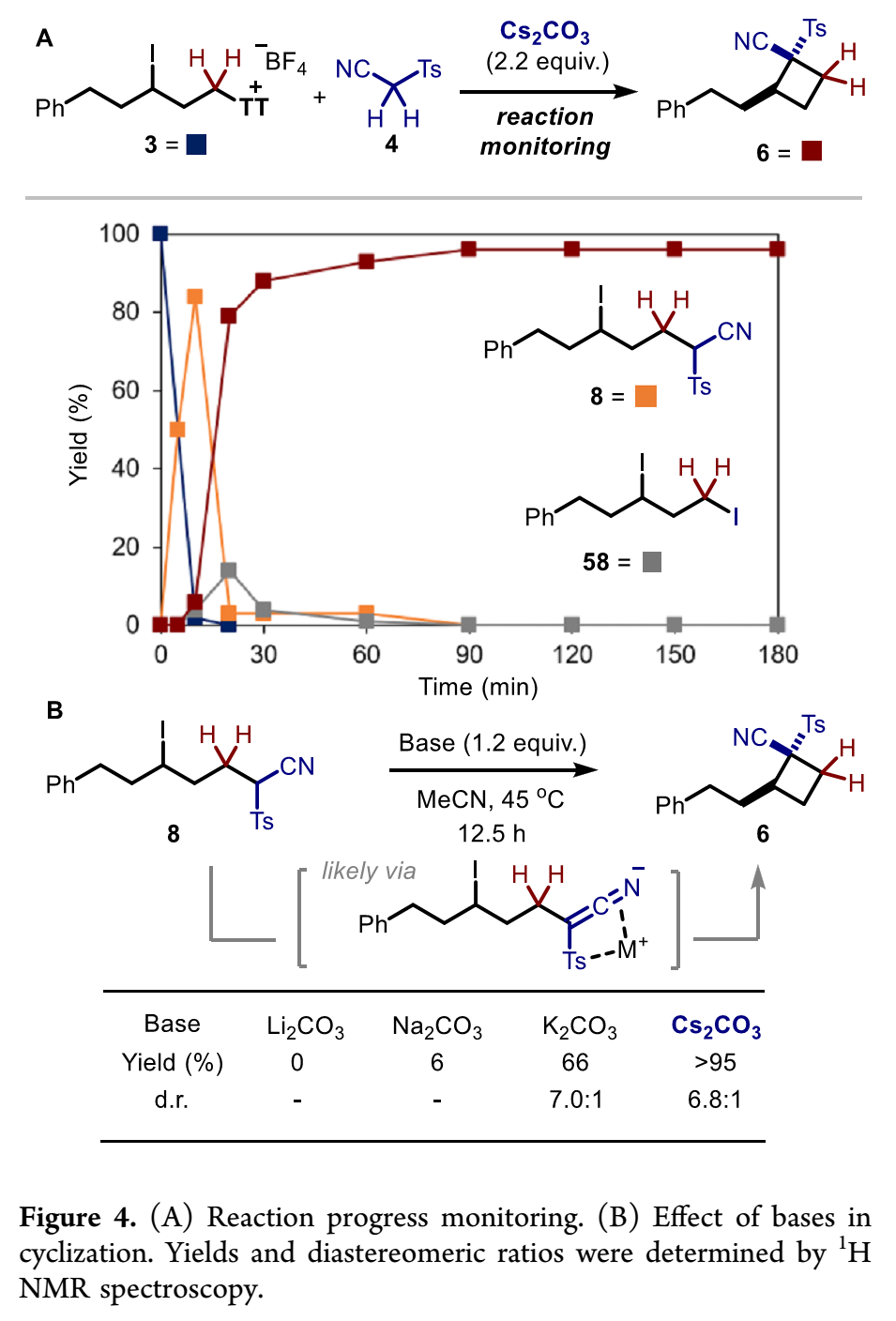
(Figure 4,来源:J. Am. Chem. Soc.)
环丁烷合成底物拓展:如Table 3所示,在[2+1+1]环化优选反应条件下,多种非活性末端烯烃和前亲核试剂腈化物,可以和碘甲基噻蒽鎓盐发生理想反应,以可观收率和非对映选择性得到1,2-双官能团化环丁烷。反应兼容含苯基、苄醚、酰亚胺、磺酰胺、酯基等基团的末端烯烃,以及含磺酰基、噻唑、吡啶、嘧啶等多种基团的腈化物。
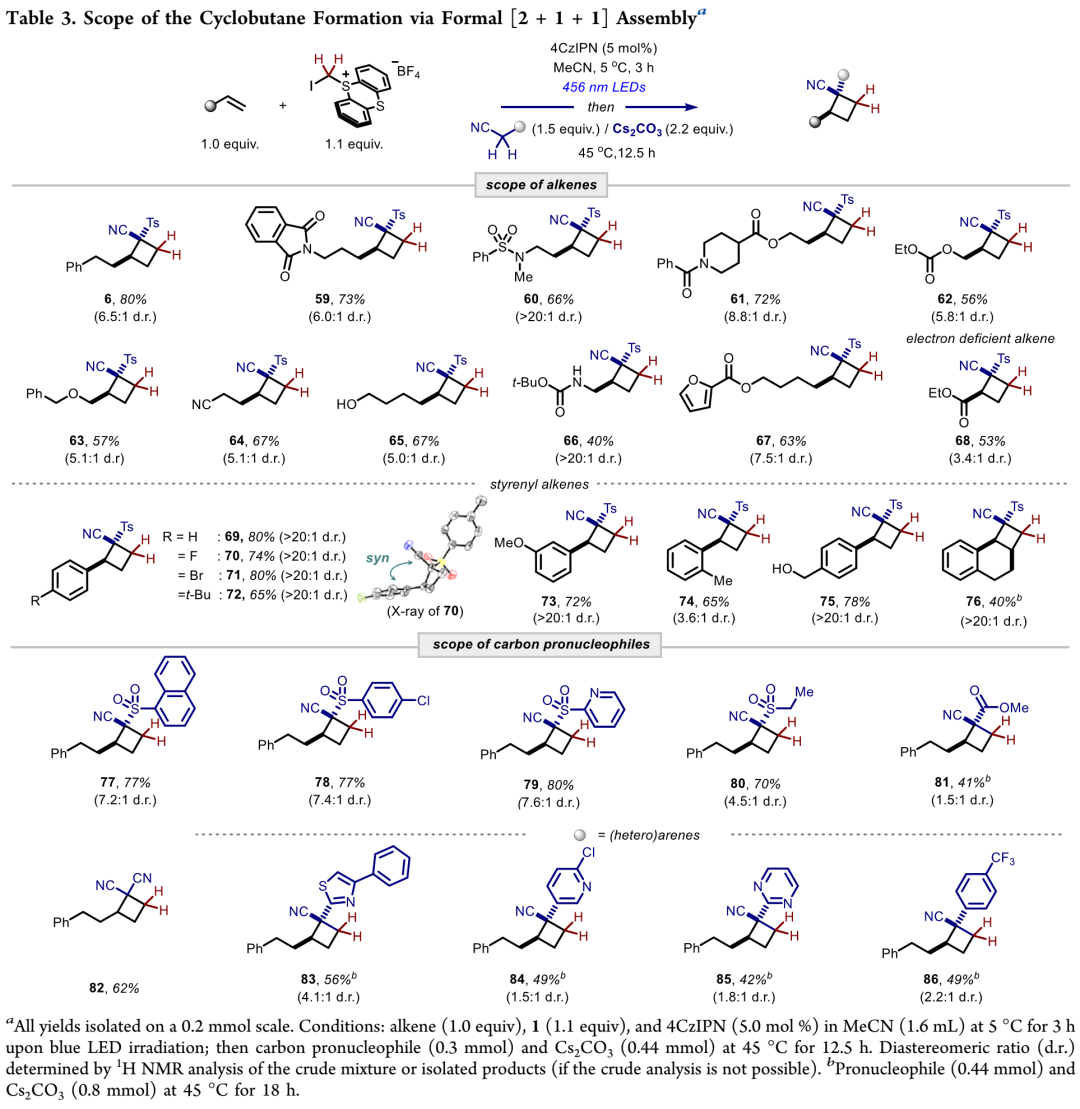
(Table 3,来源:J. Am. Chem. Soc.)
环丁烷合成应用和衍生:如Figure 5所示,1)各种药物衍生物或生物活性分子,可经[2+1+1]环化反应,转化成1,2-双官能团化环丁烷类似物;2)所得环丁烷产物69和95,可分别经水解反应、四唑化、氟化、磺酰胺化、酯化和脱磺酰基,转化成酰胺93、四唑94、磺酰氟96、磺酰胺97、酯98。
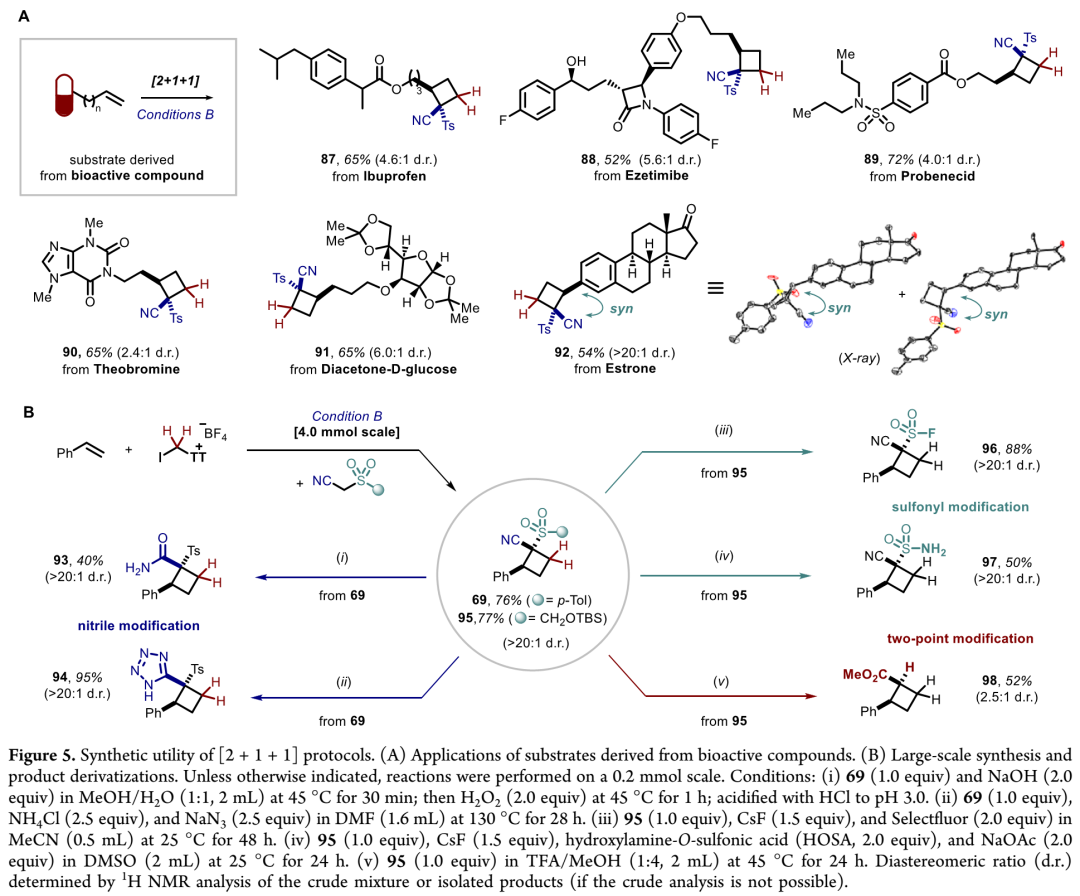
(Figure 5,来源:J. Am. Chem. Soc.)
利用3-碘代烷基噻蒽鎓的双重反应性,Seung Youn Hong课题组发展出新颖的烯烃参与[2+1]和[2+1+1]环化反应,可以非对映选择性合成1,2-双官能团化环丙烷和环丁烷。这两种反应均适用于复杂分子的后期结构修饰,为1,2-双官能团化环丙烷和环丁烷提供了一种模块化且高非对映选择性合成方法。
论文信息:
[2+1] and [2+1+1] Cyclization: Diversifying Alkenes for Small Carbocycles via Photocatalytically Accessed 1,3-Dielectrophiles
Junseong Jang, Chaewon Kim, Junhwan Won, and Seung Youn Hong*
doi:10.1021/jacs.5c18227
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




