Angew:铁光催化烷烃的C(sp³)-H磷酰化反应
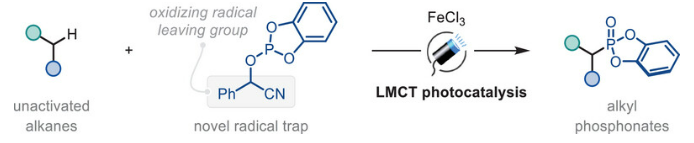
烷基膦酸酯是一类极具价值的关键结构单元,具有广泛的合成用途,且其普遍存在于生物活性分子中。到目前为止,研究人员已开发出多种方法以实现有机分子的高效膦酰化,通常涉及利用磷(III)试剂对常见官能团进行取代来构建C(sp³)-P键。然而,未活化的C(sp³)-H键的直接膦酰化反应仍鲜有报道,且目前尚缺乏将膦酸酯基团引入复杂分子(后期官能团化)的普适性方法。基于此,英国布里斯托尔大学(University of Bristol)Adam Noble和Varinder K. Aggarwal课题组报道了一种利用铁光催化剂,基于氢原子转移(HAT)策略实现未活化烷烃C(sp³)-H键光诱导膦酰化的方法。该反应成功的关键在于开发了一种新型的扁桃腈衍生亚磷酸酯自由基捕获剂,该试剂带有具氧化性的苯乙腈自由基离去基团,能够实现光催化剂的有效循环。该方法表现出良好的官能团兼容性,对空间位阻较小的C-H键的膦酰化具有高选择性,且适用于复杂分子中膦酸酯的后期区域选择性引入。相关成果发表在Angew. Chem. Int. Ed., 2026, DOI: 10.1002/anie.6650940上(Scheme 1)。
作者以环己烷的膦酰化反应作为研究起点,在390 nm LED光照下使用FeCl₃作为光催化剂进行了考察(Table 1)。为了实现膦酸酯生成,作者需要一种能够有效捕获由LMCT(配体到金属的电荷转移)介导的HAT过程产生的仲烷基自由基的亚磷酸酯。此前,作者曾开发了二苯甲基邻苯二酚亚磷酸酯P1,用于光氧化还原催化的伯烷基和仲烷基自由基膦酰化反应。在该试剂中,芳香二醇配体通过稳定中间体磷酰基自由基来促进自由基对磷的加成,而二苯甲基则作为高效的自由基离去基团,通过β-断裂促进后续膦酸酯的生成。令人欣慰的是,使用P1对环己烷进行膦酰化反应取得了成功,在最初生成的邻苯二酚膦酸酯1b经部分甲醇解后,得到了膦酸酯1a(Scheme 2),但产率仅为15%(Table 1,entry 1)。尽管将催化剂改为FeCl₂后,1a的产率可提升至43%(entry 2),但继续使用亚磷酸酯P1未能实现产率的进一步提升。
作者对基于P1的膦酰化反应机理假设如下:磷酰基自由基中间体I发生β-断裂生成膦酸酯1b和二苯甲基自由基II,随后II被光催化剂还原为碳负离子,再经质子化生成二苯甲烷III(Scheme 2)。出乎意料的是,作者在粗产物混合物中并未检测到III,而是发现了大量由二苯甲基自由基二聚生成的1,1,2,2-四苯基乙烷(IV)。这表明光催化剂还原二苯甲基自由基的速率较慢,从而导致催化剂循环效率低下。因此,作者测试了几种带有更具缺电子性自由基离去基团的新型邻苯二酚亚磷酸酯,旨在生成具有更强氧化性的自由基,从而通过将Fe(II)重新氧化为Fe(III)来促进催化剂循环。将P1中的苯基替换为甲基酯基(P2)导致产率急剧下降(entry 3);而引入氰基则起到了相反的作用,在使用扁桃腈衍生亚磷酸酯P3时,1a的产率达到了85%(entry 4)。随后,作者探索了其他带有苄腈类自由基离去基团的亚磷酸酯,包括联苯和苯甲腈衍生的亚磷酸酯P4和P5,但它们相比P3并未带来进一步的改善(entries 5-6)。研究发现亚磷酸酯上的邻苯二酚基团是不可或缺的,因为使用乙二醇或频哪醇亚磷酸酯时仅观察到痕量产物。作者对其他催化剂及其用量的考察证实,10 mol%的FeCl₃为最优条件,尽管使用20 mol%的FeCl₂也能获得相当的产率(entries 7-10)。最后,控制实验证明了光和光催化剂在C(sp³)-H膦酰化反应中不可或缺(entries 11-12)。
在最优条件下,作者考察了该C(sp³)-H膦酰化反应的底物范围(Scheme 3)。为简化产物的纯化,易水解的邻苯二酚膦酸酯被转化为二甲膦酸酯。环状与无环烷烃均能以中高收率转化为相应产物。该反应对空间位阻较小的C(sp³)-H键具有高选择性,优先发生甲基取代,这与此前LMCT光催化氯自由基介导反应的选择性一致。氯代烷烃能在远离氯原子的位置实现极高选择性膦酰化。通过空间位阻屏蔽,可在含弱烯丙基或苄基C(sp³)-H键的底物中实现甲基选择性修饰。含芳环和酮的底物能高选择性地生成苄基或β-酮膦酸酯。此外,酯基、氰基、磺酰胺、酰亚胺及甲基硅烷等官能团均良好兼容,展现出高区域选择性。该策略还能以高区域选择性和实用收率实现氨基酸、药物分子及单糖等复杂分子的后期膦酰化。此外,针对部分底物,作者微调条件可提升效果,如使用FeCl₂光催化或改用乙腈/氯乙腈混合溶剂。有趣的是,在含叔C(sp³)-H键底物中添加亚苄基丙二腈(BMN)能显著提升产率,推测其通过捕获未反应的叔烷基自由基,为催化剂循环提供了替代途径。
为了探究反应机理,作者开展了一系列研究(Scheme 4)。1,6-庚二烯的自由基捕获实验生成了环状产物,证实了氯自由基的参与。针对本反应反常的高伯碳选择性,竞争实验表明,反应确实生成了叔烷基自由基,但其在膦酰化中呈惰性。而真正的选择性由后续的C-P键形成决定,即经历无选择性的HAT后,P3优先捕获伯烷基自由基。此外,BMN能捕获未反应的惰性叔自由基,抑制其导致的催化剂失活,从而解释了其提升产率的原因。
环己烷及其氘代物的分子间和平行动力学同位素效应(KIE)分别为1.1和1.3,表明HAT并非决速步,与LMCT光催化机制一致。副产物苯乙腈的氘结合率为57%,加等当量水后降至10%,证实该副产物源于苯乙腈自由基经单电子还原后,从HAT产生的HCl中获取质子。
基于上述结果,作者提出的该C(sp³)-H膦酰化反应机理如Scheme 5a所示。FeCl₃发生光诱导的LMCT产生氯自由基和Fe(II)物种。氯自由基从烷烃V中发生HAT,生成HCl和烷基自由基VI。随后,VI加成到亚磷酸酯P3上生成磷酰基自由基VII,该中间体因未成对电子离域到邻苯二酚骨架上而得到稳定。接下来的β-断裂生成环状邻苯二酚膦酸酯VIII和稳定的苯乙腈自由基IX。最后,IX被光催化剂的Fe(II)态还原,并与HCl发生质子转移,生成副产物43,同时再生基态Fe(III)氯配合物,从而完成光催化循环。与二苯甲基亚磷酸酯P1相比,扁桃腈亚磷酸酯P3带来的反应效率提升可归因于自由基离去基团IX具有更高的氧化电位,而二苯甲基自由基II的氧化电位较低。
基于Scheme 4b中的竞争实验,该反应对甲基而非亚甲基和次甲基具有高膦酰化选择性,是由于P3与伯烷基自由基的反应效率高于仲烷基和叔烷基自由基(Scheme 5b)。这很可能是因为,与由位阻较大且较稳定的仲/叔自由基相比,由空间位阻较小且稳定性较差的伯自由基生成磷酰基自由基VII的反应速率更快,且可逆性更低。仲烷基和叔烷基自由基较慢的膦酰化速率使得其他竞争路径占据了主导地位。例如,副产物43中较弱的苄基C-H键(键解离能 = 82 kcal/mol)可能发生HAT,从而再生起始烷烃并生成苯乙腈自由基IX,该自由基能够将Fe(II)重新氧化为Fe(III)。这种伴随光催化剂循环的逆HAT过程可以解释为什么在初始HAT阶段形成伯烷基自由基的选择性相对较低的情况下依然能够观察到高产率的伯位选择性膦酰化。在含次甲基的底物中,BMN的有益作用可能源于:与仲自由基相比,向更稳定的叔烷基自由基发生逆HAT的过程更为不利,这就必须加入BMN作为协同自由基捕获剂,以实现光催化剂的循环。
Adam Noble和Varinder K. Aggarwal课题组报道了一种利用廉价铁催化剂、通过光诱导LMCT过程实现未活化烷烃直接C(sp³)-H膦酰化的方法。该反应在温和条件下进行,并对多种官能团表现出良好的兼容性,从而能够将膦酸酯基团引入到广泛的底物中。该反应成功的关键在于设计了一种新型的自由基膦酰化试剂—扁桃腈邻苯二酚亚磷酸酯(P3),其含有一个关键的苯乙腈基团,该基团作为一种良好的自由基离去基团,通过磷酰基自由基中间体的快速β-断裂促进膦酸酯的生成;此外,其生成具有强氧化性的自由基,能够通过将Fe(II)重新氧化为Fe(III)来实现光催化剂的循环。对于无环底物,反应表现出对甲基膦酰化的高选择性,这源于空间位阻较小的伯烷基自由基在形成C-P键时具有极高的偏好性。因此,该C(sp³)-H膦酰化方法适用于将膦酸酯基团区域选择性地后期引入到复杂有机分子中。尽管该反应的整体效率通常仅为中等水平,但这种简便的条件为合成多种膦酸酯产物提供了一种实用的策略。
论文信息:
Iron-Photocatalyzed C(sp³)-H Phosphonylation of Alkanes
Ya Dong, Wangyujing Han, Hanwen Zhang, Santosh K. Pagire, Harry Meats, Adam Noble, Varinder K. Aggarwal
Angew. Chem. Int. Ed. 2026, DOI: 10.1002/anie.6650940.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




