【Chem. Sci.】河南大学王华教授团队:光化学选择性骨架编辑策略一步构筑π-拓展螺烯
近日,河南大学王华教授团队在Chemical Science上发表了一项突破性研究,报道了一种新颖的光化学骨架编辑策略构筑碳螺烯。该策略能够将易于合成的二芳基联二噻吩直接转化为具有精准区域选择性的π-拓展螺烯,实现了“一个噻吩环编辑为两个苯环”的高效转化。该方法不仅绕过了传统多步合成的繁琐步骤和区域选择性难题,也为功能化手性光电材料的构建开辟了新路径。
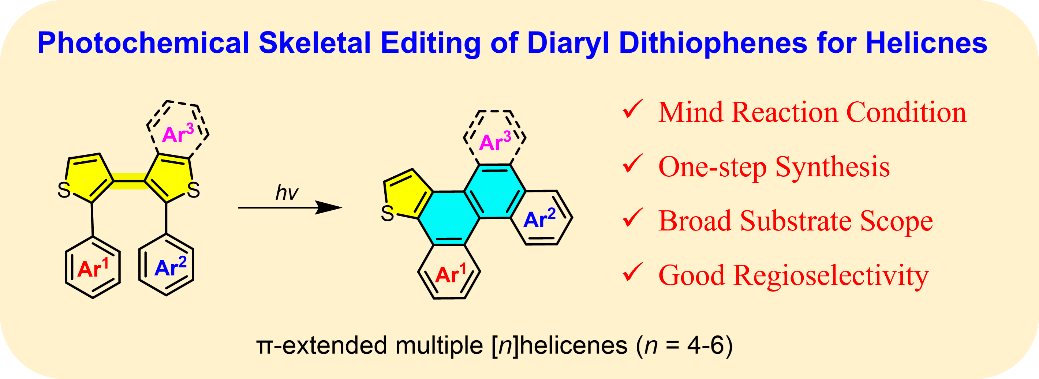
骨架编辑正在推动合成化学从传统的“成键/断键”范式,转向直接在分子骨架上进行原子级别的“改写”。尽管在简单芳香体系中通过插入或删除单个原子已取得进展,但由于C-S键的惰性以及缺乏温和、直接的骨架重构方法,对复杂功能分子中的硫杂环进行编辑仍极具挑战性。螺烯是一类具有独特螺旋手性的多环芳烃,在手性识别、不对称催化和圆偏振发光(CPL)领域备受关注。经典的Mallory光化学合成法依赖二苯乙烯类前体的逐步环化,往往面临结构多样性受限和区域选择性难以预测的困境。研究团队设计了一种易于获得的二芳基联二噻吩作为关键前体,利用光化学骨架编辑实现了前所未有的“选择性噻吩-苯环交换”反应(图1)。该反应在光照条件下,通过级联光环化、C-S键断裂、第二次环化及脱硫,在一步操作内同时完成两个苯环的构建和一个噻吩环的开环转化。
方法发展与底物拓展:研究人员以二萘基联噻吩为前体,通过光化学方法构筑螺烯结构,单晶结构明确证实 2a 是一种不对称的π-拓展螺烯,由稠合的碳[5]螺烯和硫[4]螺烯组成(图2)。这种骨架变化证实了反应路径与经典的光环化反应有根本差异,验证了二芳基联噻吩骨架成功重构为π-拓展螺烯结构的可行性。随后研究人员通过改变二芳基联噻吩的芳基取代基(如苯基、萘基、芘基、菲基等),以中等至良好的产率获得了一系列π-拓展螺烯(图3-5),展现出广泛的底物适应性。更重要的是,该方法能够选择性控制环化位点,解决了传统光合成中常见的区域异构体混合物问题。
机理研究:为了阐明反应机制,研究人员进行了一系列系统的对照实验和理论计算(图6-9)。通过对称二芳基联噻吩及非对称二芳基联噻吩底物环化位点的理论计算及实验验证为关键中间产物(如1ab和3aa)的形成提供了有力证据。结果表明,反应首先经历区域选择性的光环化,形成含硫[4]螺烯螺烯的中间体;随后发生C-S键的断裂和重排,最终完成第二次环化并脱硫。
手性光学性质:所得π-拓展螺烯表现出优异的手性光学性质。圆二色(CD)光谱和圆偏振发光(CPL)表明,这些螺烯分子具有显著的手性光学活性,其发光不对称因子(|glum|)达到了10⁻³量级(图10)。这表明该骨架编辑策略不仅是一种合成方法学上的创新,更为制备高性能手性发光材料提供了直接的技术路径。
王华教授团队开发一种光化学构筑螺烯的新方法,通过“光化学选择性骨架编辑”策略,实现了二芳基联噻吩向π-扩展螺烯的一步转化。该方法不仅提供了一种合成复杂π-扩展螺烯的简洁途径,更重要的是展示了骨架编辑在构建高阶复杂共轭分子体系中的巨大潜力。该工作为未来设计其他类型的“硫杂环编辑”反应及功能性多环芳烃指明了方向。相关研究工作发表在Chemical Science(DOI: 10.1039/D6SC01717G)。河南大学王光霞副教授、马志英博士和王华教授为论文通讯作者,河南大学硕士研究生石晓利和梅玲为论文第一作者。该研究工作得到了国家自然科学基金项目(22471061, 22271076和U20042132)的资助。
论文信息:
Photochemical Skeletal Editing: One-Step Transformation of Diaryl Dithiophenes into Regiodefined Helicenes
Xiaoli Shi, Ling Mei, Chenxi Dong, Chunmei Zhao, Chen Chen, Yimin Xu, Wan Xu, Chunli Li, Guangxia Wang* Zhiying Ma* and Hua Wang*
Chem. Sci., 2026, DOI: 10.1039/D6SC01717G
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




