【ACS Catal.】Keiji Maruoka等团队:光氧化还原/镍双重催化实现对映选择性C(sp³)−C(sp³)交叉偶联反应

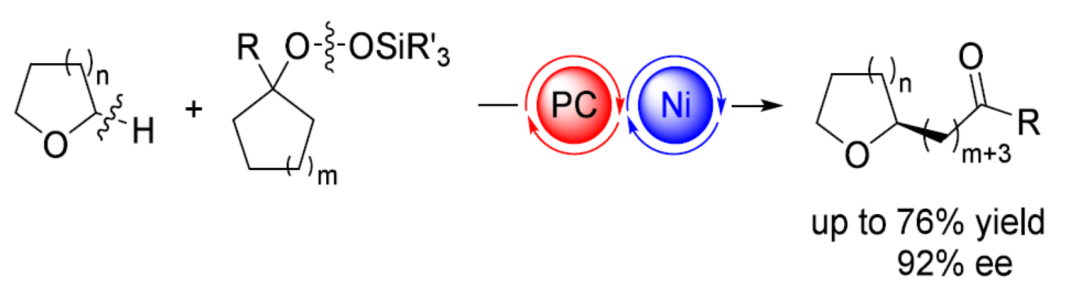
对映选择性C(sp³)−H键官能团化是合成高价值手性分子的重要途径。然而,在无导向基团参与的条件下,通过烃类底物直接构建不对称C(sp³)−C(sp³)键仍具有挑战。近日,日本京都大学Keiji Maruoka与Jia-Hao Xie团队开发了一种光氧化还原-镍双重催化体系,实现了氧杂环化合物(oxacycles)与烷基硅基过氧化物(alkylsilyl peroxides)之间的对映选择性C(sp³)−C(sp³)交叉偶联反应。相较于其他自由基前体,烷基硅基过氧化物的反应活性可通过硅取代基的调整实现精细调控。手性镍催化剂可高效实现对映选择性烷基-烷基自由基交叉偶联,获得一系列对映体富集的氧杂环化合物。相关研究成果发表在ACS Catal.上(DOI: 10.1021/acscatal.6c00536)。
在过去的几十年中,C(sp³)−H键的对映选择性官能团化已成为一种高效的策略,能够以原子与步骤经济性的方式,从易得的烃类底物中直接合成高价值的手性分子(Scheme 1A)。尽管C(sp³)−H键官能团化存在C−H键的高键解离能以及难以精确控制区域和对映选择性等挑战,但通过过渡金属催化导向基团辅助C−H活化、协同式金属卡宾/氮宾C−H插入及氢原子转移(HAT)等策略,该领域已取得重大进展。相比之下,金属催化导向基团辅助C−H活化和协同金属卡宾/氮宾C−H插入通常需要高温、贵金属催化剂或配位导向基团,而HAT途径能在温和条件下高效断裂C(sp³)−H键,通常无需上述苛刻条件。近年来,双重光氧化还原/镍催化体系已成为一种新型策略,可促进氢原子转移过程,实现C(sp³)−C键的对映选择性构建(Scheme 1B)。其中,对于烃类底物参与的催化对映选择性构建C(sp³)−C(sp²)键的反应(如芳基化、烯基化及酰基化)已有大量的研究报道,但对于C(sp³)−C(sp³)键的对映选择性构建仍具有挑战。2024年,霍浩华课题组开发了一种精妙的光氧化还原/镍双重催化体系,利用易得的氧化还原活性酯作为偶联底物,实现了α-酰胺基C(sp³)−H键的对映选择性烷基化反应。2025年,孔望清等课题组报道了一种精妙的镍催化对映选择性烷基化方法,通过氧杂环化合物的官能团化构建C(sp³)−C(sp³)键(Scheme 1C)。在此转化过程中,烯烃作为烷基化试剂,而DTBP充当自由基引发剂,实现在无光条件下从氧杂环化合物中产生自由基。然而,涉及小分子氧杂环化合物的光催化对映选择性构建C(sp³)−C(sp³)键,仍有待进一步的开发。近日,日本京都大学Keiji Maruoka等团队开发了一种光氧化还原-镍双重催化体系,实现了氧杂环化合物与烷基硅基过氧化物之间的对映选择性C(sp³)−C(sp³)交叉偶联反应,合成了一系列对映体富集的氧杂环化合物(Scheme 1D)。
首先,作者以四氢呋喃(1,作为底物与溶剂)与(1-苯基环戊基)(三甲基硅基)过氧化物(2)作为模型底物,对反应条件进行了大量的筛选(Table 1)。筛选结果表明,当以2ac作为底物,NiCl₂·DME作为金属催化剂,L1作为手性配体,Ir[dFCF₃ppy]₂(dtbbpy)PF₆作为光催化剂,K₂CO₃作为碱,蓝色LEDs作为光源,在室温下反应,可以76%的分离收率得到产物3a,ee为92%。
在获得上述最佳反应条件后,作者对底物的范围进行了扩展(Table 2)。首先,多种不同环尺寸的烷基硅基过氧化物,均可顺利进行反应,获得相应的产物3a-3f,收率为24-76%,ee为87-92%。其次,当底物2中的R为不同电性取代的芳基、萘基、杂芳基与烷基等时,也与体系兼容,获得相应的产物3g-3u,收率为27-72%,ee为83-92%。1-茚酮衍生的过氧化物,可以33%的收率得到产物3v,ee为88%。当使用硅基过氧缩醛作为自由基前体时,观察到适度的反应性和对映选择性,如3w和3x。在优化的条件下,四氢吡喃和氧杂环丁烷,也是合适的底物,如3y和3z。然而,对于其他氧杂环化合物(如氧杂环庚烷、四氢-4H-吡喃-4-酮、四氢呋喃-2-甲酸甲酯及15-冠-5-醚等)均未能生成目标产物。值得注意的是,通过钴催化选择性C−C键断裂及烯烃硅基过氧化反应制备的烷基硅基过氧化物(6和8),在该体系中同样适用,分别获得产物7和9。同时,以烯烃10为底物,通过一锅法也可直接制备产物7。硅基过氧化物11在标准条件下也与体系相容,可以47%的收率和82%的ee得到酯产物12。12可直接水解,然后与2-苯酰氯反应,可以77%的收率和81%ee得到化合物13。
最后,作者对反应的机理进行了研究(Scheme 2)。自由基实验结果表明,反应同时涉及形成α-氧代烷基自由基和一级烷基自由基的过程,其分别源自四氢呋喃与烷基硅基过氧化物(Scheme 2A)。通过对不同镍前体的对照实验结果表明,氯自由基在此转化过程中充当氢原子转移试剂,且镍前体的选择对反应效率至关重要(Scheme 2B)。通过相关的电化学数据,进一步证实了光诱导电子转移过程存在还原淬灭机理。Stern-Volmer淬灭研究进一步证实了这一观点,该研究表明2ac对光催化剂的发光未产生显著淬灭作用,有效排除了能量转移路径的可能性。基于上述的研究以及前期的研究,作者提出了一种合理的反应机理(Scheme 2C)。首先,在还原条件下可形成镍(I)配合物(I),其通过单电子转移还原2ac,生成镍(II)配合物(II)及烷氧自由基(III)。其次,自由基(III)经β-断裂,生成带有酮基侧链的烷基自由基(IV)。自由基(IV)与[IrII]还原中间体(II)形成的镍(I)配合物偶联,生成镍(II)配合物(V)。同时,[IrIII]在蓝色LED光照下发生光激发,生成激发态[IrIII]*,其与中间体(V)进行单电子转移,生成还原态[IrII]与镍(III)配合物(VI)。随后,配合物(VI)经光解,生成氯自由基和镍(II)配合物(VII)。氯自由基从四氢呋喃攫取氢原子,生成的α-氧代烷基自由基与镍(II)配合物(VII)结合,生成镍(III)中间体(VIII)。最终,经还原消除反应生成对映体富集的产物(3a)并再生镍(I)物配合物(I),从而完成催化循环的过程。
日本京都大学Keiji Maruoka与Jia-Hao Xie团队开发了一种含氧杂环化合物的对映选择性C(sp³)−C(sp³)交叉偶联方法。该方法无需外源导向基团,通过光氧化还原与镍催化的协同作用实现。烷基硅基过氧化物作为可调控的自由基前体,其反应活性可通过硅取代基的变化进行调节。手性镍催化剂促进了烷基-烷基自由基的对映选择性交叉偶联,从而高效合成了一系列对映体富集的含氧杂环化合物。
论文信息:
Enantioselective C(sp³)−C(sp³) Cross-Coupling between Oxacycles and Alkylsilyl Peroxides via a Dual Photoredox/Nickel Catalytic System
Jia-Hao Xie, Terumasa Kato, Keiji Maruoka
Romi S. Aggarwal, Wenbin Mao, Craig M. Robertson, John F. Bower
ACS Catal. DOI: 10.1021/acscatal.6c00536
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




