【Org. Lett.】石河子大学蔡志华、杨盛超/华东师范大学刘路:光诱导串联沃尔夫重排/C−S键插入反应模块化合成四取代联烯酸硫酯
联烯(allenes)作为一类重要的结构基元,广泛存在于天然产物和生物活性分子中,同时也是有机合成中极具价值的合成砌块。过去几十年间,联烯化学蓬勃发展,通过联烯负离子、联烯正离子、联烯自由基等中间体构建结构多样的联烯化合物取得了长足进展。其中,末端炔烃与醛或酮的联烯化反应(allenation of terminal alkynes,ATA)是构建取代联烯最为直接的策略之一,而卡宾化学的发展进一步拓展了该类反应的应用边界。然而,联烯酸硫酯(thioallenoates)的合成仍主要依赖于传统的多步反应策略,如Wittig反应,其原子经济性较差,发展高效、高原子经济性的合成方法仍是该领域亟待突破的挑战。
另一方面,重氮化合物介导的C−S键断裂与重组是构建含硫有机分子的重要手段。经典的[2,3]-σ迁移重排(Doyle−Kimse重排、Sommelet−Hauser重排)和[1,2]-σ迁移重排(Stevens重排)通过硫醚与重氮化合物形成叶立德中间体,进而发生重排构建C(sp³)−S键。近年来,刘路课题组及其他研究团队相继报道了一系列新颖的[1,4]-迁移反应,成功构建了烯基和芳基C(sp2)−S键。然而,通过卡宾中间体构建酰基C(sp²)−S键的研究未见报道。
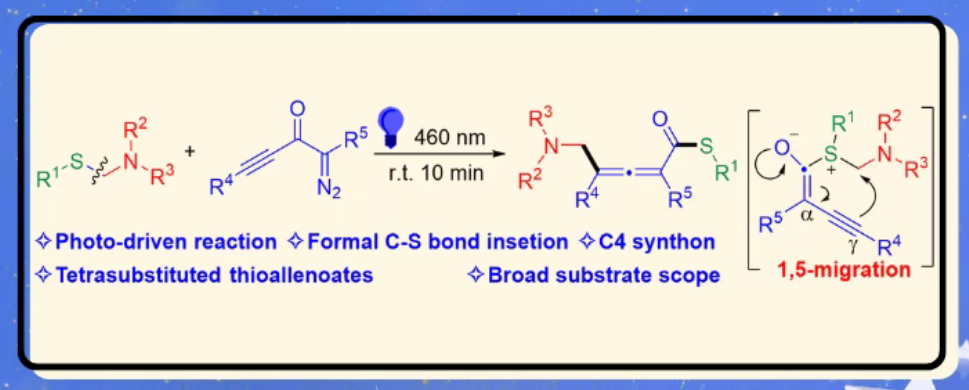
炔基重氮酮作为一类多功能合成试剂,可以充当C1-C4合成子参与多种键插入反应。基于刘路课题组在卡宾化学和联烯合成领域的持续兴趣,作者设想炔基重氮酮可作为C4合成子,与N,S-缩醛发生插入反应,构建四取代联烯酸硫酯。该转化面临化学选择性和区域选择性的双重挑战:N,S-缩醛具有氮和硫两个亲核位点,硫原子进攻(路径a)将得到C−S键插入产物,而氮原子进攻(路径b)则得到C−N键插入产物;此外,1,5-迁移过程还涉及α-和γ-区域选择性问题,仅γ-选择性路径能生成目标联烯产物(图1e)。
石河子大学硅化工课题组与华东师范大学刘路课题组近期联合报道了光诱导的炔基重氮酮与N,S-缩醛的串联沃尔夫重排/C−S键插入反应,成功实现了四取代联烯酸硫酯的模块化合成。该策略具有反应条件温和、时间短、底物适用范围广、可放大等优点。相关成果发表于Organic Letters(DOI: 10.1021/acs.orglett.6c00595)。
作者以N,S-缩醛1a和炔基重氮酮2a为模板底物,确定了最佳反应条件:氯仿(CHCl₃)为溶剂,5 Å分子筛为添加剂,在氩气氛围下以2 W 460 nm LED光照10分钟,目标产物3a的分离收率为90%。并在最佳反应条件下考察了底物的适用性(图2)。首先,作者考察了N,S-缩醛中硫取代基部分的电子效应对反应的影响,苯环上带有不同电性取代基的N,S-缩醛均能顺利反应。无论是含有给电子基团(如4-甲基、2-甲基、4-甲氧基)还是吸电子基团(如4-氯、4-溴)的底物,都能以80%-99%的优异产率得到相应的目标产物。值得注意的是,空间位阻对该转化未产生明显影响,如2-甲基取代的底物可以以同样优异的产率得到产物3b。接下来,对于烷基取代的N,S-缩醛,无论是硫代-正十八烷基还是硫代-环戊烷基取代的底物,均表现出良好的反应活性,分别以82%和86%的产率得到相应的联烯产物。此外,还考察了N,S-缩醛中胺基部分对反应的影响。发现,带有不同N,N-二取代基的N,S-缩醛均能适用于该转化,以74%-96%的产率顺利得到相应的联烯产物。随后,保持N,S-缩醛不变,考察了炔基重氮酮2的底物适用范围。当R4位为芳基时,无论苯环上带有给电子基团还是吸电子基团,均能以61%-99%的产率得到相应产物。值得注意的是,当R4位为烷基时,炔基重氮烷基酮类底物同样适用于该转化,分别以87%和99%的产率顺利得到联烯产物。R5位带有不同苯基取代基的炔基重氮酮底物也能顺利反应,以63%-99%的产率成功获得目标产物。当R4,R5位均带有不同苯基取代基的重氮底物也能顺利反应得到产率为87%的联烯产物。
为验证该合成策略的实用性,作者在标准条件下进行了克级规模放大反应。得到了0.488 g产物3a,分离收率88%(图3 a)。此外,作者对四取代联烯酸硫酯进行了衍生化研究(图3 b):化合物3f与正丁基锂(n-BuLi)反应,经双正丁基加成得到烯丙基酮4,收率50%;化合物3m与N-碘代丁二酰亚胺(NIS)反应,以93%的收率得到四取代呋喃5,其结构通过单晶X射线衍射分析确认。
基于前期研究,作者提出了可能的反应机理(图4)。首先,炔基重氮酮2a在光照射下发生沃尔夫重排,生成活性炔基烯酮中间体I;随后,N,S-缩醛1a通过硫原子对中间体I进行亲核加成,形成中间体II;最后,中间体II经历1,5-迁移,释放目标产物3a。
综上,本文发展了一种温和、无金属的光诱导串联沃尔夫重排/亲核加成/1,5-迁移反应,实现了N,S-缩醛与炔基重氮酮的骨架编辑,模块化合成了多种结构多样的四取代联烯酸硫酯。该策略具有良好的底物适用范围和官能团兼容性,为硫代联烯类化合物的高效合成提供了新途径。目前,课题组正致力于进一步拓展炔基重氮酮和N,S-缩醛在有机合成中的应用。
本研究的第一作者为石河子大学与华东师范大学联合培养研究生赵学迪和华东师范大学硕士研究生倪宇豪。华东师范大学刘路教授、石河子大学蔡志华副教授、以及杨盛超教授为本文的通讯作者。研究工作得到了国家自然科学基金、新疆维吾尔自治区重点研发计划等经费资助。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




