ACS Catal.:钴/光氧化还原催化、膦介导的未活化烷基羧酸的碳同位素交换
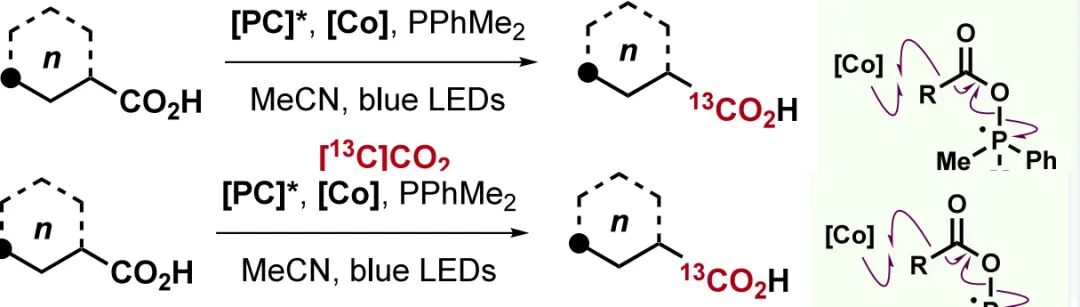
碳同位素交换(CIE)反应已成为一种有用的同位素标记策略,为合成药物与农药研发以及医学成像所需的化合物提供了一种便捷的传统合成替代路线。使用同位素标记CO₂对烷基羧酸进行的CIE过程,通常局限于紧邻羧基处带有稳定阴离子的基团(即苄基、亚氨基或酮酸)的底物,或者需要对底物进行预活化以发生脱羧和交换。为了拓展CIE方法的范围,作者致力于开发一种机理不同的过程,利用光氧化还原催化结合膦介导,实现对未活化烷基羧酸的直接标记。最近,美国强生创新医药(Johnson & Johnson Innovative Medicine)Fengbin Song课题组与加拿大阿尔伯塔大学(University of Alberta)Rylan J. Lundgren课题组联合报道了在钴催化剂存在下,烷基羧酸在低压[¹³C]CO₂(1 atm,约3当量)条件下发生的钴/光氧化还原催化、膦介导的CIE反应。与基于成熟的膦介导羧酸自由基脱氧方法而得出的初始机理假设相反,该反应似乎是通过羧酸底物首先脱羧,随后进行钴催化羧化来进行的。值得注意的是,对照实验揭示,在CIE反应过程中,通过光氧化还原催化、膦介导的CO₂还原生成了大量的CO。相关成果发表在ACS Catal. 2026, DOI: 10.1021/acscatal.5c08302上(Scheme 1)。
首先,作者以羧酸1为底物对反应进行探索(Figure 2)。通过一系列条件筛选,作者发现当使用2% Ir-1, 5% Co-1, PPhMe₂ (2.0 equiv), [¹³C]CO₂(1 atm,约3当量),在MeCN [0.1 M]中蓝色LED光照下室温反应20小时,可以以44%的¹³C标记率和42%的产率得到相应的¹³C标记产物[¹³C]1(entry 1)。控制实验表明在没有Ir-1、Co-1、PPhMe₂以及光照的条件下均无法实现¹³C标记。
鉴于反应具有新颖性质,作者进行了机理研究(Figure 3)。监测显示反应存在约4–6小时的诱导期,期间无底物消耗。随后¹³C掺入比例稳步增加,但产率因酸的不稳定性逐渐下降,标准反应时间即为平衡二者所致。反应中检测到醛及氧化膦,证实了酰基自由基中间体的生成。顶空气体分析检出大量CO,对照实验表明CO源于CO₂的光催化还原(需Ir-1、膦及蓝光协同),而非底物脱羰。作者通过同位素标记实验进一步证实,利用¹³CO₂反应生成的¹³CO进行钯催化氨基羰基化,成功合成了高标记率的酰胺产物。同位素洗出实验中,¹³C-1在未标记CO₂下反应释放出¹³CO₂,确证了脱羧途径。气相分析显示生成的CO主要为¹³CO,排除了底物脱羰的主导地位。此外,钴催化剂的存在抑制了磷酰基自由基的β-断裂及酰基自由基捕获,避免了副反应发生。综上,该CIE反应机理涉及光催化氧化膦产生膦自由基阳离子,其与羧酸结合生成磷酰基自由基,经钴介导的脱羧α-断裂生成钴-烷基物种,最终发生还原羧化。
与作者的实验观察相符的总体机理如Figure 4所示。未活化烷基羧酸的直接CIE可能通过磷酰基自由基的脱羧α-断裂,随后发生钴-烷基中间体的还原羧化来实现。具体而言,Ir(III)光催化剂的激发会产生激发态Ir(III)物种 [Ir-1 *Ered Ir(III)/Ir(II) = +1.21 V vs SCE in MeCN],正如其他研究所证实的那样,该物种可被PPhMe₂ [Eox = +0.89 V vs SCE in MeCN] 还原淬灭,从而生成基态Ir(II)还原剂和膦自由基阳离子。随后,羧酸底物可与膦自由基阳离子反应生成磷酰基自由基i1。磷酰基自由基的钴介导脱羧α-断裂将生成CO₂和PPhMe₂,以及有机金属Co(III)物种。随后,Ir(II)光催化剂 [Ir-1 Eox Ir(II)/Ir(III) = −1.37 V vs SCE in MeCN] 对Co(III)烷基配合物 [Co(III)(salen) Ered Co(III)/Co(II) = −0.022 V vs SCE in DMF] 进行单电子还原,将生成有机金属Co(II)烷基中间体。随后[¹³C]CO₂的插入会生成作为Co(II)羧酸盐的标记产物,该产物经质解后会释放出¹³C标记的羧酸产物。鉴于该反应的还原特性,在此条件下也很可能生成Co(I)中间体。相反,通过还原性自由基极性反转(RRPCO)机理形成未稳定的碳负离子是不太可能的,因为基态Ir(II)还原剂 [Ir-1 Eox Ir(II)/Ir(III) = −1.37 V vs SCE in MeCN] 还原未稳定的烷基自由基 [•CH₂CH₃ Ered = −2.23 V vs SCE in DMF] 将是高度吸能的,因而在热力学上是不利的。
为了进一步阐明钴催化剂的存在如何使磷酰基自由基i1偏离通常观察到的β-断裂途径,作者进行了一些初步的DFT计算。在无钴存在的情况下,计算得到的ΔG值表明,在非催化途径中,β-断裂优于α-断裂(14.3 vs 24.6 kJ/mol;Figure 5)。因此,以羧酸底物1作为模型,发生β-断裂生成相应酰基自由基在热力学上更为有利(高出约10 kJ/mol),这与先前开发的磷酰基自由基反应中观察到的产物相一致。相反,在Co(salen)催化剂存在下,由脱羧α-断裂生成的Co-1-烷基中间体将该过程的ΔG显著降低至-58.2 kJ/mol,为观察到的反应提供了驱动力。然而,鉴于在标准条件下同时观察到了α-断裂和β-断裂的产物,表明这两条途径在动力学上均是可行的。值得注意的是,计算发现Co-1的芳基衍生物比源自底物1的伯烷基衍生物具有高得多的能量,这表明此类底物可能缺乏实现有效CIE的驱动力,反应的底物范围研究也证实了这一点。
最后,作者对底物范围进行了考察(Figure 6)。氢肉桂酸([¹³C]2)及其相应的富电子([¹³C]3、[¹³C]4)和缺电子([¹³C]5)衍生物被成功标记,¹³C掺入率为22–61%,产率中等(24–37%)。较长链的芳基脂肪族酸顺利发生CIE反应,以51%的¹³C掺入率和28%的产率得到目标标记产物[¹³C]6。N-Boc保护的烷基胺产物[¹³C]7也通过该标记过程获得,¹³C掺入率为29%,产率为31%。在标准条件下,顺-蒎酮酸([¹³C]8)被高效标记,目标产物的¹³C掺入率达65%,产率为21%,且未观察到立体化学的流失。此外,标记的β-CF₃羧酸([¹³C]9)能够以41%的¹³C掺入率和42%的产率获得。饱和杂环也同样适用于该标记过程,包括含有哌啶基([¹³C]10,40% ¹³C,24%产率)、四氢呋喃基([¹³C]11,57% ¹³C,24%产率)、四氢吡喃基([¹³C]12,38% ¹³C,18% 产率)和氮杂环丁基([¹³C]13,16% ¹³C,32% 产率)结构的产物。复杂目标分子阿托伐他汀缩酮(14)发生了羧基CIE反应,¹³C掺入率为38%,分离产率为57%。未能发生有效标记(¹³C<5%)的底物类别包括α-杂原子酸、芳基酸以及烯基/炔基酸。尽管产物产率和同位素掺入水平仍然有限,但使用已知方法无法直接由未衍生化的前体来制备此类标记的烷基羧酸产物。
Fengbin Song课题组与Rylan J. Lundgren课题组联合建立了一种具有独特机理的碳同位素交换方法,能够直接从未修饰的烷基羧酸出发进行反应。机理研究得出由磷酰基自由基-羧酸盐发生脱羧α-断裂生成钴-烷基物种,该物种能够在低压[¹³C]CO₂条件下发生还原羧化。此外,作者还观察到了意想不到的光诱导CO₂还原为CO的现象,并确定该过程是由铱基光催化剂与烷基膦协同促进的。这些研究对于开发碳同位素交换反应以及光氧化还原/膦介导的羧酸反应均具有重要价值。
论文信息:
Cobalt/Photoredox-Catalyzed, Phosphine-Mediated Carbon Isotope Exchange of Unactivated Alkyl Carboxylic Acids
Michael G. J. Doyle, Xingya Zhao, Fengbin Song,* Rhys Salter, Ismael A. Elayan, Alex Brown, and Rylan J. Lundgren*




