【J. Org. Chem.】南京农业大学邓红平教授:光致氧化还原/布朗斯特碱协同催化双环[1.1.0]丁烷的顺式烷基化-酯基化反应
近五年来,可见光诱导的双环[1.1.0]丁烷(BCB)双官能团化反应逐渐发展成为构建多取代环丁烷的高效策略之一。然而,该反应的非对映选择性调控仍是该领域长期存在的核心挑战,迄今为止仅有极少数报道能够实现优异的非对映选择性控制。近日,南京农业大学邓红平教授课题组利用光致氧化还原/布朗斯特碱协同催化策略,以丙二酸二酯为双官能团化试剂,在温和条件下成功实现了双环[1.1.0]丁烷(BCB)的顺式烷基化-酯基化反应。该体系对多种双环[1.1.0]丁烷衍生物及1,3-二羰基化合物均展现出优异的底物普适性。相关研究成果发表于The Journal of Organic Chemistry (DOI: 10.1021/acs.joc.6c00354) 。
1,3-二羰基化合物(如丙二酸二酯等)作为一类常见的亲核试剂,被广泛应用于有机合成中。此外,在可见光催化条件下,1,3-二羰基化合物能够实现极性翻转,作为亲电性烷基自由基参与非活化烯烃、炔烃等的官能团化反应。根据可见光催化条件下1,3-二羰基化合物的活化机理,可大致分为三种类型:(1)光致氧化还原催化;(2)光致氧化还原/氢原子转移(HAT)协同催化;(3)光诱导能量转移催化,先形成高活性烯醇中间体,再与非活化烯烃发生de Mayo反应。与前两种反应类型不同,在de Mayo反应中1,3-二羰基化合物可作为双官能团化试剂,但现有报道主要集中于1,3-二酮与β-酮酸酯类化合物,关于丙二酸二酯参与的de Mayo类反应尚未有报道。基于此,本课题组结合前期研究,利用光氧化还原/布朗斯特碱协同催化策略,以丙二酸二酯为双官能团化试剂,实现了BCB的顺式烷基化-酯基化反应,以良好到优秀的收率得到一系列1,6-二羧酸二酯类衍生物。该催化体系对多种BCB衍生物及1,3-二羰基化合物均能表现出良好的兼容性。
作者以3-苯基双环[1.1.0]丁烷-1-羧酸甲酯和丙二酸二甲酯为原料,对反应条件进行了优化。结果表明,在2 mol% Ir(ppy)2(dtbbpy)PF6为光催化剂、20 mol%碳酸铯为布朗斯特碱催化剂、四氢呋喃为溶剂、在蓝色LED室温照射24小时的最佳反应条件下,以84%的收率及优秀的区域选择性得到顺式烷基化-酯基化产物。
在最优反应条件下,作者考察了双环[1.1.0]丁烷的底物普适性。结果表明,该方法适用于各类酯基、酰胺基和酰基取代的双环[1.1.0]丁烷,以中等到良好的收率及优秀的区域选择性单一生成顺式烷基化-酯基化产物;对于苯基上带有各种官能团取代的BCB底物,反应同样能够顺利进行。
随后,作者在最优反应条件下考察了1,3-二羰基化合物的底物普适性。结果显示,三氟乙醇和苄醇衍生的丙二酸二酯均能很好地兼容该反应。对于对称或不对称的1,3-二酮衍生物,该反应同样展现出良好的兼容性。
通过一系列简单地转化,该顺式烷基化-酯基化产物能很容易地转化为相应的复杂的羧酸衍生物和酮类衍生物。
接着,作者利用一系列控制实验(开关灯实验、自由基捕获实验、荧光淬灭实验及循环伏安法测定反应物的氧化电势等)对反应的机理进行了详细研究。
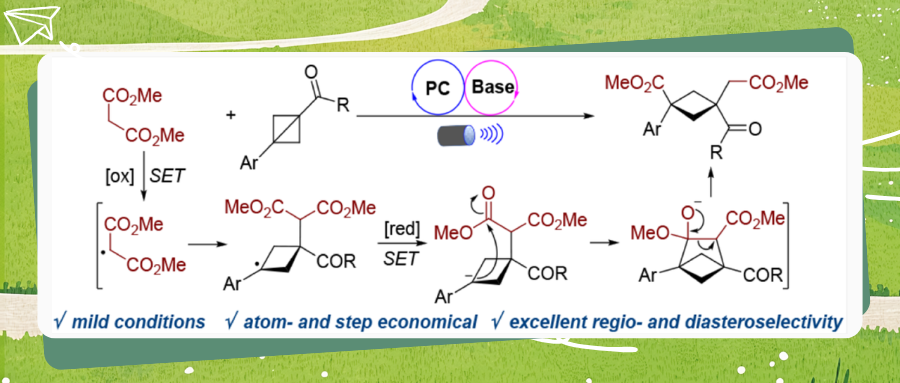
基于上述实验结果,作者提出了可能的反应机理。在碱性条件下,丙二酸酯2a的负离子被激发态光催化剂Ir(ppy)2(dtbbpy)PF6*单电子氧化,生成烷基中间体I。根据自由基极性匹配原则,亲电性自由基中间体I易于加成到BCB 1a的 C1–C3 σ 键中酯基取代的碳原子一端,形成亲核性苄基自由基中间体II。随后,中间体II被还原态光催化剂单电子还原,生成苄基阴离子中间体III,同时再生光催化剂。最终,苄基阴离子III依次经历逆Claisen酯缩合及质子化过程,生成目标产物3。
综上所述,本文发展了一种光致氧化还原/布朗斯特碱协同催化体系,以丙二酸二酯为双官能团化试剂,实现了双环[1.1.0]丁烷(BCB)的顺式烷基化-酯基化反应,以良好至优异的收率高选择性合成一系列环丁烷类1,6-二羰基化合物。该方法具有优异的区域及非对映选择性;底物普适性较广,可适应于多种双环[1.1.0]丁烷衍生物与1,3-二羰基化合物。该研究不仅拓展了丙二酸二酯在de Mayo类反应中的合成应用,也为选择性构建多取代环丁烷衍生物提供了新思路。
文章的共同第一作者为南京农业大学硕士研究生郑超艺和博士研究生洪洋(现为安庆师范大学讲师),邓红平教授为文章的通讯作者。研究工作得到了国家自然科学基金(21901121)和南京农业大学科研启动经费的资助。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




