【JACS】上海科技大学高得伟课题组:胺基自由基促进的光/镍协同催化构建C(sp³)–C(sp³)键
Suzuki-Miyaura偶联反应是构建C(sp²)–C(sp²)键的经典方法,因其优异的底物兼容性与适用性,已成为合成化学、药物研发及材料科学领域的核心工具。相比之下,C(sp³)–C(sp³)键作为sp³特征生物活性分子的关键结构单元,其高效、高选择性的构建仍是有机合成领域长期面临的重要挑战。核心难题在于:烷基频哪醇硼酸酯(APEs)自由基生成难度大、烷基亲电试剂反应活性低,且反应过程中存在竞争性的β-氢消除过程。因此,开发以低毒、稳定性的APEs为前体的C(sp³)–C(sp³)构建新方法,对推动有机合成方法学发展及促进药物分子创制具有重要的科学意义和应用价值。
上海科技大学高得伟课题组聚焦于“硼基转化过程中的立体选择性与反应活性调控”这一关键科学问题,在手性硼化合物的不对称合成及惰性烷基C–B键活化转化领域取得系列成果(Nat. Commun. 2026, 17, 1941; Angew. Chem. Int. Ed. 2025, 64, e202504224; Angew. Chem. Int. Ed. 2024, 63, e202318441; Angew. Chem. Int. Ed. 2023, 62, e202307447; Angew. Chem. Int. Ed. 2023, 62, e202312605; Sci. Adv. 2025, 11, eadz8755; CCS Chem. 2025, 7, 10.31635/ccschem.025.202505879; Nat. Commun. 2024, 15, 10810; Org. Lett. 2024, 26, 1595; J. Org. Chem. 2025, 90, 16584)。最近,该课题组利用胺基自由基活化APEs,并结合光/镍协同策略,经由卤原子转移过程,成功实现了惰性烷基硼酸酯与烷基卤化物的高效偶联反应。该方法反应条件温和,底物适用范围广,官能团耐受性优异,不仅可兼容游离醇羟基、酚羟基、羧酸等多种官能团,还能高效实现1,n-烷基双硼化合物的选择性烷基化、烯基化、炔基化与芳基化(图1)。
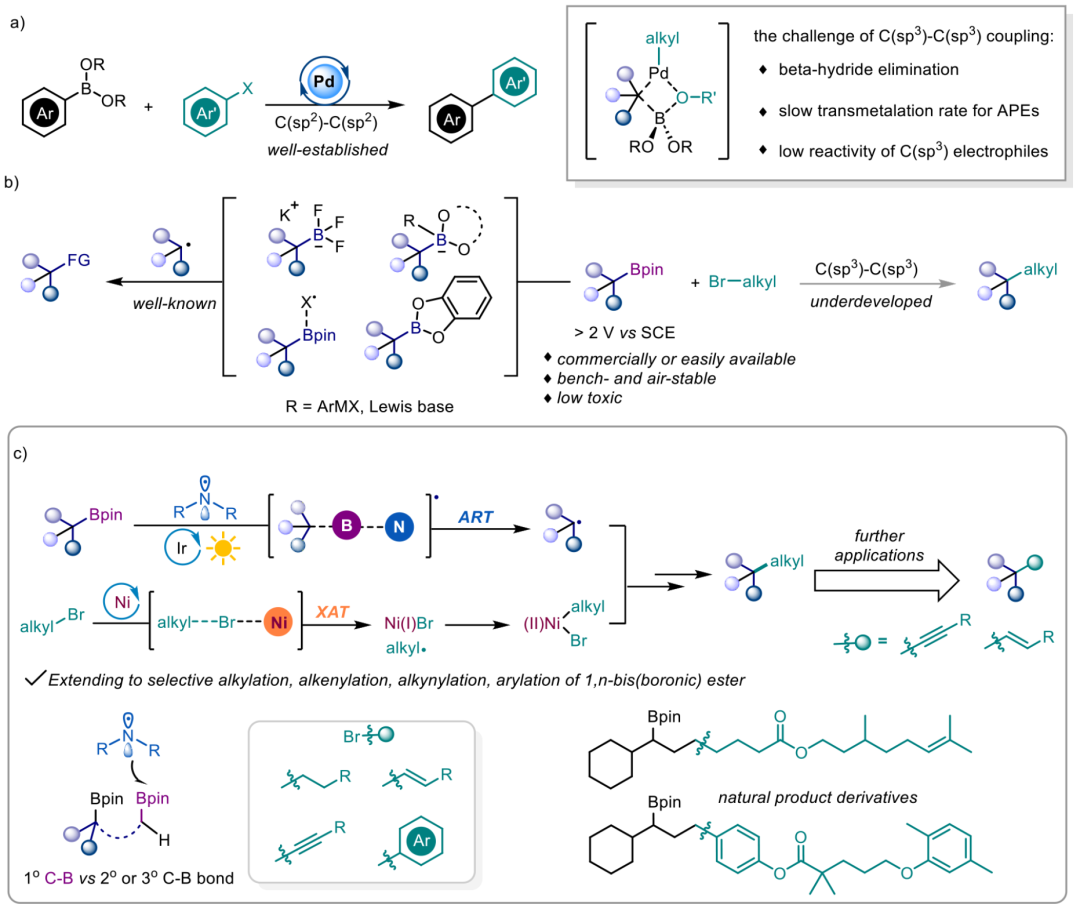
图1. 研究背景以及课题设想(图片来源:J. Am. Chem. Soc.)
作者以哌啶保护的烷基硼酸酯和叔丁基3-溴氮杂环丁烷-1-羧酸酯为模板底物,系统考察了镍源、胺基自由基前体、光催化剂等对反应收率的影响,最终确定了最优反应条件。在该条件下,目标产物分离收率可达80%,系列控制实验证明光催化剂、可见光光源、镍催化剂与仲胺自由基前体均为反应顺利进行的必需条件。底物范围拓展研究表明,该方法展现出优异的底物普适性与兼容性:可高效兼容环丁基、环己基、环庚基等环烷基溴化物及各类直链、支链的伯烷基溴化物,还能实现1,3-二溴丙烷的选择性单烷基化,保留的C–Br键可用于后续分子多样化修饰;游离羟基、羧酸等经典偶联反应中的敏感官能团在该体系中均能很好的兼容。各类环状、链状的伯、仲烷基硼酸酯均能顺利参与反应,甲基硼酸酯、甚至环己基硼酸也可直接作为偶联底物,进一步拓宽了反应的适用范围。此外,该方法无需额外优化反应条件,可直接拓展至炔基化和烯基化反应,天然产物衍生的硼酸酯、含强酸性酚羟基的底物也能高效参与反应,为复杂天然产物和药物分子的后期官能化提供了高效工具(图2)。
课题组进一步实现了1,n-双硼酸酯的选择性官能化,胺基自由基可依据C–B键的空间位阻和电子环境的细微差异,精准识别与选择性活化一级C–B键,优先在一级C–B键位点发生烷基化、烯基化、炔基化和芳基化反应,且兼容烷基、苯基、酯基、氰基、烯烃、羟基、羧基等多种官能团,底物中的已有立体中心不会对反应收率和选择性产生不利影响。杂芳环作为药物化学中常见的结构砌块,在该体系中同样表现出优异的反应性,即使是吡啶、嘧啶等强配位的杂环结构,也能顺利地参与偶联反应,突破了传统偶联反应的相关限制,凸显了该方法的实际应用价值(图3)。
为深入阐释反应机理,课题组开展了系统的机理研究,包括自由基捕获实验、紫外-可见吸收光谱分析、循环伏安法测试、Stern-Volmer荧光淬灭实验,并结合密度泛函理论(DFT)计算进行深入分析(图4)。实验证明,该反应遵循自由基反应路径:激发态的光催化剂氧化仲胺生成胺基自由基正离子,脱质子后形成关键的胺基自由基,进而与APEs硼中心空p轨道发生相互作用,发生自由基转移生成烷基自由基。镍(0)催化剂与烷基溴化物发生卤原子转移过程,生成烷基镍(II)物种。胺基自由基对1,n-烷基双硼酸酯中的一级C–B键的活化能比二级C–B键低3.0 kcal/mol,是实现位点选择性的根本原因。体系中烷基镍(III)中间体经还原消除步骤生成目标产物,为整个反应的速率决定步骤,其自由能垒为20.3 kcal/mol。
为验证该方法的实用性,作者开展了一系列放大实验、连续流实验和后续转化研究:流动化学证明,即使是放大至5 mmol,可在2小时内以73%的分离收率得到目标产物。此外,6 mmol规模的批量放大实验收率达78%,且反应效率和选择性无明显降低;反应产物中的烯烃结构和未反应的C–B键可实现Wacker氧化、氢硼化、烯烃复分解、烯丙基化、酰基化、脱硼炔基化、C–N键构建、C–S键构建等多种后续衍生化反应,为后期转化提供了多种可能性。此外,该方法还成功应用于抗血小板药物替罗非班的简洁高效合成,无需对分子中的羟基进行保护/脱保护操作,直接以含游离羟基的烷基溴化物为底物,经三步反应以55%的总收率得到目标产物,相比传统方法避免了羟基保护/脱保护步骤(图5)。
综上所述,该研究将胺基自由基活化策略与光/镍协同催化体系相结合,成功实现了惰性烷基硼酸酯的C(sp³)–C(sp³)偶联。该方法具有反应条件温和、反应效率高、底物适用范围广以及优异的官能团兼容性等优点。这一策略不仅为C(sp³)–C(sp³)键的构建提供了一种全新的合成工具,也为1,n-双硼酸酯的位点选择性官能化开辟了新路径。此外,该方法可进一步拓展至烯基化、炔基化及芳基等多种转化,在药物分子合成、复杂天然产物全合成及功能材料制备等领域展现出重要的应用前景。
这一成果近期发表在Journal of the American Chemical Society上,上海科技大学博士研究生张玉文为本文的第一作者,高得伟教授为通讯作者,上海科技大学为唯一通讯单位。
论文信息:
Aminyl Radical-Enabled Photoredox/Nickel-Catalyzed C(sp³)–C(sp³) Suzuki-Miyaura Cross-Coupling via Halogen-Atom Transfer Strategy
Yu-Wen Zhang, Chong-Lei Ji, Ang Chen, Jia-Xuan Bi, and De-Wei Gao*
J. Am. Chem. Soc. 2026, 148, doi/10.1021/jacs.6c00526.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




