【JOC】河南工业大学袁金伟课题组:可见光驱动的芳乙炔基喹唑啉酮的自由基胺化/环化合成磺酰胺化喹啉并喹唑啉衍生物
近日,河南工业大学袁金伟课题组开发了一种高效简便的方法,用于合成磺酰胺基喹啉并[2,1-b]喹唑啉酮衍生物。即利用稳定易得的氨基吡啶鎓盐作为磺胺基自由基前体,开发了芳乙炔基喹唑啉酮的可见光驱动的自由基胺化/环化。在无氧化剂和添加剂的条件下成功合成了一系列磺胺基喹啉[2,1-b]喹唑啉酮。相关研究成果发表在J. Org. Chem(DOI: 10.1021/acs.joc.5c03167)。
磺胺类化合物是一类重要的含氮化合物。作为酰胺的经典生物等排体,它们在保持酰胺键结构相似性的同时,展现出优异的特性:强的氢键供体与受体能力、高的水解稳定性以及更大的极性表面积。凭借这种独特的理化与生物特性组合,磺胺类化合物已广泛应用于药物化学、材料科学、物理化学乃至化妆品行业。图中展示了具有生物活性的磺酰胺衍生物代表性实例。因此,将磺酰胺结构单元整合到不同分子骨架中,已成为药物研发与合成设计中的关键策略。然而,开发实用高效的磺酰胺骨架合成方法仍是当前面临的重要挑战。
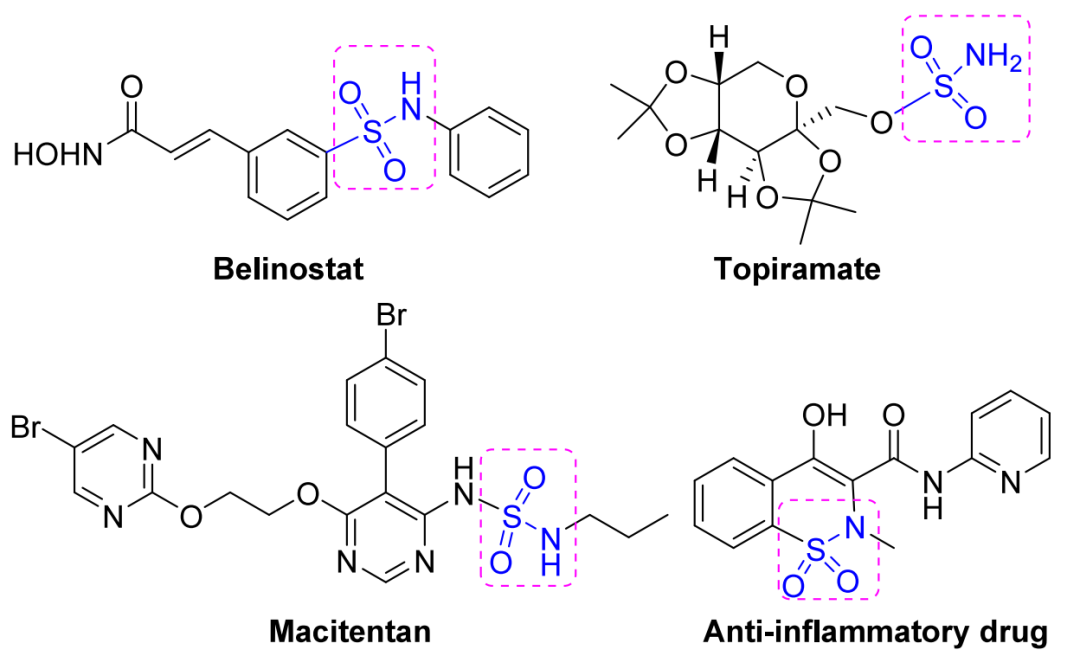
(图片来源:J. Org. Chem.)
含喹唑啉酮结构的杂环化合物存在于许多具有生物活性的天然产物以及药物分子中。特别是喹啉并[2,1-b]喹唑啉酮作为一种重要的分子骨架,因其广泛的生物活性和药用价值而备受关注。大量研究致力于开发高效合成策略以构建功能化喹啉[2,1-b]喹唑啉酮衍生物。其中,通过环化反应实现炔基喹唑啉酮的自由基引发串联功能化方法已得到广泛研究。采用该方法已成功合成多种氰烷基化、磺酰化、磷酸化、硫酰化、氟甲基化的喹啉[2,1-b]喹唑啉酮衍生物。但这些策略通常需要苛刻的反应条件,例如使用贵金属催化剂、氧化剂及高温环境。在分子中引入磺酰胺基等官能团,能够显著改善化合物的生物活性与成药性能,已成为新药分子设计的常用策略。以炔基喹唑啉酮为底物,通过光催化自由基串联反应合成磺酰胺化喹啉[2,1-b]喹唑啉酮衍生物的研究报道尚未见报道。
河南工业大学袁金伟课题组报道了一种无需氧化剂和添加剂条件下,利用可见光驱动的N-氨基吡啶盐与喹唑啉酮进行自由基磺酰胺化/环化反应。该方法为合成磺酰胺化多环喹啉并[2,1-b]喹唑啉酮衍生物提供了一种可靠高效的途径,采用N-氨基吡啶盐作为磺酰氨基自由基前体并在温和条件下进行反应。该转化反应具有广泛的底物适用范围、良好至优异的产率,并且无需使用强氧化剂和添加剂即可完成。
本研究成功开发了一种通过可见光诱导的氮自由基经过分子内环合反应实现磺胺化喹啉并[2,1-b]喹唑啉衍生物的合成新策略。该方法以未活化的芳乙炔基喹唑啉酮为原料,稳定易得的N-氨基吡啶鎓盐作为磺酰氨化试剂,4CzIPN为光催化剂,蓝光照射下,乙腈为溶剂,在温和条件(室温)下进行。
底物范围广泛:适用于多种N-芳磺酰氨基吡啶鎓盐(如苯环上带有吸电子和供电子等基团),甚至含有NH基团的氨基吡啶盐;适用于多种含有炔基的喹唑啉酮衍生物(如苯环上带有吸电子和供电子等基团),展现出良好的底物适用性。
反应机理验证:通过控制实验证实反应经由磺酰氨基自由基途径,通过分子内环化反应构建喹啉并喹唑啉酮四环骨架结构。
1. 反应设计与条件优化
首先,作者以3-(2-(苯乙炔基)苯基)喹唑啉-4(3H)-酮1a和N-对甲苯磺酰胺吡啶盐2a为底物的反应作为模板反应,对反应条件进行了优化。最终确定最优反应条件为:4CzIPN作光催化剂,CH₃CN作溶剂,室温,在氮气保护条件下,使用蓝光455 nm照射反应3小时,最终以76%的产率得到目标产物3a。
2. 底物适用范围研究
在确定最佳反应条件后,作者对反应的底物适用范围进行了探究。首先在标准条件下评估了多种含Ar和R³取代基的底物2的适用性。总体而言,苯环上不同位置带有供电子基团(甲基、乙基和叔丁基)或吸电子基团(氟、氯、溴和碘)的N-氨基吡啶鎓盐2均表现出良好的底物耐受性,以41%-89%的收率得到对应产物3a-3j。值得注意的是,苯环上带有强吸电子基团-CN的底物同样适用,以70%的收率获得目标产物3k。此外,含2-噻吩基团的底物也表现出良好耐受性,以64%的产率得到预期产物3l。含NH基团的N-氨基吡啶鎓盐也能成功应用于该反应,以良好收率得到对应产物3m和3n。苯环上带有两个或三个取代基的N-氨基吡啶鎓盐存在底物不相容性,未能获得目标产物3o和3p。这可能是底物中反应位点周围空间位阻的增加导致3o和3p的不能生成。此外,未能生成目标产物3q和3r,这可能是由于中间体反应活性降低所致。在尝试合成3o-3r过程中,以42-60%的收率获得了相同的副产物3s。
此后,作者对多种底物1进行了拓展,均表现出良好的反应耐受性,以62%-88%的产率成功制备出对应产物4a-4h。但含有噻吩-2-基乙炔基、环己基炔基或末端炔基取代基的喹唑啉酮类化合物与该串联胺化/环化反应不兼容,未能获得目标产物4r、4s和4t。其原因可能是其结构特性决定的,对关键的自由基加成和环化步骤产生不利影响。随后,在苯环上带有供电子基团或吸电子基团取代基的3-(2-(苯乙炔基)苯基)喹唑啉-4(3H)-酮类化合物1,在标准条件下进行反应,反应顺利进行,以良好至优异的收率(60-93%)得到相应产物4i-4q。此外,含氯和溴基的底物与该转化反应相容,得到产物4o和4p,这些产物具有进一步修饰衍生的潜力。遗憾的是,苯环上带有强吸电子-NO₂基团的底物未能得到目标产物,可能是由于所得缺电子中间体的反应活性降低所致。
同时,作者为验证所开发反应的实际应用性,使用2.5 mmol(0.805 g)3-(2-(苯乙炔基)苯基)喹唑啉-4(3H)-酮1a和N-氨基吡啶鎓盐2a进行了克级实验。当反应时间延长至21 h时,目标产物3a的分离产率为65%。此外,还进行了日光照射实验,该反应在自然光照下经过12 h反应后,产物3a的产率为49%。这些结果表明该反应具有潜在的实际应用价值。此外,化合物3a在98%硫酸和氢氧化钠分别作用下,可成功转化为 5-(甲基氨基)-6-苯基-12H-喹啉[2,1-b]喹唑啉-12-酮3a′,产率高达88%。该转化过程证明了所得产物的合成实用性,去除甲苯磺酰保护基可获得游离胺基团,该基团可作为多功能中间体。
3. 反应机理研究
为阐明环化反应机制,作者进行了多项控制实验。首先开展了一系列自由基捕获实验。在标准反应条件下,当引入2,2,6,6-四甲基-1-哌啶氧基(TEMPO)、2,6-二叔丁基-4-甲基苯酚(BHT)和1,1-二苯乙烯(DPE)等自由基捕获剂时,产物3a的生成受到显著抑制。此外,通过高分辨质谱(HR MS)成功检测到TEMPO-N(Me)Ts加合物5、BHT-N(Me)Ts加合物6及DPE-N(Me)Ts加合物7。这些结果表明环化反应通过涉及磺酰胺基自由基的途径进行。
基于上述实验结果和文献报道,作者提出了一种可能的反应路径。首先,在可见光照射下,光催化剂4CzIPN从基态被激发至激发态。随后,激发态PC*通过3-(2-(苯乙炔基(苯基)喹唑啉-4(3H)-酮1a淬灭,经单电子转移(SET)过程形成中间体I和PC自由基阴离子。PC自由基阴离子随即被N-氨基吡啶盐2a快速氧化,生成酰胺基自由基II和吡啶,同时再生成PC,通过另一个SET过程得以恢复。路径A:生成的自由基阳离子I通过共振作用转化为中间体III。随后,III通过分子内亲核加成/环化反应形成中间体IV。接着,中间体IV与酰胺基自由基II反应生成含氮中间体V。最终通过脱质子反应获得目标产物3a。路径B:中间体I与酰胺基自由基II反应生成中间体VI。中间体V通过III的分子内环化反应形成,目标产物3a则通过脱质子反应获得。
本研究发展了一种实用的可见光诱导合成磺酰胺化喹啉并[2,1-b]喹唑啉衍生物的策略,以未活化的芳乙炔基喹唑啉酮为原料,采用稳定易得的N-氨基吡啶鎓盐作为磺酰氨化试剂。从反应机理看,该转化过程由可见光诱导生成磺酰胺基自由基引发,随后通过分子内环化反应构建四环骨架结构。该方法具有底物适用范围广、产率优异、无需强氧化剂和添加剂、反应条件温和等优点。相关研究发表于J. Org. Chem.(DOI:10.1021/acs.joc.5c03167)。
鸣谢:本研究得到了河南省自然科学基金、河南工业大学博士科研启动基金的资助。
论文信息:
标题:Visible-Light-Driven Radical Amination/Cyclization of Arylethynyl Quinazolinones To Access Sulfonaminated Quinolino[2,1-b]quinazolines
作者:Qiyang Liu, Jinwei Yuan,* Jianning Zhang, Pan Zhao, Hewen Gao, Liangru Yang, Ji Ma,* Lingbo Qu*
通讯作者及单位:
袁金伟:河南工业大学,化学化工学院
马骥:中国烟草总公司郑州烟草研究院,烟草香料基础研究重点实验室
屈凌波:河南省科学院化学研究所
期刊:The Journal of Organic Chemistry
DOI:https://doi.org/10.1021/acs.joc.5c03167
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




