【J. Org. Chem.】云南民大:在水介质中通过光氧化还原催化自由基加成/环化可持续合成3-酰甲基化香豆素
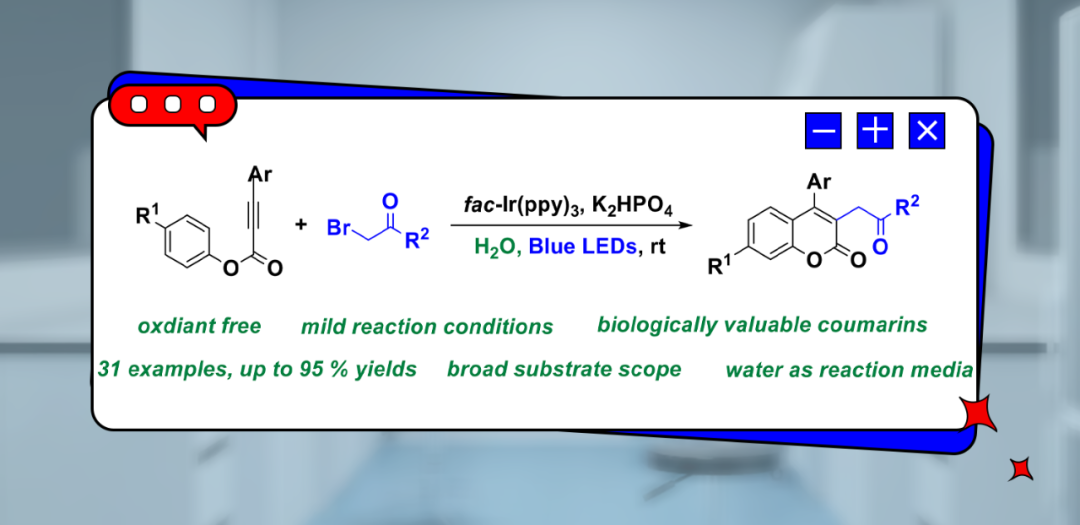
云南民族大学樊保敏教授和陈景超副教授团队开发了一种光氧化还原催化级联自由基反应,用于室温下芳基炔酸盐与α-溴酮在水中的加成/环化反应,为合成 3-酰甲基化香豆素提供了一种绿色高效的方法。这种方法无需使用传统的有机溶剂、相转移催化剂和过量的氧化剂,确保了操作的简便性和环境的可持续性。该反应具有良好的可扩展性,可用于多种底物,对官能团具有出色的耐受性,为获得具有生物价值的香豆素提供了一条多功能途径。相关研究成果发表在J. Org. Chem.上。
可见光因其丰富性、安全性和可再生性而成为一种重要资源,可实现多种光氧化还原转化。然而,传统的光催化方法主要依赖于有毒、易挥发的有机溶剂,易引发严重的环境和安全问题。在这种情况下,水为化学转化提供了一种可持续、环保且随时可用的介质。同时,水的独特物理化学特性不仅符合可持续化学的原则,还能提高反应效率。最近,König 及其合作者报告了一种新型的水相光催化过程,即在油水界面形成电子供体-受体(EDA)复合物,通过氢键加速转化(Science 2024, 383, 750−756)。然而,尽管取得了这些进展,可见光氧化还原催化在水介质中的应用仍处于早期阶段。因此,开发更高效的可见光介导的水中反应对于推进绿色化学至关重要,同时还能发掘水作为多功能反应介质的潜力。
香豆素及其衍生物是重要的天然产物、药物和生物活性分子。尤其是C3-官能化香豆素,如 3-(羰基)香豆素,已被确定为设计许多具有生物活性和药理意义的分子的关键骨架(Scheme 1a)。芳基炔酸盐的自由基加成级联环化反应(RACC)已成为构建 3-官能化香豆素的有效策略。多种自由基前体已被使用,包括Togni试剂、二苯基氧化膦、亚磺酸、2-氧代乙酸和二硒醚,从而形成了 3-官能化香豆素。具体实例见Scheme 1b(Org. Lett. 2016, 18, 3846−3849;J. Org. Chem. 2016, 81, 11489−11495;Org. Biomol. Chem. 2016, 14, 9033−9039)。尽管取得了这些进展,但许多方法仍然依赖于过量的化学氧化剂,如TBHP、TBPB和DLP,以及高温处理。这不仅会引发环境问题,还限制了反应的整体效率。因此,开发环境友好、温和条件下不使用氧化剂的方法仍然是一项重大挑战,也是推进3-官能化香豆素合成的关键。
另一方面,α-卤酮,尤其是 α-溴酮,由于能够在 C-Br 键断裂时形成烷基自由基,因此已成为合成杂环和生物活性分子的易得反应物。在此,樊保敏教授和陈景超副教授团队报告了芳基炔酸盐与 α-溴酮在水中进行自由基加成/环化的光氧化还原催化级联反应,以制备 3-酰甲基化香豆素(Scheme 1c)。该方法无需氧化剂或高温,可在水中制备 3-酰基甲基化香豆素,具有底物范围广、可扩展性强和效率高等特点。
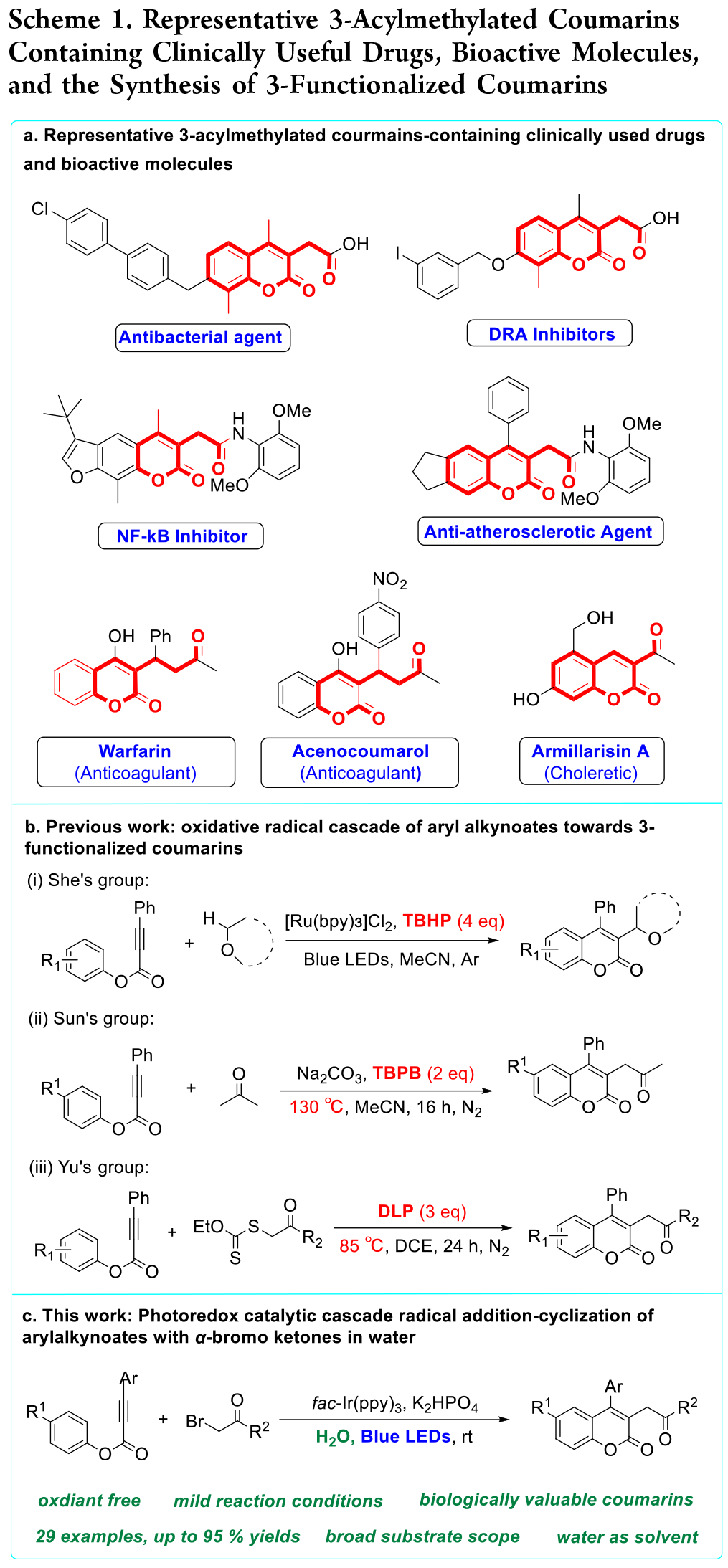
(Scheme 1,图片来源:J. Org. Chem.)
在最初的优化实验中,作者选择了3-苯基丙酸苯酯 1a 和2-溴苯乙酮 2a 作为代表性底物(Table 1)。使用 4CzIPN (3 mol %) 作为光催化剂,Na₂CO₃(2.0 equiv) 作为碱,在CH₃CN/H₂O (9:1) 混合溶剂中,室温下蓝光照射,生成了 3-酰基甲基化香豆素 3aa,产率为37%(entry 1)。随后对一系列光催化剂进行了评估,以提高产率(entries 2−8)。Ru(bpy)₃Cl₂将产率提高到55%(entry2),而fac-Ir(ppy)₃进一步将产率提高到66%(entry 3)。接着,测试了各种碱替代Na₂CO₃的能力(entries 9-11)。当使用温和的碱 NaHCO₃时,产率提高到77%(entry 9);当使用K₂HPO₄作为碱时,产率提高到 92%(entry 11)。此外,研究了反应介质的影响,当反应完全在水中进行时,产率进一步提高到95%(entry 13)。对照实验表明,没有光催化剂或光照时,反应无法进行,且在没有K₂HPO₄(entries 14−16)的情况下,产率仅为22%。

(Table 1,图片来源:J. Org. Chem.)
作者进一步研究了芳基炔酸盐(1)与2-溴苯乙酮(2a)在优化条件下的作用范围(Scheme 2)。苯环上的对甲基取代(3ba)和对叔丁基取代(3ca)产生了很好的收率,分别高达77% 和 90%。与此相反,在对位上的卤素取代基导致中等产量(3da-fa)。然而,对位的吸电子甲基酯取代(3ga)导致了低产率(42%)。使用其他吸电子取代基(3ha-ja)时,仅获得微量产物。接下来,作者研究了取代基对乙炔基团的影响,3ka-3qa的产率在50%-97%之间。不过,1a 的酰胺衍生物在本转化过程中没有反应,无法生成3ra,这可能是由于其反应活性较低。
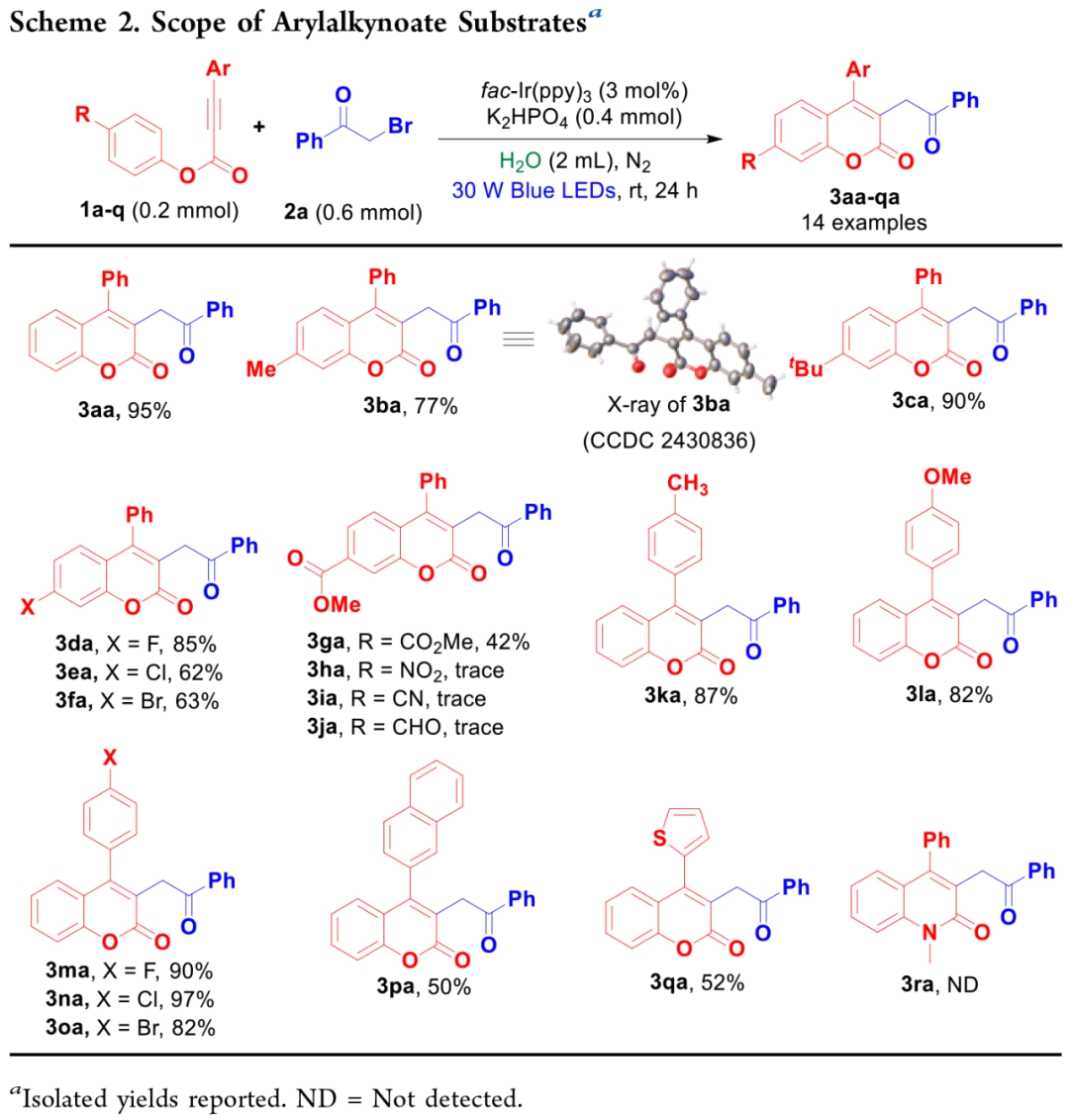
(Scheme 2,图片来源:J. Org. Chem.)
随后,在优化的条件下用1a 探索了α-溴酮 (2a-q) 的范围,以中等到优异的收率得到了目标香豆素(3ab-aq)(Scheme 3)。用 2-chloro-1-phenylethan-1-one 代替 2a,可以得到收率为80% 的 3aa,这表明α-酮氯化物也是可行的底物。研究发现,在对位(3ab-ad)、间位(3ae-ag)和邻位(3ah-aj)上带有吸电子基团的2-溴苯乙酮能顺利发生反应。将苯环替换为杂环结构,得到3ak,产率为51%。苯环的对位和间位带有甲基取代基的 2-溴苯乙酮也是合适的反应物(3al-am)。此外,α-溴酮也表现出良好的兼容性(3an-ar),这突显了该方法的稳健性和多功能性。然而,未活化的烷基溴化物未能生成预期的产物(3as-au)。
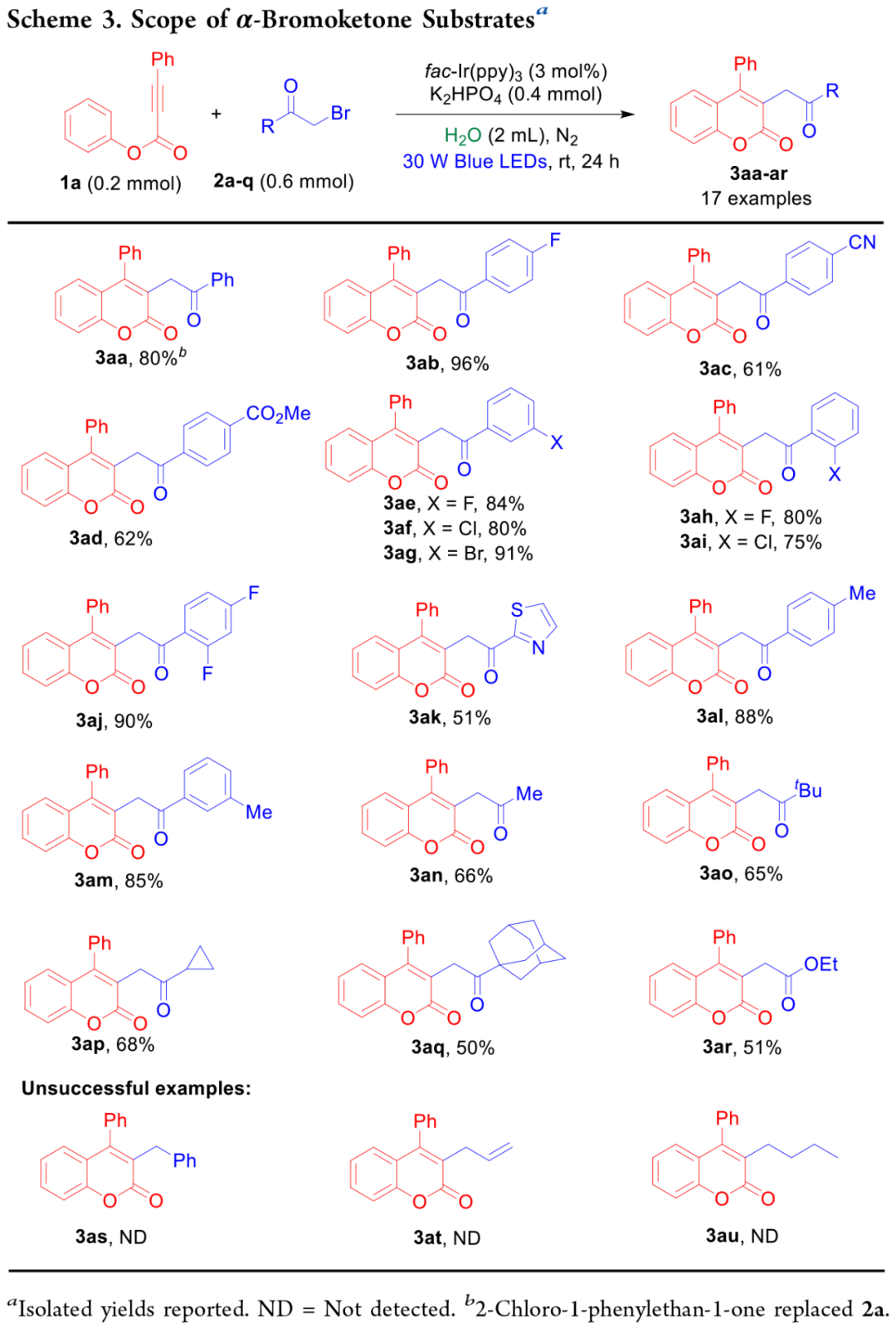
(Scheme 3,图片来源:J. Org. Chem.)
为了验证其可扩展性,在优化条件下进行了克级反应,从1a(1 g)得到了 3aa(1.15g,产率 75%)(Scheme 4a)。为了研究光氧化还原催化环化的机理,作者使用二丁基羟基甲苯(BHT,3.0 equiv)作为自由基淬灭剂,在既定的反应参数下进行了自由基捕获实验(Scheme 4b)。该实验完全抑制了3aa的形成,并以60%的产率产生加合物4,从而证实了α-羰基自由基中间体参与了机理途径。荧光淬灭实验表明,4CzIPN 在 540 nm(803 au)处发出强烈的发射光,加入 1a 后发射光仍保持不变。然而,观察到2a 对激发态fac-Ir(III)(PY)₃*物种的线性、浓度依赖性淬灭(Scheme 4c)。这一现象证实了激发态催化剂和 2a 之间的光诱导电子转移,从而启动了催化循环。光-暗间隔研究表明,3aa 仅在蓝光照射下形成(Scheme 4d)。根据机理研究和先前的文献,该反应过程的催化循环如Scheme 5所示。
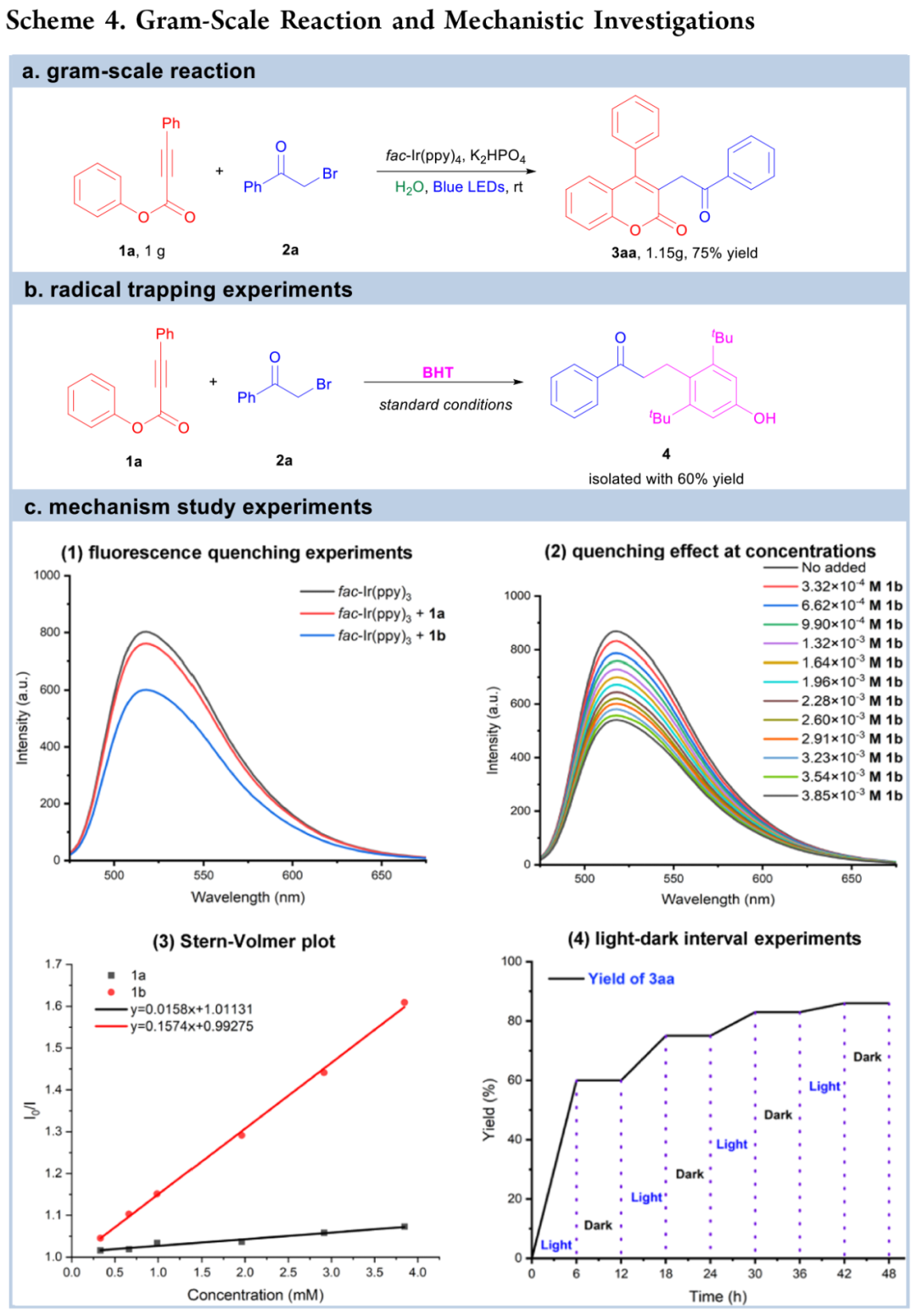
(Scheme 4,图片来源:J. Org. Chem.)
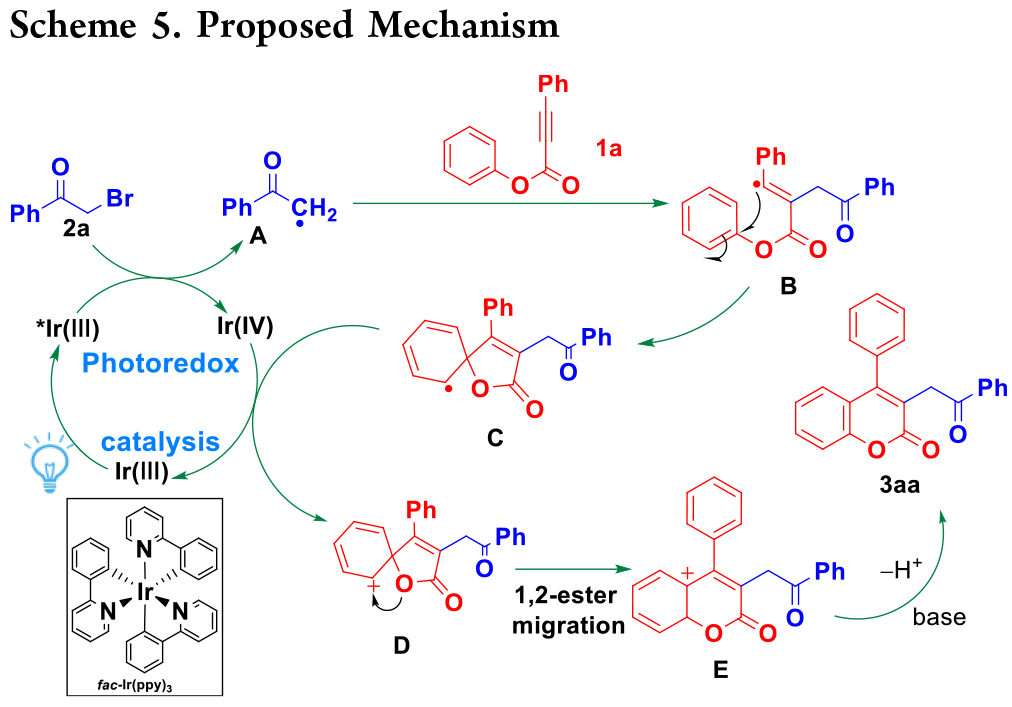
(Scheme 5,图片来源:J. Org. Chem.)
总之,樊保敏教授和陈景超副教授团队成功地开发了一种高效的合成方法,在水相中通过可见光诱导芳基炔酸盐与α-溴酮的级联酰甲基化和环化反应制备 3-酰甲基化香豆素。该反应采用易于获取的底物,避免使用有机溶剂和氧化剂,可在常温条件下进行,与各种官能团兼容,具有显著的效率和出色的可扩展性,因而具有广泛的适用性。根据控制实验的结果,提出了一个可信的反应机理。该方法首次描述了在非氧化条件下在水中合成 3-酰基甲基化香豆素的实例,既提供了具有生物价值的 3-烷基香豆素,又在水体系光催化反应的开发方面取得了重大进展。
论文信息:
Binfeng Zhu, Devendar Ponnam, Mingzhu Li, Guokai Li, Ruifeng Fan, Jingchao Chen*, Baomin Fan*. Sustainable Synthesis of 3-Acylmethylated Coumarins via Photoredox Catalytic Radical Addition/Cyclization in Aqueous Media. J. Org. Chem., 2025
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




