【Science】加州大学伯克利Sarpong组重磅:光激发二氢苯并呋喃骨架重排实现1,2-酰基转移
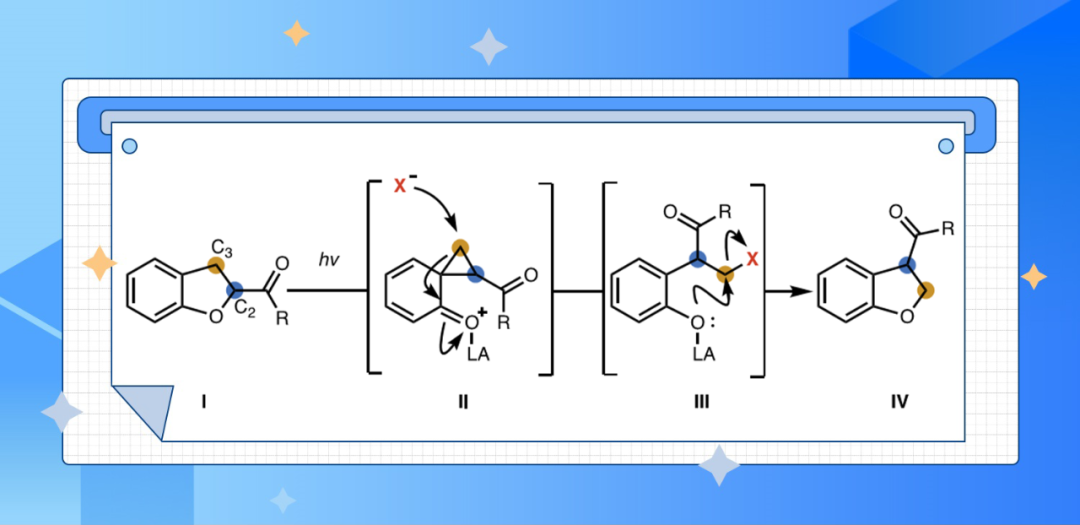
最近,加州大学伯克利分校(UCB)Richmond Sarpong课题组,报道了一种2,3-二氢苯并呋喃的形式1,2-酰基转移(transposition)光化学方法。其中,(杂)芳基酮底物在370 nm光激发下实现酰基转移,羧酸、酯、酰胺类底物在310 nm光激发下实现酰基转移。该方法通过光激发2,3-二氢苯并呋喃生成双自由基,经自由基重组得到高度亲电的螺-环丙烷中间体,然后被卤素亲核试剂捕获,开环生成卤化物中间体,最后关环,从而将酰基官能团从C2位转移至C3位。相关研究成果发表在近期的Science上。
官能团转移重要性:杂环的后期外围官能团化和官能团转移,已成为构效关系(SAR)研究中必不可少的研究项目,可以识别和优化生物活性化合物。然而,后期官能团转移相关研究仍然比较少。Fig. 1A中对比了后期官能团转移(transposition)和原子转移在概念上的可视化区别。Fig. 1C中则举例说明1,2-官能团转移,在提高药物分子药效和选择性方面的巨大潜力。
已报道相关研究:如Fig. 1B所示,涉及C-C键裂解的光激发1,3-酰基转移,相关研究比较深入。相比之下,1,2-酰基转移比较难实现,已报道案例比较少,且缺乏通用方法。如Fig. 1E-G所示,Hansen, H. Schmid等人、Y. Kanaoka和K. San-nohe、A. G. Schultz等人,都报道过经螺-环丙烷策略实现光激发1.2-官能团转移,但仅有个别案例。
此研究工作简介:本文Richmond Sarpong组报道的方法,也是基于螺-环丙烷策略,实现2,3-二氢苯并呋喃的光激发形式1,2-官能团转移。如Fig. 1D所示,2,3-二氢苯并呋喃在光激发下生成螺-环丙烷中间体II,然后发生环丙烷选择性开环生成中间体III,III的卤原子被酚羟基取代,从而实现酰基在C2位至C3位的转移。
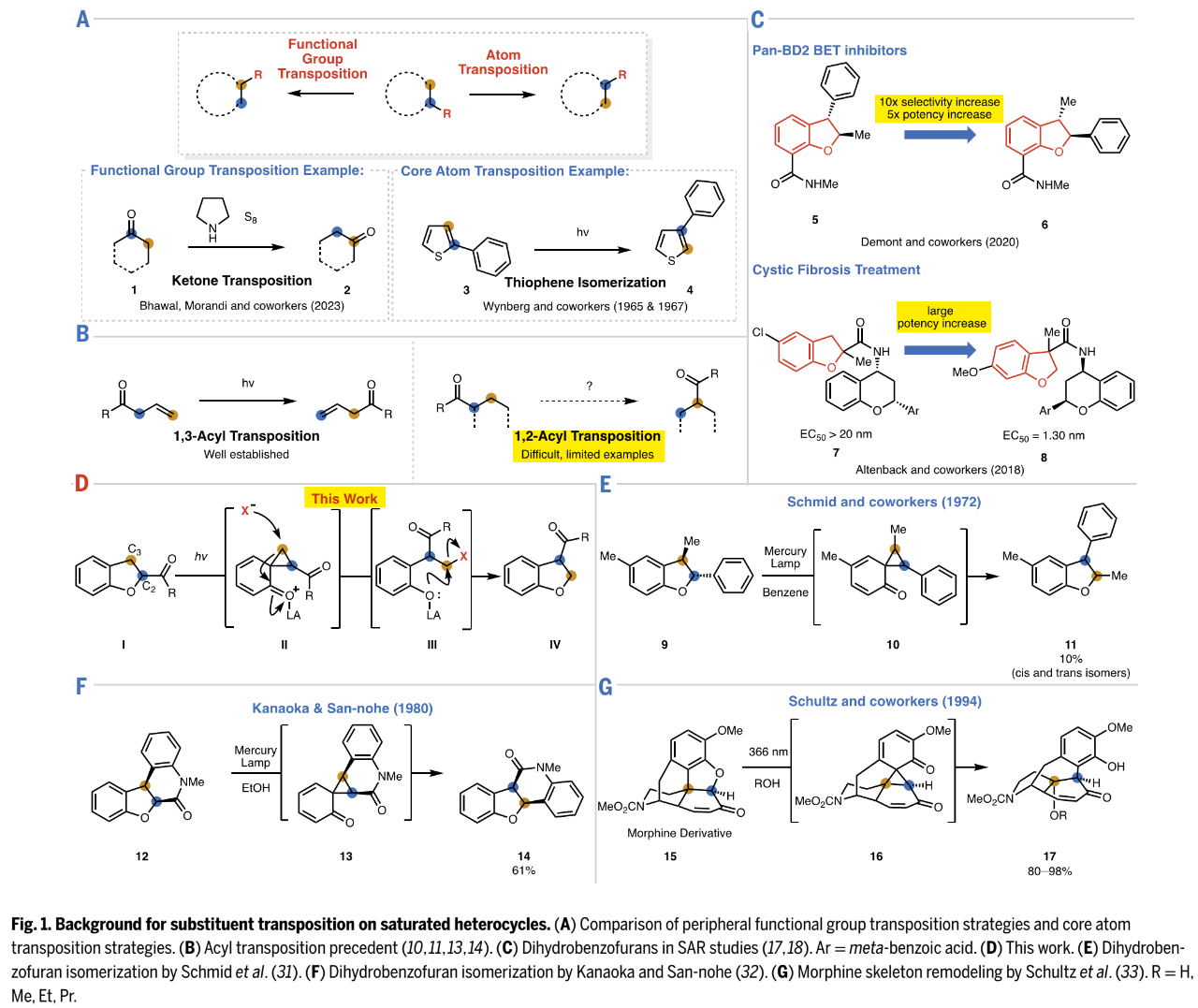
(Fig. 1,图片来源:Science)
条件筛选:作者首先以18a或18b为模板底物开展条件筛选研究。如Fig. 2B所示,在370 nm光照下,1)氮气鼓泡除氧的异丙醇/水作溶剂,以盐酸水溶液作卤源不加碱,18a的反应只得到氯化物中间体20(entry 2)。光照后再加三乙胺处理,能得到理想产物21(51%)和副产物22(entry 3)。其它质子酸类卤源和碱的搭配组合,效果都较差;2)以除氧后的丙酮/水作溶剂下,以碘化锂作卤源,18b能以64%收率得到21(entry 8)。据此得出两种优选反应条件,8小时光照再加入三乙胺的两步一锅法,底物可以反应完,和24小时光照的一步反应,但底物反应不完,不过都需要控制光激发时间,因为实验发现光照时间长会降低产率,可能是产物发生了降解。Fig. 2C的控制实验表明,光照、极性质子溶剂、溶剂除氧对反应是必须的,否则会导致反应不发生或产物降解。Fig. 2D的同位素标记实验,证明反应发生了骨架重排,酰基从C2位转移至C3位。
异构化机理:基于Fig. 2B-2D的实验,作者提出如Fig. 2A所示简单机理:18在光激发下所生成螺-环丙烷中间体19,在质子酸作用下会经路径1发生转化,环丙烷开环生成20,20在碱作用下可以关环生成理想产物21,也可以发生单分子共轭碱消除(E1cB)得到副产物22;在路易斯酸作用下则经路径2发生转化,经中间体23关环得到理想产物21。
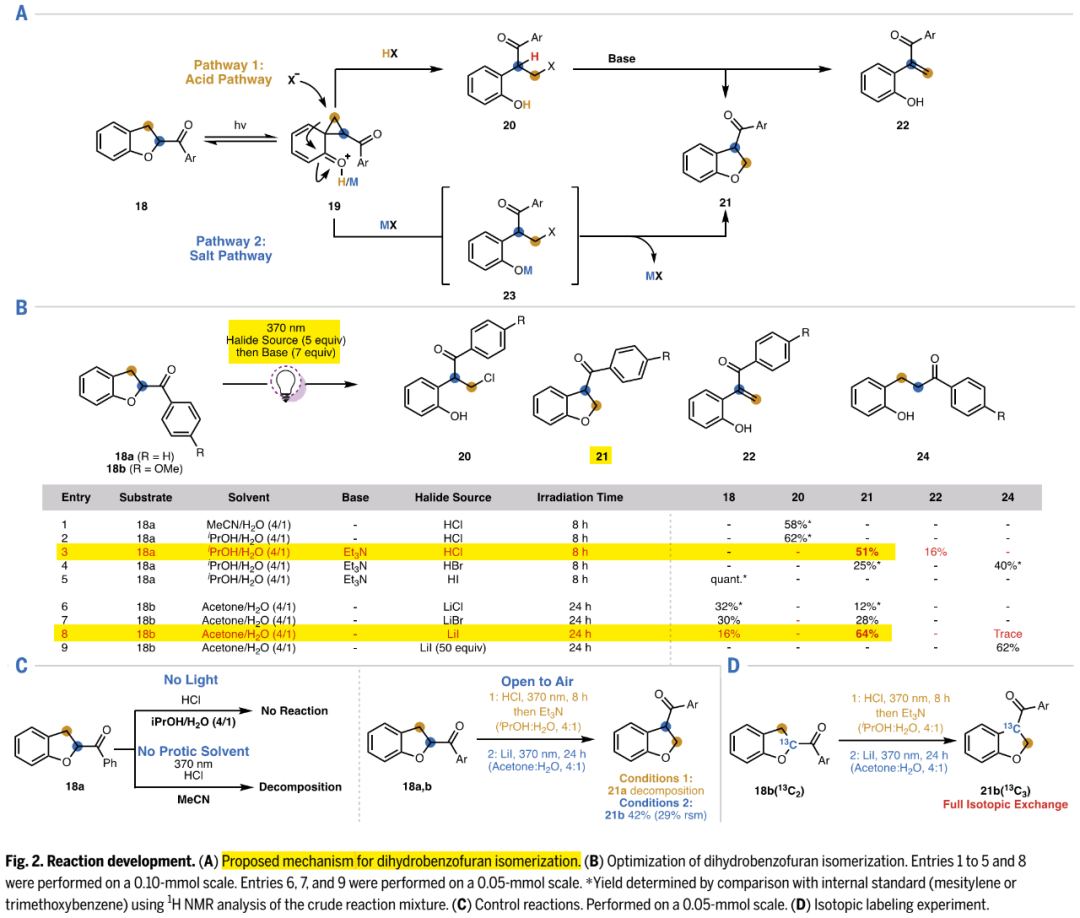
(Fig. 2,图片来源:Science)
酮底物拓展:如Fig. 3所示,在两种优选条件下,带各种酰基官能团、和苯环上带各种基团的2,3-二氢呋喃18,大部分都可以实现酰基转移,得到理想产物21。虽然多数产物只有中等或比较低的收率,但鉴于只需1步反应,无需为了得到C3位酰基产物而从头合成,还是很具性价比的。例如18ak能以大于50%收率转化成21ak,若采取从头合成策略,各方面成本应该会高的多。C3位带甲基的2,3-二氢呋喃25,也能发生反应得到理想产物26,这个很惊喜。C2位带甲基的2,3-二氢呋喃29,则未得到理想产物。
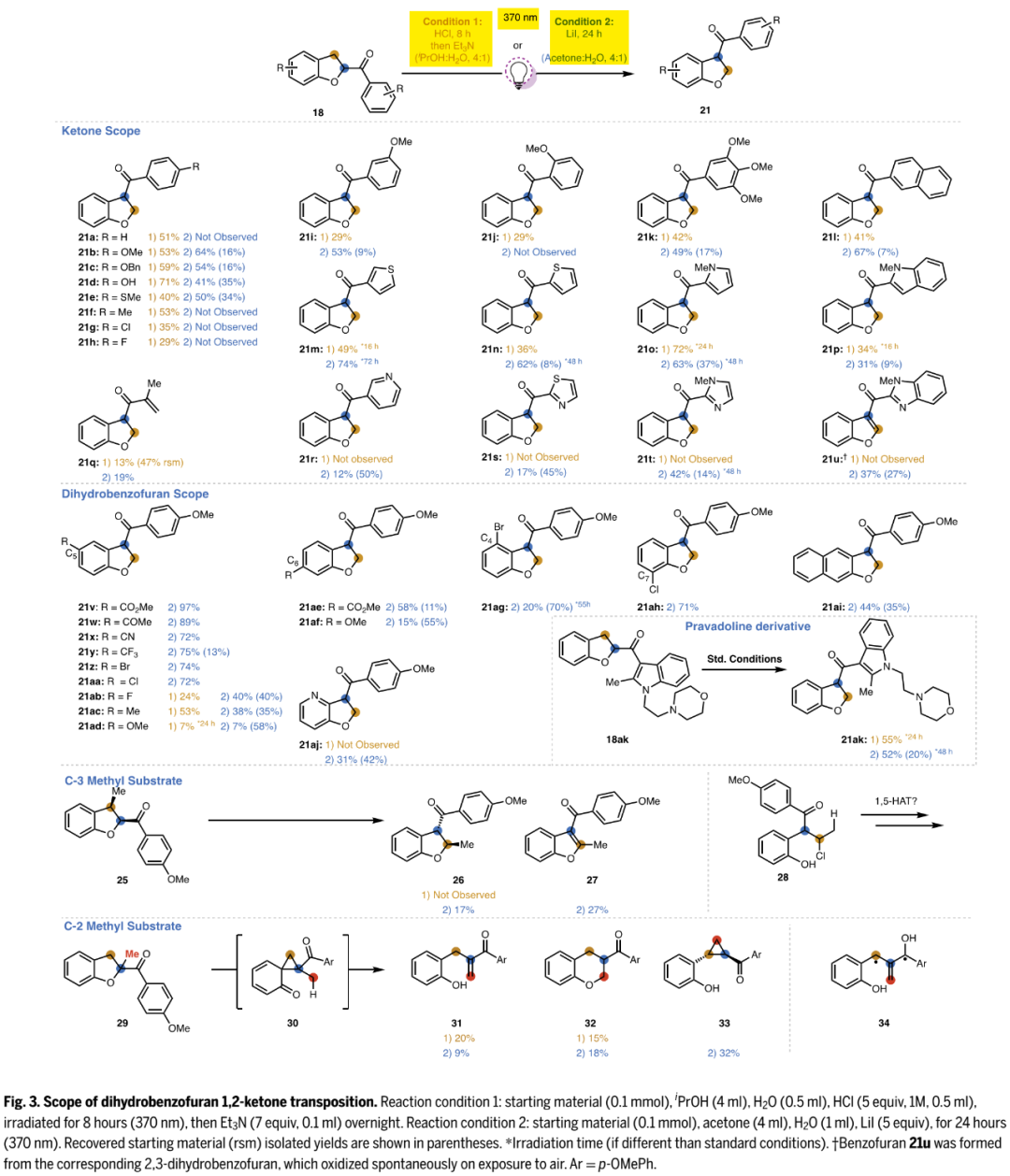
(Fig. 3,图片来源:Science)
羧酸酯转移条件:如Fig. 4A所示,在310 nm光激发下,以盐酸作卤源,也能实现羧酸酯底物35a的酰基转移,以82%收率得到理想产物37a,碘化锂作卤源则不行。310 nm光照更有效原因,1)如Fig. 4B所示,底物和中间体36a吸收波长在300 nm下,且光化学反应通常在比底物更长波长光照下更有效;2)溶剂丙酮对300-330 nm光有微弱吸收峰。
羧酸酯/羧酸/酰胺底物拓展:如Fig. 4C所示,多种羧酸酯、羧酸、酰胺类底物35,在310 nm光照条件下,也能发生酰基转移,得到理想产物37。其中,生物活性分子35h和35i的成功反应,进一步验证了反应的应用价值。比较遗憾的是,甲基酮38、炔基酮39参与的反应,会发生降解(Fig. 4D)。甲基、烯基、苯基、氰基类底物40-43,不会发生理想反应,证明羰基在此反应中起着重要作用。
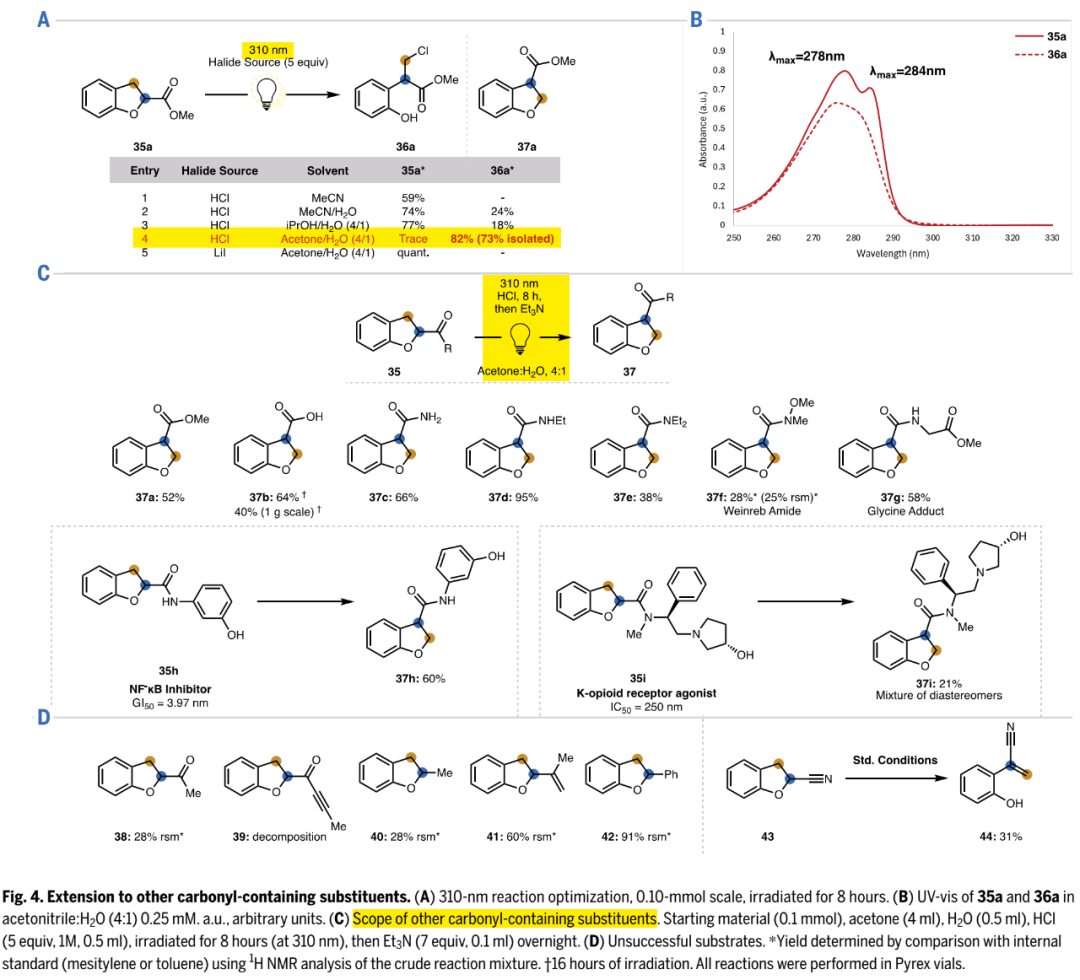
(Fig. 4,图片来源:Science)
机理研究:对于关键的螺-环丙烷中间体生成,作者提出如Fig. 5A所示三种假设途径:1)[1,3]-σ重排的协同路径I,具有立体保持性;2)C-O键均裂/双自由基重组的自由基路径II,可能导致外消旋化;3)单电子转移/自旋中心移位开环/双自由基重组的自由基路径III,也可能导致外消旋化。作者通过机理验证实验,得出经双自由基重组的路径II或III更具可行性。
相关机理验证实验和结论:1)Fig. 5B、5C的实验,证明底物外消旋化是受光激发影响,而不是添加剂酸影响。氘水作溶剂实验未发现原料和产物中含氘,证明反应中发生的外消旋化,不是通过生成光-烯醇化物发生;2)SI中底物18和氯代中间体20的时间-反应进程研究(详见Fig. S11和S13),发现反应中中间体20比剩余底物18的e.e.低,且20的外消旋化实验(详见Fig. S21和S22)发现20在光反应条件下不会发生外消旋化,这表明反应可能经双自由基VI发生外消旋化;3)SI中自由基捕获实验未发现TEMPO加合物,只是发现产物收率中度降低,进一步证实双自由基存在。
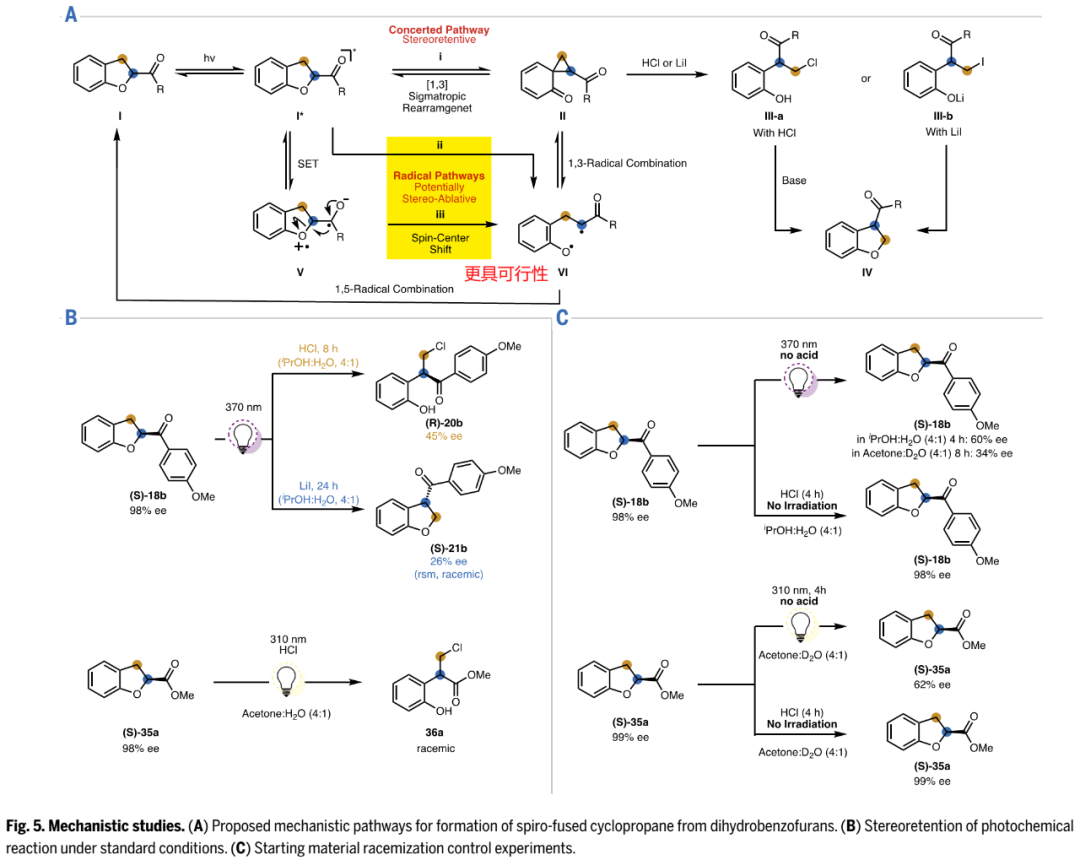
(Fig. 5,图片来源:Science)
Richmond Sarpong课题组发展出一种独特的光激发骨架重排策略,可以实现2,3-二氢苯并呋喃C3位酰基至C2位的高效转移。该研究工作表明,骨架重排策略在实现外围官能团修饰方面具有重大应用潜力。
论文信息
1,2-Acyl transposition through photochemical skeletal rearrangement of 2,3-dihydrobenzofurans
Ryan T. Steele†, Motohiro Fujiu†‡, Richmond Sarpong*
Science, 2025
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




