利用光催化卤原子转移和基团转移化学实现去官能团化过程
CNRS/图卢兹第三大学(CNRS/Université Toulouse III-Paul Sabatier)Sami Lakhdar课题组与亚琛工业大学(RWTH Aachen University)Daniele Leonori课题组发展了基于卤原子转移和基团转移化学,在温和条件下实现了烷基和芳基卤化物以及醇和硫醇衍生物的活化-去官能团化过程。实验和计算研究揭示了一个非典型的反应路径,即环己二烯基自由基经历了芳构化-卤原子(基团)转移过程。相关成果发表在Science上。
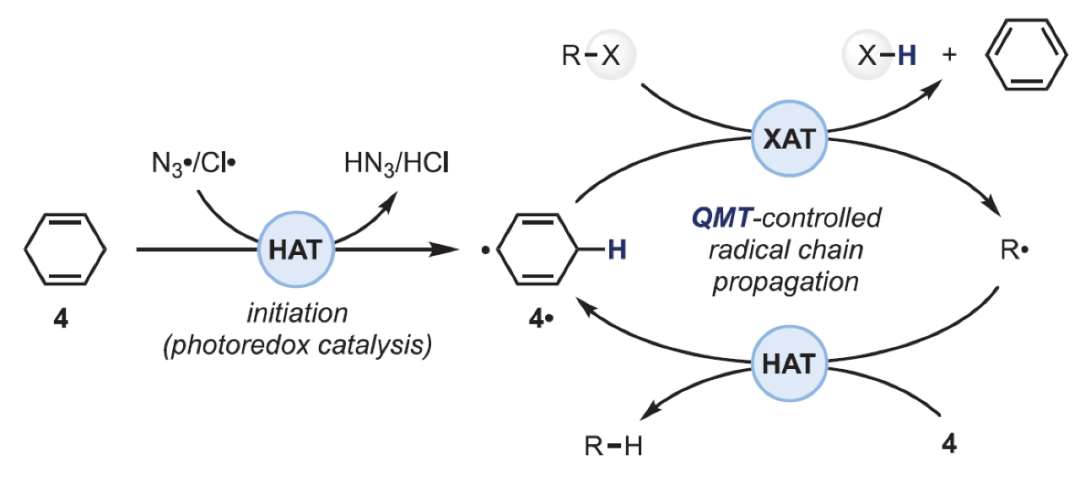
碳自由基是合成许多有机化合物的重要活性中间体。而在其众多合成方法中,使用商业可得或简单易得的卤化物和醇或硫醇衍生物,基于卤原子转移和基团转移化学策略实现其生成具有较大的优势。
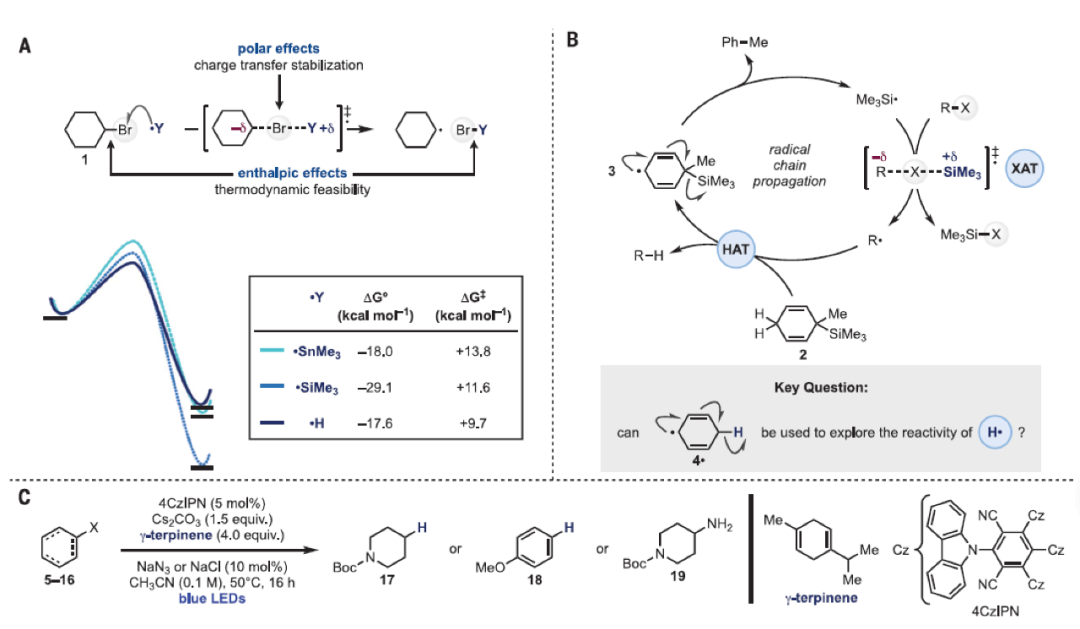
卤原子转移过程通常会遵循一下三个原则(Fig. 1A):1)其依赖于参与该过程的三个原子(C、X和Y)之间的共线排列,以实现自由基物种Y•的SOMO轨道和C-X反键轨道(σ*)之间的最大轨道重叠。2)Y-X键需要比反应物中的C-X键更强,这样整个过程才能是热力学上有利的。3)快速的动力学过程是由过渡态极性效应的相互作用引起的,从而通过电荷转移降低了反应能垒。鉴于C-X键固有的极化性,亲核性的自由基则非常适合稳定出现的正离子,从而加速原子攫取过程。比如锡自由基和硅自由基等,由于其可以最大限度地提高焓效应和极性效应,因此仍被常规用于自由基的生成过程中。但是此类试剂存在毒性高、成本高和废物处理等问题,因此发展碳自由基生成的替代策略至关重要。最近,CNRS/图卢兹第三大学Sami Lakhdar课题组与亚琛工业大学Daniele Leonori课题组发展了基于卤原子转移和基团转移化学,在光催化下实现了烷基和芳基卤化物以及醇和硫醇衍生物的活化-去官能团化过程。作者推测氢原子(H•)可以作为合适的试剂来实现此类反应。由于氢原子可以展现质子类特征从而使过渡态发生极化,因此有助于电荷转移过程的稳定性。作者通过对CyBr 1与Me3Sn•, Me3Si•和H•的卤原子转移反应过程的计算,结果表明所有三种攫取过程均是高放热的,但由H•介导的攫取过程有着最小的动力学阻碍(Fig. 1A)。尽管以上实验结果将支持H•介导的攫卤模式,但由于在合成中缺少形成H•的方法而在实施过程中受到了一定的阻碍。为了实现这一挑战,作者注意到前芳香性这一概念,其广泛应用于硅自由基的形成过程中(Fig. 1B)。基于利用环己二烯自由基物种3•产生硅自由基的反应过程,作者希望利用简单的环己二烯自由基4•来实现H•的形成。
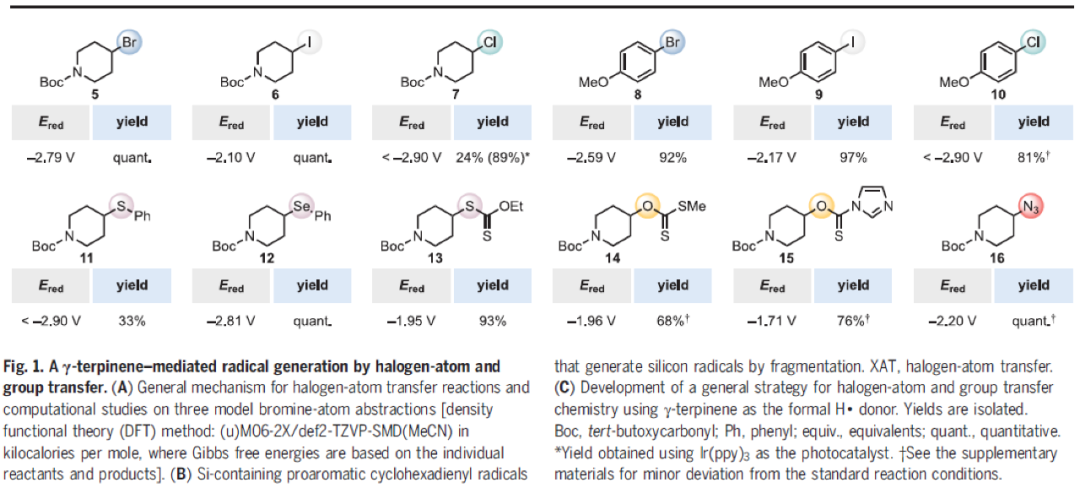
作者选用从互生叶白千层的精油中提取的环己二烯衍生物γ-terpinene 5作为原料,利用有机染料4CzIPN(5 mol%)作为光催化剂,NaCl或NaN3(10 mol%)作为添加剂,蓝光照射下在乙腈中反应,可以以当量的产率得到脱溴产物17。此外,对于其它前芳香性试剂,如简单的1,4-环己二烯也可以实现类似的转化,从而与作者最初的机理假设相一致。接下来,作者对此转化的底物范围进行了探索(Fig. 1C)。相应的C-4碘化物6和氯化物7均可以实现脱卤过程。此外,富电子芳基卤化物(8-10)也具有良好的兼容性,分别以良好的产率得到产物18。值得注意的是,此策略并不仅仅局限于有机卤化物的活化,当作者使用C-4硫化物11、C-4硒化物12、C-4黄原酸酯13、C-4醇衍生物14和15均可以以中等到良好的产率得到产物17。烷基叠氮化物16在此体系下可以实现相应的一级胺产物19,这相当于在无过渡金属存在的条件下实现了叠氮化物的氢化过程。
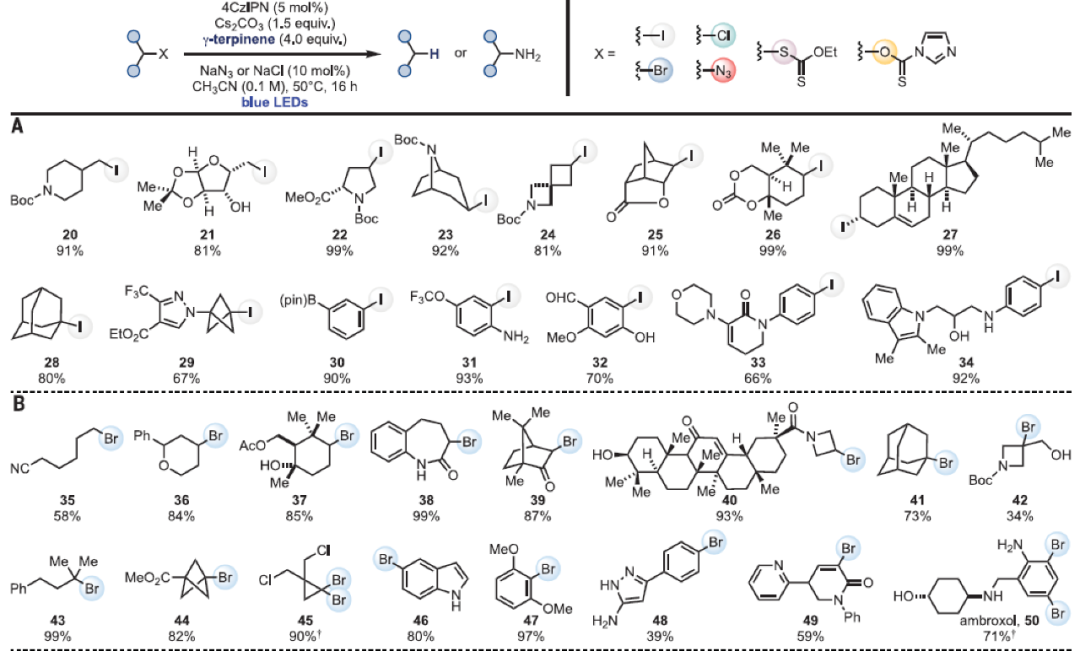
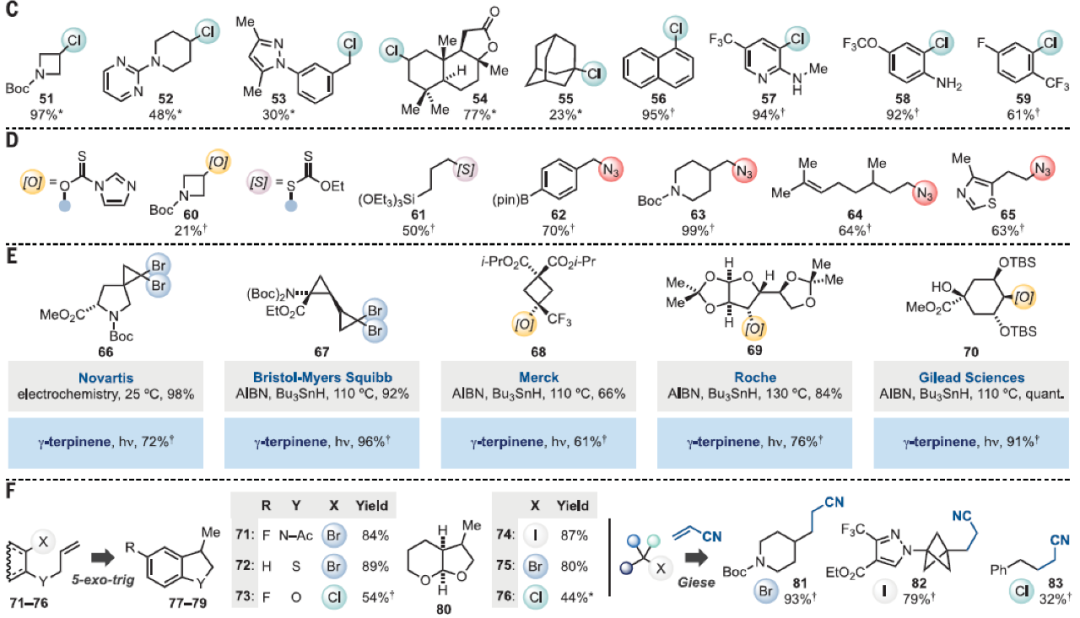
上述实验结果表明此温和的反应策略可以避免锡或硅自由基活化过程中需要使用强还原剂等不足,因此可能具有更宽的底物适用性。一系列官能团化的烷基或芳基卤化物20-59均可实现此转化,以相对高的产率得到相应的还原产物(Fig. 2, A-C)。多样的官能团,如保护或非保护的醇和胺、缩醛、酯、内酯、内酰胺、醛、酮以及苄基碳、烯丙基碳和杂原子α-碳等结构单元均可兼容。值得注意的是,当使用光化学流动反应器时可实现大规模制备而产率基本不受影响。在芳基卤化物兼容性探索过程中,作者发现含有强给电子基的底物同样具有较好的兼容性,而此类底物通常在基于单电子转移(SET)策略中具有较大的挑战性。除了卤化物外,醇或硫醇衍生物(60,61)和许多烷基叠氮(62-65)也可实现此类转化,分别得到相应的还原产物和胺化产物(Fig. 2D)。接着,作者尝试将此方法应用在药物分子的去官能团化反应中,从而在避免使用有毒的锡或硅试剂下,即可在温和条件下实现具有较高价值生物活性分子的制备(Fig. 2E)。最后,为了进一步证明此方法的普适性,作者还探索了烷基或芳基卤化物的其它反应模式,如还原5-exo-trig环化(71-73→77-79,74-76→80)和Giese加成(81-83),均取得了成功(Fig. 2F)。
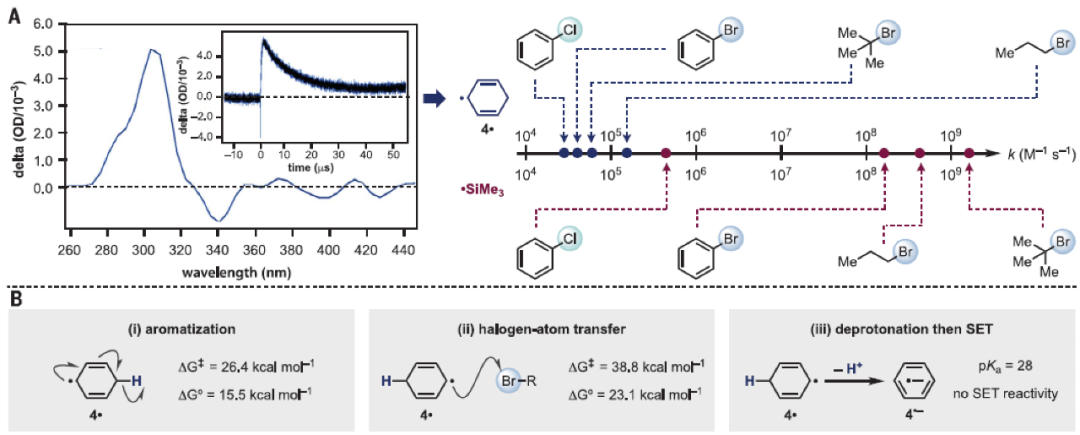
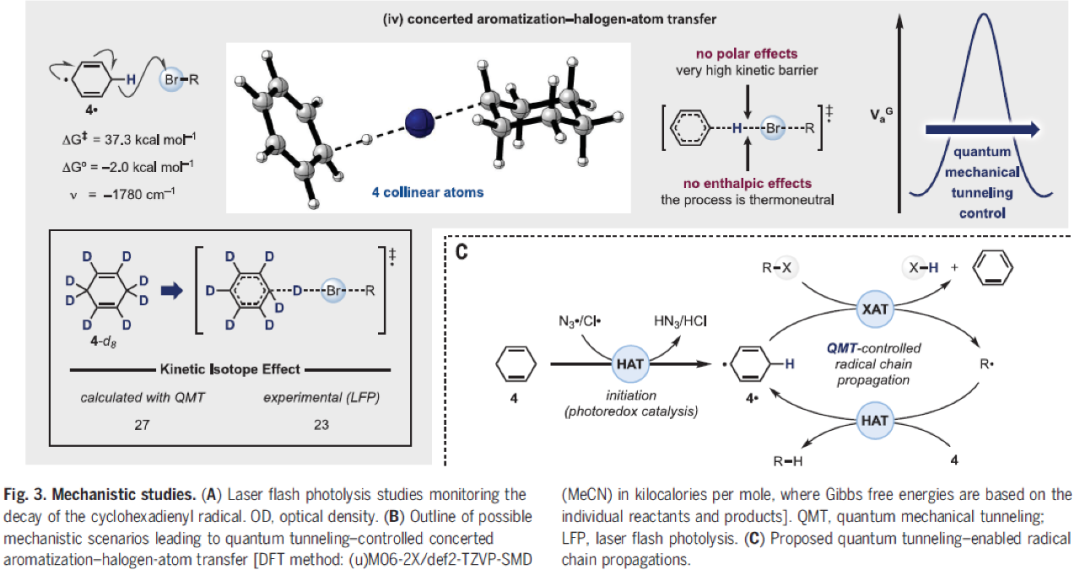
接下来,作者对此过程的反应机理进行探索。首先,作者通过控制实验证实γ-terpinene和光照对此反应至关重要。随后,作者在(t-BuO)2和卤化物存在的情况下,在hν = 355 nm(其中普朗克常数和ν是光子频率)下照射环己二烯,通过激光光解测试来监测环己二烯自由基4•(λmax = 315 nm,其中λmax是最大吸收波长)的生成和反应性。值得注意的是,所有实验结果得出4•的衰变具有相似的双分子速率常数(k2),且均在105 M-1 s-1附近。这一动力学结果与在类似淬灭剂存在条件下测量到的硅自由基的衰变速率的巨大差异形成鲜明对比。硅自由基的衰变通常更快,并取决于碳-卤素键的键解离能(BDE),因此跨越了三个数量级(Fig. 3A)。作者最初将这一非典型结果归因于芳构化过程,随之而来的是H•快速地攫取卤原子。然而,计算结果表明生成H•需要 > 15 Kcal mol-1的能量,具有很高的动力学障碍,这与作者在合成实验中观察到的快速反应性并不一致(Fig. 3B, part i)。以上实验结果表明,此反应应该会有一个不同的反应途径。接下来,作者排除了从4•开始发生的溴原子转移或基团转移过程,因为该过程为较强的吸热过程(ΔG°= 23.1 Kcal mol-1)且在动力学上是不利的(ΔG‡= 38.8 Kcal mol-1,其中ΔG‡为吉布斯活化能)(Fig. 3B, part ii)。此外,计算表明4•中亚甲基质子的pKa = 28,从而通过4•的脱质子过程得到相应的苯基负离子4•-,随后实现底物的SET活化过程也可以被排除了(Fig. 3B, part iii)。作者还尝试将γ-terpinene的反应性转化到易于还原但不能进行原子或基团转移的底物上,结果发现其并没有反应性,因此排除了反应中包含SET过程。结合上述实验结果,作者对最初的机理假设进行了重新审视,认为此反应可能是芳构化和H•介导的攫卤过程相互关联并同时发生的混合机理(Fig. 3B, part iv)。作者认为,首先添加剂NaCl或NaN3发生单电子氧化得到相应的Cl• 或N3•。随后其与环己二烯(或γ-terpinene)在光催化下发生快速的攫氢过程得到环己二烯基自由基4• 。接下来,4•与卤化物发生芳构化-卤原子转移过程得到相应的烷基和芳基自由基,随后这些自由基物种可以通过与4发生HAT重新启动实现4•的生成从而实现循环(Fig. 3C)。
CNRS/图卢兹第三大学(CNRS/Université Toulouse III-Paul Sabatier)Sami Lakhdar课题组与亚琛工业大学(RWTH Aachen University)Daniele Leonori课题组发展了基于卤原子转移和基团转移化学,在光催化下实现了一系列烷基和芳基卤化物以及醇和硫醇衍生物的活化-去官能团化过程。反应条件温和,底物和官能团兼容性好并可以实现大规模制备,具有良好的实用性。实验和计算研究揭示了一个非典型的反应路径,即环己二烯基自由基经历了芳构化-卤原子(基团)转移过程。




