引入光催化活性非天然氨基酸的人工光酶催化
激发三重态
电子的自旋量子数为+1/2(自旋向上)或-1/2(自旋向下)。根据Pauli exclusion principle,在占据同一个轨道时,电子是以一个自旋向上和自旋向下的方式。
s为体系的电子自旋量子数,M为电子的多重度,等于2s+1。
如果体系所有电子都是配对的,那么体系总的自旋量子数为0,多重度(2s+1)为1,此时分子状态为单重态,用S表示。一般的有机分子,基态时为单重态,用S0表示。
当受到激发后,一个电子从低能量的轨道跃迁到高能量的轨道,如果此电子的自旋没有发生变化,那么分子的自旋量子数仍然为0,多重度(2s+1)仍然为1。这时分子形成单重激发态,用S1表示。
S1态有一定概率发生电子自旋翻转(称为系间窜跃),那么分子的自旋量子数为1,多重度(2s+1)为3。此时的分子形成三重激发态,用T1表示。三重激发态的寿命较单重激发态更长。
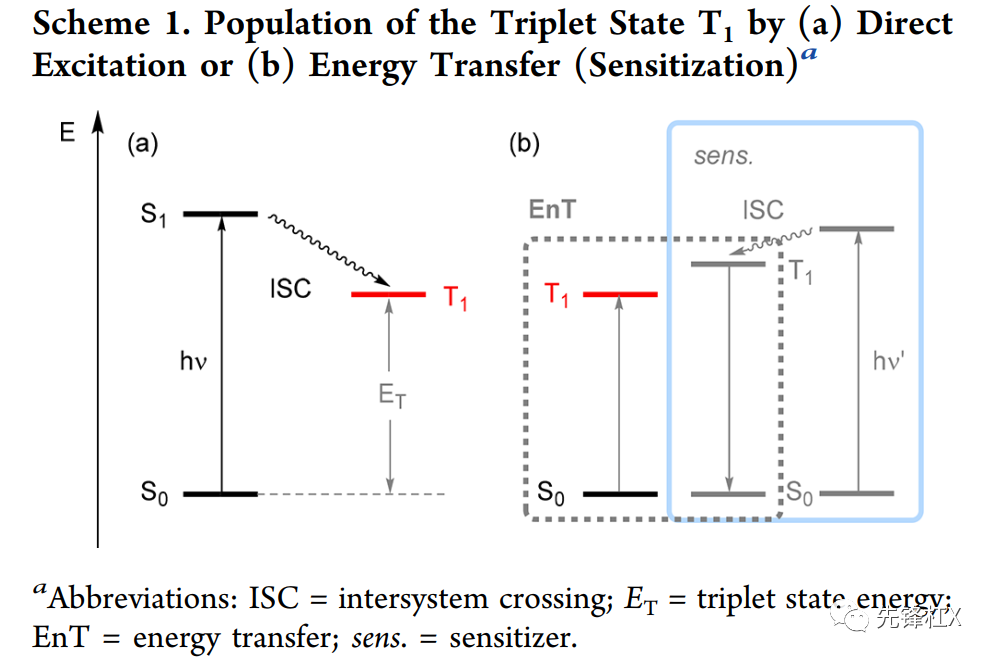
三重态能量转移(EnT)
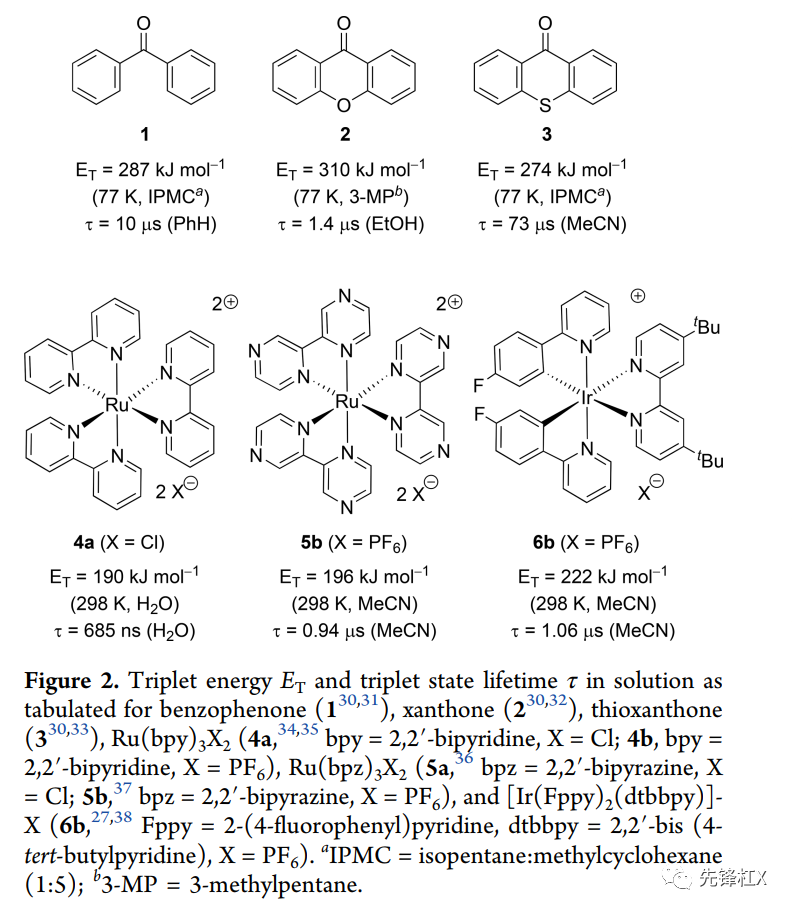
光敏剂吸收光后,比其它类型分子更容易发生系间窜跃,变为三重激发态T1。当底物分子与三重态光敏剂碰撞时,光敏剂可将三重态能量传递给底物。因此光敏剂的选择是十分重要的,常见的三重态的光敏剂有二苯甲酮、氧杂蒽酮、噻吨酮、Ru复合物、Ir复合物等。底物在三重激发态时比基态时更活泼,因此通过三重态能量转移机制的光催化反应在有机合成中发挥了巨大作用。
基因密码子扩展技术
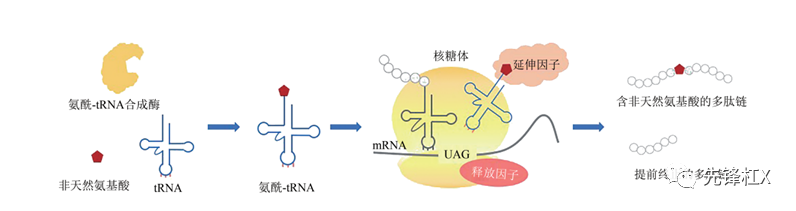
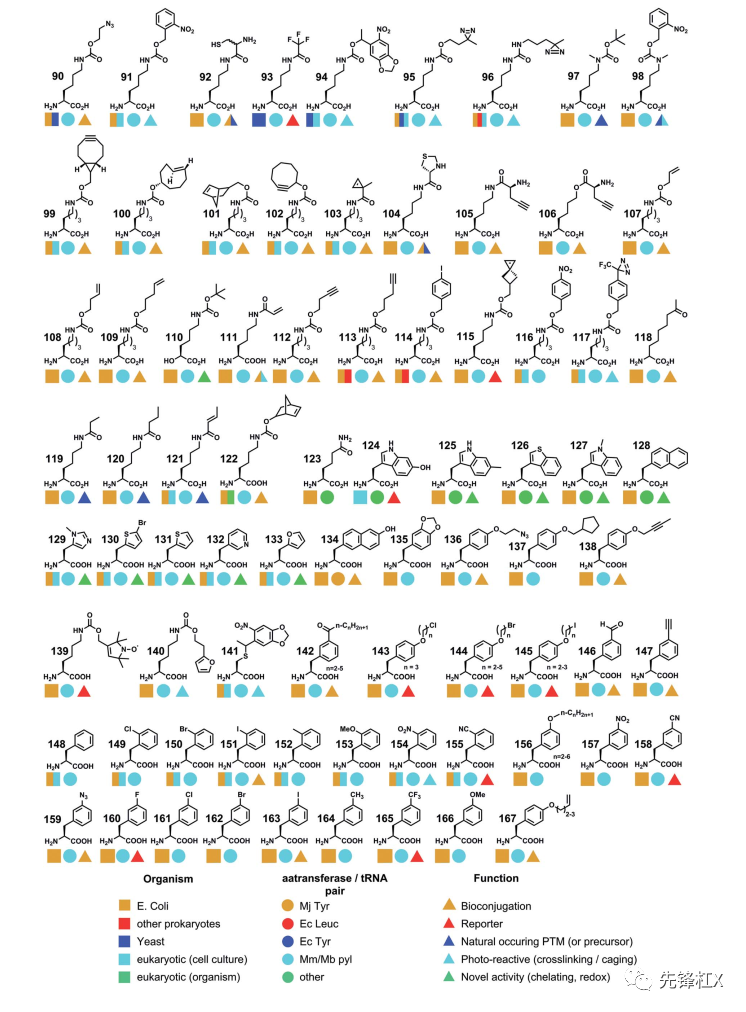
基因密码子扩展技术可以将非天然氨基酸特异性地引入目标蛋白的特定位点,利用非天然氨基酸中特殊官能团赋予蛋白新的功能。其原理是设计一对正交的tRNA和氨酰tRNA合成酶,利用琥珀密码子UAG,在蛋白翻译过程中向目标蛋白中引入一个特定的非天然氨基酸。目前通过基因密码子拓展技术可以将超过150种非天然氨基酸引入目的蛋白中。

光酶人工构建的背景
光催化合成手性手性化合物主要是借助于两种催化方式(1)选择手性光敏剂-Single Catalyst 。(2)将非手性光敏剂和手性催化剂相结合-Dual Catalysis 。但是,光催化的手性控制通常存在对映选择性低、氧气敏感、催化剂用量高、底物谱窄的缺陷。而酶催化可以将底物控制在活性口袋中,精确控制手性,并可以进一步通过定向进化精准调控口袋以提高酶的对映选择性。那如果将光敏剂也引入酶的活性口袋中,进一步调节酶口袋、底物、光敏剂之间的相互作用,就会构建出高效且选择性高的光酶。
而将光敏剂通过基因密码子拓展技术引入目的蛋白,遇到的第一个问题就是选择什么光催化剂?我们需要考虑以下几点:(1)水溶性好。(2)在光催化条件下能量转移,且三重态能量高、寿命长。(3)有合适的引入非天然氨基酸的正交tRNA和氨酰tRNA合成酶体系。考虑以上三点,对可引入目的蛋白的150种非天然氨基酸和常用的三重态光敏剂进行结构比对并取交集,不难发现二苯甲酮是一个很好的选择。而验证人工光酶催化可行性的模式反应,可以选择二苯甲酮光催化的[2+2]环加成反应。
因此,这两篇人工设计光酶的工作共同验证了可介导对映选择性能量转移的生物催化过程。
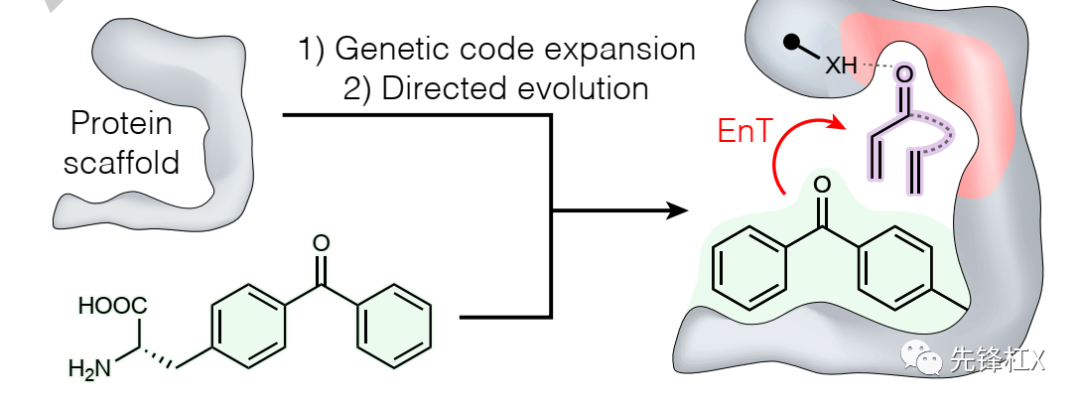
吴钰周、钟芳锐课题组和陈希课题组合作的工作
选择的蛋白骨架:多效调节因子LmrR ,其二聚体界面有一个大的疏水口袋。
选择的光催化剂:4-Benzoylphenylalanine (BpA)
选择的模式反应:吲哚衍生物的环加成。
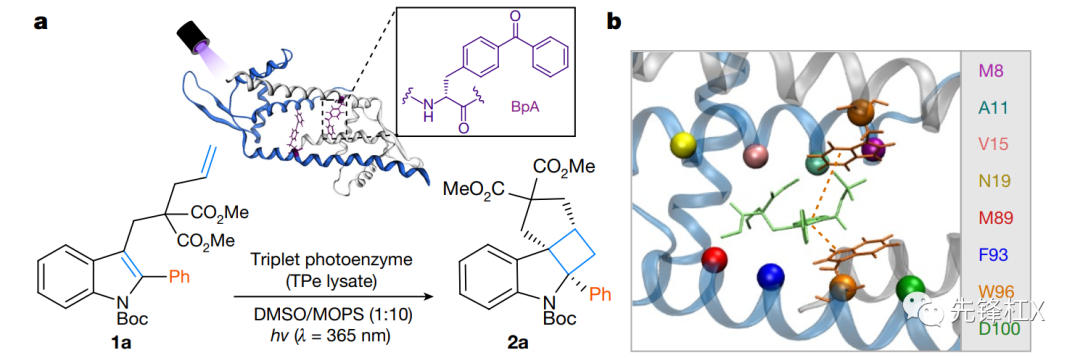
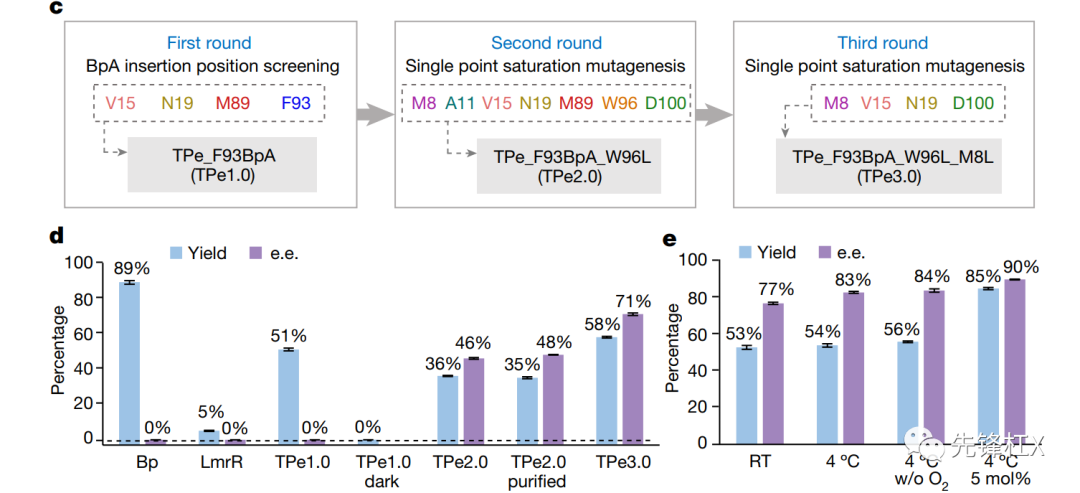
改造过程:通过分子对接确定重要的8个氨基酸残基:W96, D100, A11 ,M8 是确保底物的结合活性。V15, N19, M89, F93 和吲哚衍生物距离合适,可进行能量转移。因此首先在V15, N19, M89, F93中确认了BpA合适的插入位点,构建了TPe_F93BpA (TPe1.0) 。进一步通过对其余7个氨基酸进行了两轮定向进化,得到了TPe_F93BpA_W96L (TPe2.0) 和TPe_F93BpA_W96L_M8L(TPe3.0) 。TPe3.0 催化1a生成2a的产率达到了58%,ee值达到了71%。
反应条件的优化:通过降低反应温度(4 ℃)和提高催化剂用量(5 mol%)可将TPe3.0 催化反应的产率提高到85%,ee值提高到90%。同时发现在有氧气条件下不会影响光酶TPe3.0的催化性能(氧气是一种高效的三重态淬灭剂)。
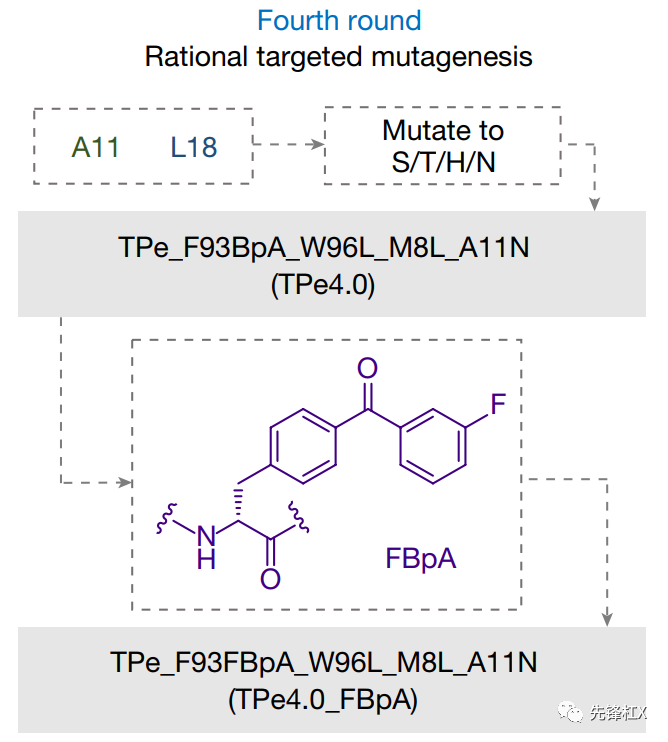
机制解析及进一步改造:通过TPe3.0-底物晶体结构来探究底物和光酶之间的相互作用,进一步对TPe3.0进行第四轮定向进化并引入新的光敏剂3-fluoro-4-benzoylphenylalanine (FBpA) 获得了优异的突变体TPe4.0_FbpA。
反应谱的拓展:共合成15种环加成产物。
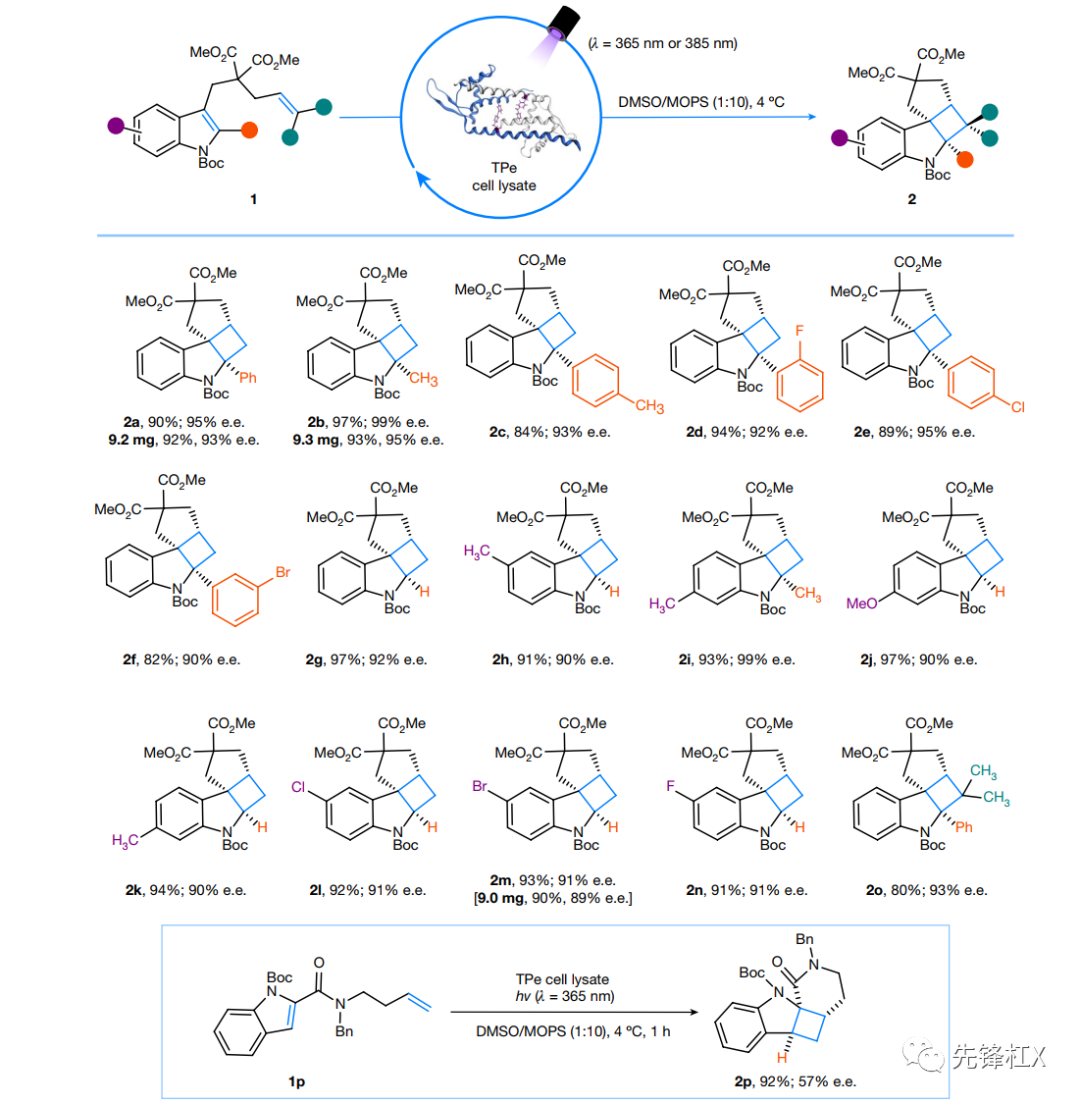
Anthony P. Green课题组的工作
选择的蛋白骨架:Diels-Alderase DA_20_00,同样具有一个大的疏水口袋。
选择的光催化剂:4-Benzoylphenylalanine (BpA)
选择的模式反应:喹诺酮的环加成。
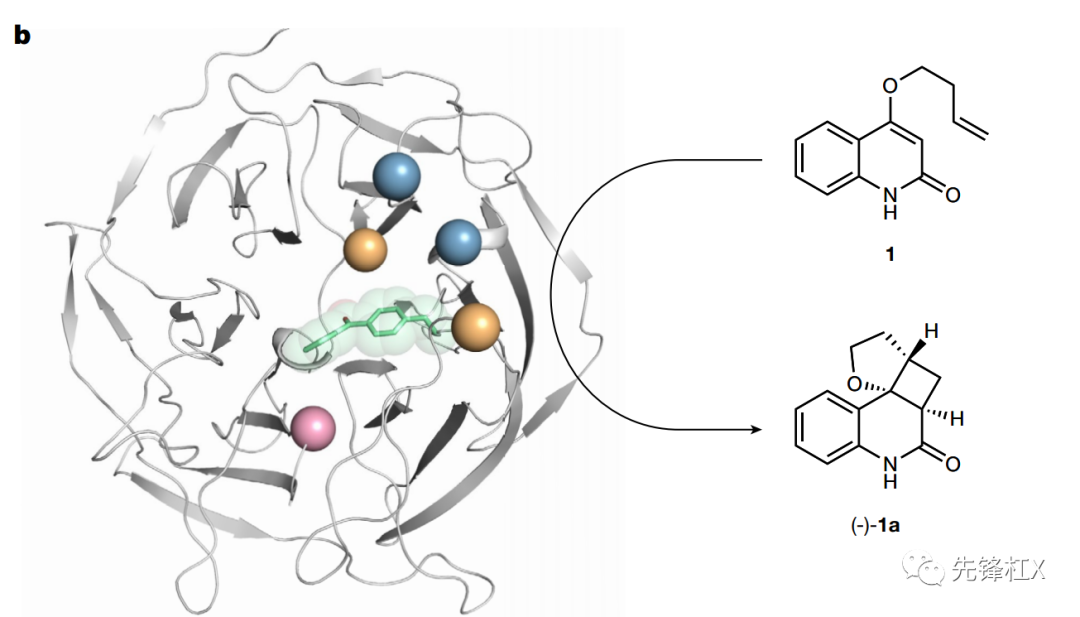
改造过程:将BpA作为光敏剂通过基因工程引入DA_20_00疏水空腔内的173位获得活性光酶EnT1.0。进一步将 BpA173附近的 8个残基突变为丙氨酸,构建EnT1.0_M90A(EnT1.1)使得催化活性和e.e.值提升。通过定向进化和高通量筛选,获得了光酶EnT1.3。
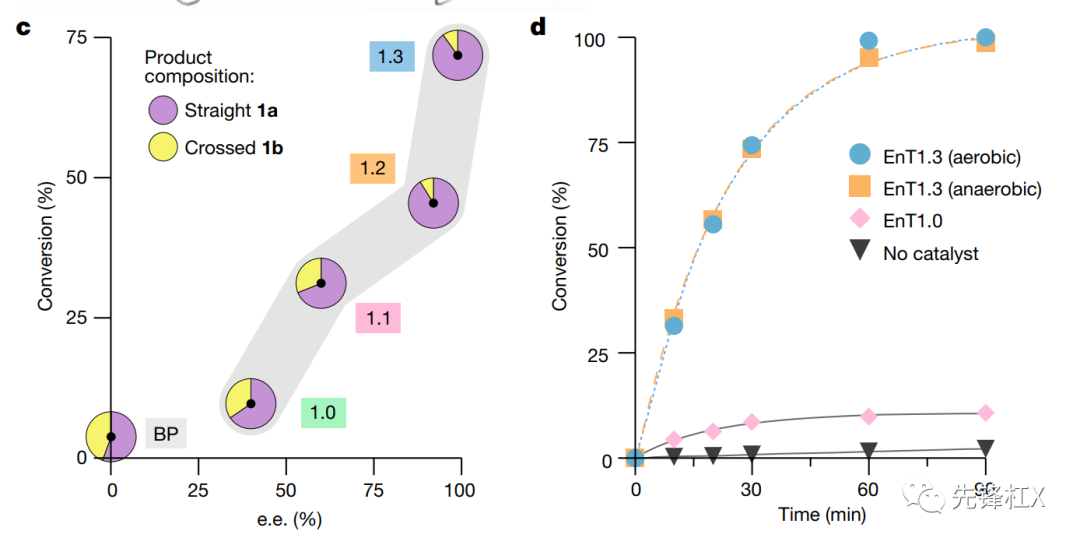
反应条件的优化:通过降低反应温度可将EnT1.3可提高催化反应的产率和ee值提高,可能是低温延长了三重态光敏剂的寿命。同样发现在有氧气条件下不会影响光酶EnT1.3的催化性能。
反应谱的拓展:共合成15种环加成产物。
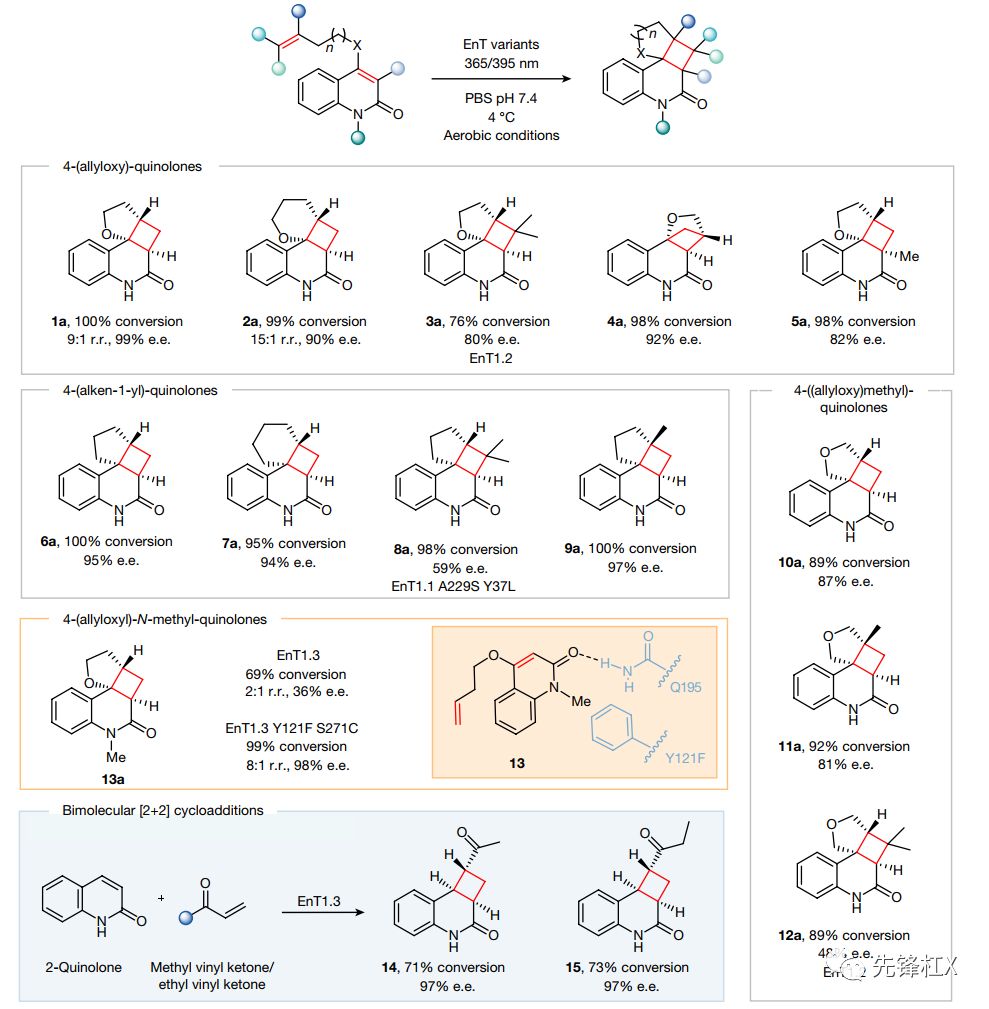
1. 这两篇人工设计光酶的工作将光催化的三重态能量转移过程与蛋白质的可调节精细疏水口袋相结合,充分利用了酶的高效选择性和光催化的高反应性,拓展了天然酶可催化的底物范围。
2. 通过挖掘更多的光敏剂和建立更多的正交的tRNA和氨酰tRNA合成酶体系,可设计的人工光酶的潜力将是无穷大的。




