【Org. Lett.】大连理工大学林禄清/大连医科大学马晓东团队:光诱导铜催化1,3-丁二烯芳胺化反应实现烯丙基胺高效合成

烯丙基胺类化合物广泛存在于天然产物、药物分子及生物活性物质中,其高效合成方法的研究一直是有机化学领域的热点。然而,利用廉价易得的1,3-丁二烯、芳基卤化物和胺三组分直接构建烯丙基胺面临巨大挑战:芳基自由基易发生氢原子转移或Heck型副反应,导致目标产物选择性差。近日,大连理工大学林禄清课题组联合大连医科大学马晓东课题组在Organic Letters上发表了一项创新研究,报道了一种可见光驱动的铜催化1,3-丁二烯芳胺化反应,成功实现了烯丙基胺的高效、高选择性合成。
1,3-丁二烯作为一种大宗化工原料,其多官能团化是获取高附加值化合物的重要途径。尽管过渡金属催化的氨基烷基化、氧烷基化等方法已取得进展,但芳基卤化物与胺参与的三组分芳胺化反应仍鲜有报道。传统双电子路径易发生Heck偶联和Buchwald-Hartwig胺化等竞争反应,而单电子路径中芳基自由基的高反应活性也导致其易从富电子位点攫取氢原子或发生Heck型加成。
最优条件:研究团队基于其在光铜催化领域的持续探索,提出了一种可见光驱动的铜催化新策略。通过优化反应条件,团队发现以Xantphos为配体、CuI为催化剂、K₂HPO₄为碱、苯甲腈为溶剂,在可见光照射下,芳基碘化物、1,3-丁二烯和脂肪胺可顺利发生三组分偶联,以最高57%的分离收率和优异的区域选择性(E/Z≤5:1)得到目标烯丙基胺产物。控制实验证实,铜催化剂、配体和光照均为反应高效进行的关键因素,且该策略可成功放大至8 mmol规模。
底物适用范围:该反应展现出广泛的底物适用范围。在芳基碘化物方面,无论是缺电子的酯基、醛基、酮基、氰基取代底物,还是电中性和富电子的芳基碘化物,均能顺利转化为相应产物。邻位、间位取代以及多取代芳基碘化物同样表现良好。杂环芳基碘化物中,噻吩和吲哚衍生物可给出中等到良好的产率,而吡啶底物反应性较低。在胺的拓展中,环状及无环脂肪族二级胺均可参与反应,兼容酯基、氯、硫醇、Cbz等多种官能团。一级胺也能顺利反应且未观察到过度烯丙基化产物。尤为值得一提的是,含有复杂药物骨架的底物如吉非罗齐、丙磺舒、布洛芬衍生物,均能以20-52%的产率得到目标产物,展示了该方法在药物后期修饰中的潜力。芳香胺及氧/硫亲核试剂在该条件下反应性不佳。
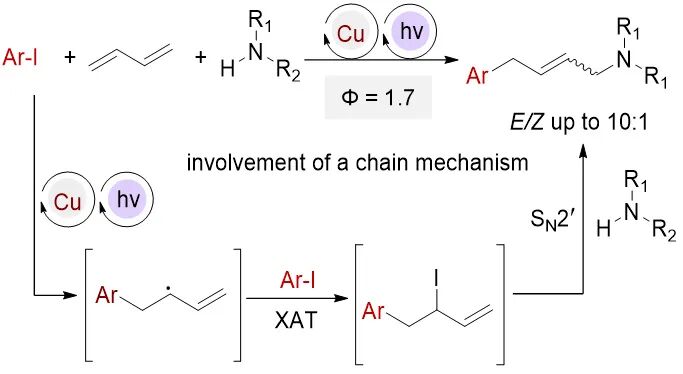
机理探究:为揭示反应机理,研究团队进行了一系列实验。UV-vis光谱分析显示CuI与Xantphos的混合物在350-400 nm范围有吸收,暗示了光活性物种的形成。自由基捕获实验表明,加入TEMPO后反应完全被抑制,且二苯二硫醚存在下检测到自由基-SPh加合物5,证实了自由基途径的参与。光开关实验发现反应在无光照条件下仍可继续进行,结合量子产率Φ=1.7的测定结果,表明反应中存在链式传递过程。部分含羰基的芳基碘化物在无铜催化下也能反应,提示胺化步骤可独立于铜催化剂。
基于以上结果,团队提出了可能的机理:光激发形成的铜配合物与芳基碘化物作用生成芳基自由基,随后被1,3-丁二烯捕获形成烯丙基自由基。该自由基可通过三条路径转化:(1) 与Cuᴵᴵ物种结合形成烯丙基铜中间体,经外球亲核进攻得到产物;(2) 经还原消除生成烯丙基碘中间体,再与胺反应;(3) 从另一分子芳基碘化物攫取碘原子生成烯丙基碘,同时再生芳基自由基维持链式循环。无论何种路径,Heck型副产物的生成均被有效抑制。
本研究成功开发了一种光诱导铜催化1,3-丁二烯芳胺化反应,通过"过量二烯作为自由基捕获剂"、"苯甲腈溶剂与过量二烯协同抑制氢原子转移"倾向于形成烯丙基碘/三价铜中间体,有效解决了芳基自由基参与反应的关键难题。该方法为烯丙基胺的合成提供了新途径,其涉及的烯丙基碘自由基链式过程也为开发无过渡金属催化体系提供了新思路。
该研究得到了国家自然科学基金(No. 22371027)的资助。
论文信息:
Light-Induced Copper-Catalyzed Arylamination of 1,3-Butadiene, Sijia Li, Hang Luo, Lei Gao, Qiwen Lin, Shizhao Xu, Xiaodong Ma*, Luqing Lin* Organic Letters, 2026, DOI: 10.1021/acs.orglett.6c00447
DOI:10.1021/acs.orglett.6c00447
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




