【Angew】 上海交通大学吴晶晶团队:光催化立体化学编辑策略实现多个甾体天然产物的高效合成
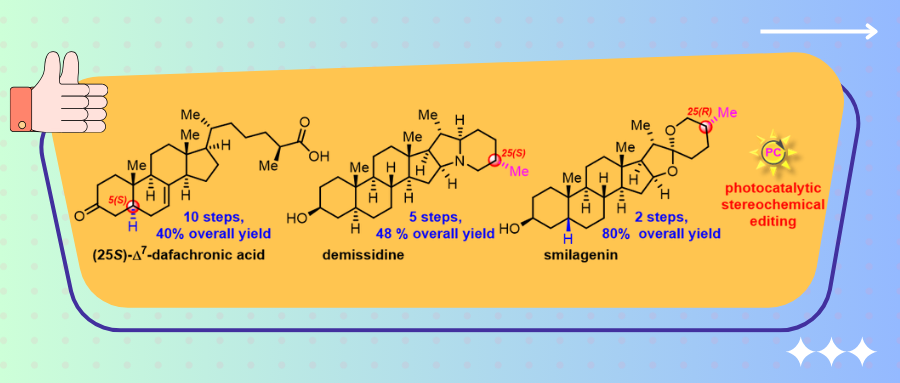
近日,上海交通大学吴晶晶课题组报道了利用光催化立体化学编辑的策略,通过对甾体分子中三级C-H键的精准调控,成功实现了(25S)-Δ7-Dafachronic acid、Demissidine 和 Smilagenin的简明合成。这是迄今为止这些天然产物最高效的合成路线,展示了立体化学编辑在提高天然产物合成效率方面的显著影响。该策略的核心在于通过底物设计,促使光催化剂(十钨酸钠)进行特定位置的氢原子攫取(HAA),形成自由基中间体,进而实现区域选择性和立体选择性的化学键断裂与重构。相关研究成果发表在Angew. Chem. Int. Ed.上线发表。
(25S)-Δ7-Dafachronic acid(1)是一种首次在线虫中发现的类固醇激素,作为核激素受体DAF-12的配体,其在线虫生命周期和寿命调控中发挥关键作用。鉴于DAF-12信号通路在多种寄生线虫中普遍存在,(25S)-Δ7-Dafachronic acid及其衍生物展现出作为抗线虫试剂的广泛应用前景。Demissidine(2)是一种从马铃薯中分离的甾体生物碱,研究表明其具有抑制肝肿瘤细胞(HepG2)生长的生物活性。此外,从天门冬中提取的甾体皂苷元Smilagenin(3)因其对阿尔茨海默病和帕金森病表现出神经保护作用而备受关注,被认为是一种具有开发潜力的苗头分子 (图1, a)。这些分子因其独特的结构和显著的生物活性,吸引了众多合成化学家的兴趣。合成过程中,C5((25S)-Δ7-Dafachronic acid)、C25(Demissidine&Smilagenin)立体中心的构筑尤为重要,对于这一关键步骤,传统合成方法步骤繁琐,区域选择性和立体选择性难以精准控制 (图1, b-c)。因此,开发一种高效、精准的立体化学编辑策略,对于合成具有复杂结构和特定生物活性的甾体分子至关重要。

图1.(25S)-Δ7-dafachronica acid (1)、desmissidine (2)、smilagenin (3)的结构,以及目前发展的的合成策略(来源:Angew. Chem. Int. Ed.)
受Wendlandt工作的启发,作者采用十钨酸钠(NaDT)作为氢原子攫取试剂,在真实底物上进行C5异构化实验。他们以廉价的鹅去氧胆酸(26)为起始原料,经C24酯化后,使用TEMPO/NaClO选择性氧化空间位阻较小的C3位羟基,以85%的收率得到27a。然而,在Wendlandt的标准条件下,底物27a未发生差向异构化。当使用Ac-保护C7位羟基时,底物27c在24小时内以86%的转化率得到28c。进一步添加1 mol% NaDT并延长反应时间24小时后,差向异构化比例显著提高,以95%的收率和96:4的非对映选择性得到产物28c。通过水解和缩合两步反应,28c顺利转化为氧化还原活性酯25。随后,在作者先前报道的标准条件下,通过光诱导脱羧烯丙基化反应以71%的收率得到化合物29。使用Burgess试剂进行消除反应生成△7(8)烯烃,经水解得到丙烯酸24。最后,以张万斌教授发展的(S,Sp)-RuPhox-Ru为手性催化剂、NaHCO3和PPh3存在下,于20 bar H2压力下对丙烯酸进行不对称氢化,成功构建了C25手性甲基,反应具有优异的收率和非对映选择性(d.r.>20:1)。由此,作者以总步骤10步、40%的总收率实现了(25S)-Δ7-Dafachronic acid(1)的简洁合成(图2)。
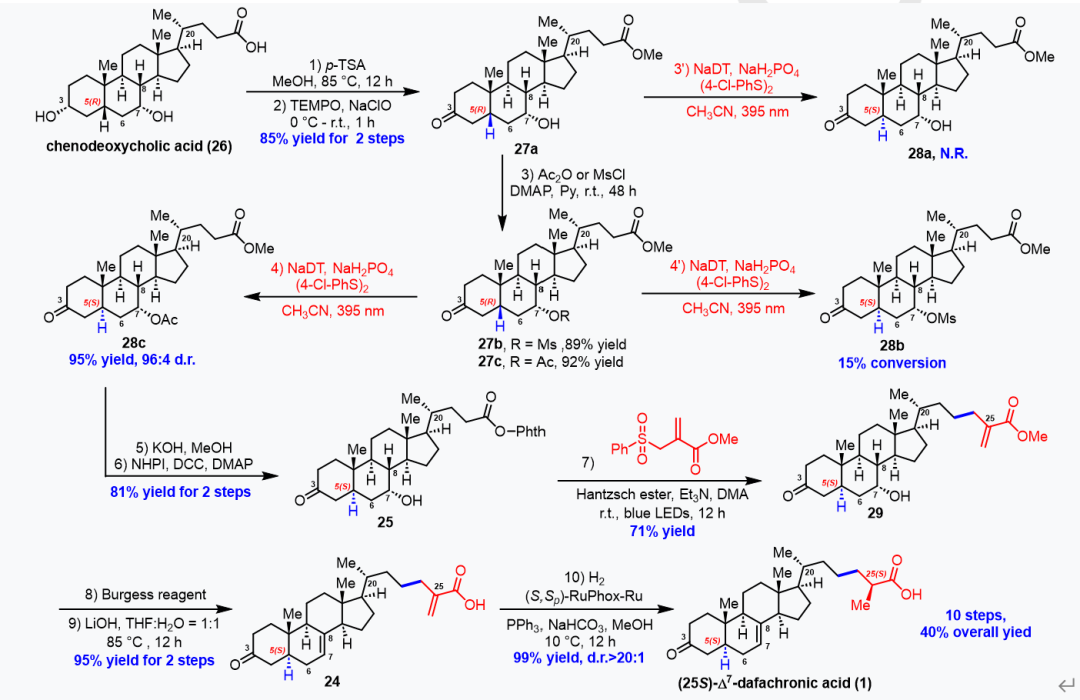
图2. 从鹅去氧胆酸合成(25S)-Δ7-dafachronic acid的十步法合成路线(来源:Angew. Chem. Int. Ed.)
在实现了(25S)-Δ7-Dafachronic acid(1)的高效合成后,作者进一步将立体化学编辑策略应用于Demissidine(2)和Smilagenin(3)的合成中。作者首先采用Morzycki报道的三步法从tigogenin醋酸酯(4)合成13,通过酸性条件对氨基进行质子化,使α-氨基位置失活,从而实现C25-H的选择性HAA反应,以93%的收率和大于20:1的非对映选择性得到C25差向异构化产物14。最后14再经过一步水解,这样作者就以总步骤5步、48%的总收率高效获得目标天然产物demissidine(图3)。
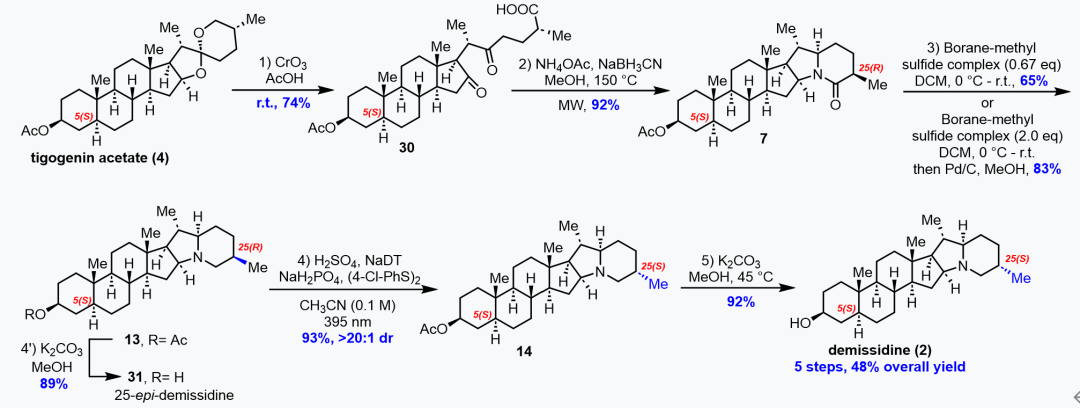
图3. 从tigogenin醋酸酯合成地demissidine的五步合成路线(来源:Angew. Chem. Int. Ed.)
随后,作者研究了该策略在同时具有A/B环顺式稠合体系和C25-甲基直立位置的同一分子中是否表现出区域选择性。作者认为,NaDT作为一种大位阻的氢原子攫取试剂,倾向于从位阻较小的位置攫取氢原子。为验证这一假设,作者使用sarsasapogenin醋酸酯32进行光化学立体化学编辑反应。正如预期,C25差向异构化产物smilagenin醋酸酯(33)以88%的收率获得,而同时发生C25和C5差向异构化的产物tigogenin醋酸酯(4)仅得到2%的收率。化合物33经水解后,以高产率得到smilagenin(3)(图4)。
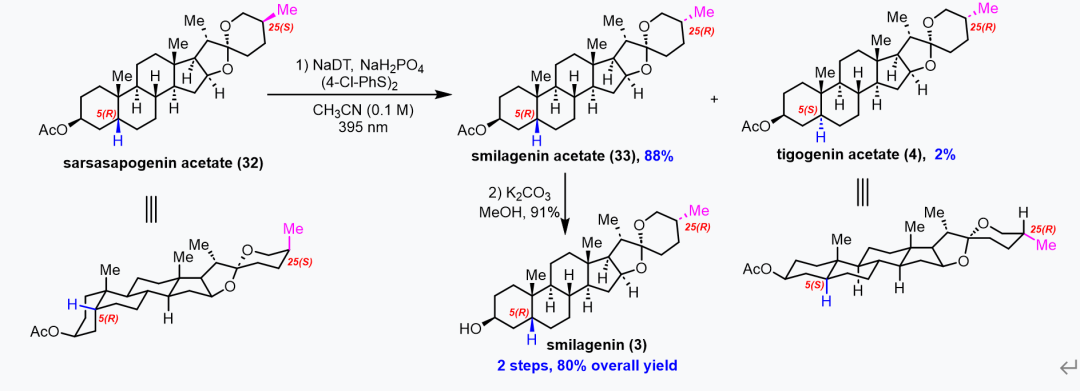
图4. smilagenin的简明合成(来源:Angew. Chem. Int. Ed.)
综上所述,通过对甾体化合物光化学立体化学编辑策略的研究,作者实现了(25S)-Δ7-dafachronic acid、demissidine和smilagenin的简洁合成。这是迄今为止这些天然产物最高效的合成路线,展示了立体化学编辑在提高天然产物合成效率方面的显著影响。通过在(25S)-Δ7-Dafachronic acid合成中采用乙酸酯保护羟基,以及在demissidine合成中对氨基进行质子化,为有效解决氢原子攫取的区域选择性问题提供了可靠的解决方案。此外,通过对sarsasapogenin醋酸酯立体化学编辑研究,作者证明了可以通过空间位阻效应调控该策略的区域选择性。
论文信息:
Photocatalytic Stereochemical Editing for the Concise Syntheses of (25S)-Δ7-Dafachronic acid, Demissidine and Smilagenin
Xiaotong Li, Zhaoguo Zhang, Jingjing Wu
Angew. Chem. Int. Ed.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




