有机-叠氮基三甲基硅烷-常见试剂介绍
【英文名称】Azidotrimethylsilane
【分子量】115.21
【CA登录号】[4648-54-8]
【缩写和别名】TMSA,TMSN3
【结构式】Me3SiN3
【物理性质】bp 95~96 oC,d 0.868 g/cm3。溶于大多数有机溶剂,通常在CH2Cl2、THF 和MeCN 中使用。
【制备和商品】该试剂在国内外化学试剂公司有销售。实验室可以方便地通过三甲基氯硅烷与叠氮化钠反应来制备[1]。
【注意事项】该试剂对湿气敏感,在500 oC会发生分解。建议在干燥阴凉处保存,在通风橱中操作和使用。
叠氮基三甲基硅烷(TMSA) 是有机合成中应用非常广泛的试剂之一。它可以看作是金属叠氮化物的替代物,几乎能够发生金属叠氮化物的所有反应。但是,TMSA能够在许多有机溶剂中反应,所以更容易操作和获得较好的结果。该试剂的反应性质来自于分子的两个组成部分,以叠氮基所发生的反应具有较高的合成价值。
TMSA 可以方便地与卤代烃或者磺酸酯发生反应,生成相应的叠氮化合物 (式1)[2,3]。反应也可以在无催化剂存在的情况下进行,但一般需要较高的反应温度。
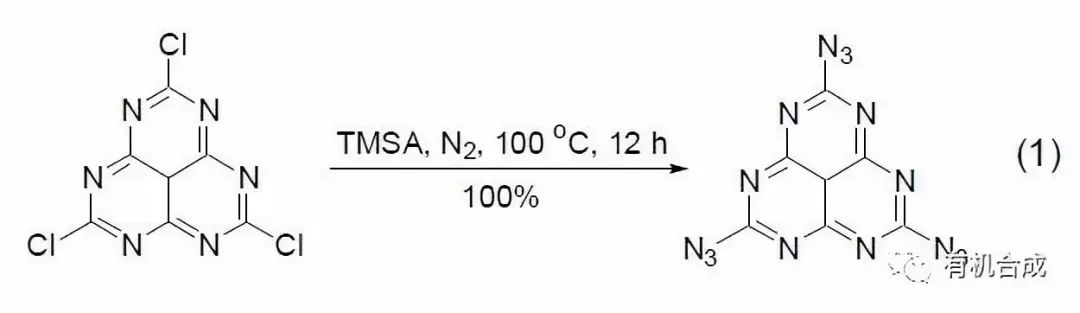
TMSA 与那些容易生成碳正离子的缩醛衍生物的反应具有较高的合成价值,特别是在糖化学转变中,用该方法可以方便地得到糖的叠氮化合物。卤代缩醛或者硫代缩醛具有较高的反应活性 (式2,式3)[4,5],半缩醛或者半缩醛的羧酸酯可以在反应中原位转化成为离去能力较强的官能团后再进行叠氮化反应[6,7]。
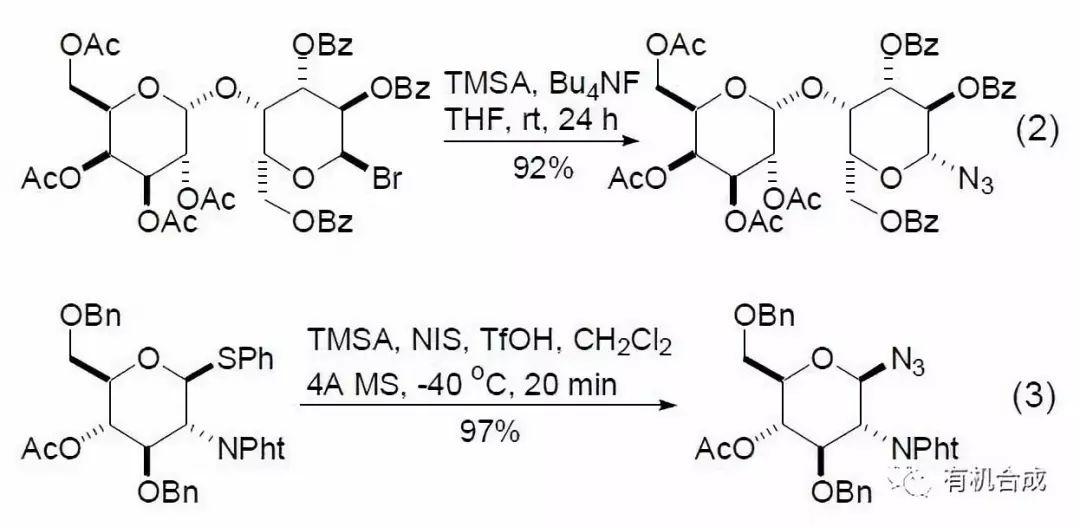
TMSA 可以在金属催化剂的作用下与环氧化合物发生开环反应,生成1(2)-羟基-2(1)-叠氮化合物。该产物进一步被还原就得到1(2)-羟基-2(1)氨基化合物,所以具有重要的合成价值。选择适当的催化剂,该反应可以显示出高度的立体选择性 (式4)[8]。如果使用手性催化剂,可以实现高度的对映体选择性[9]。
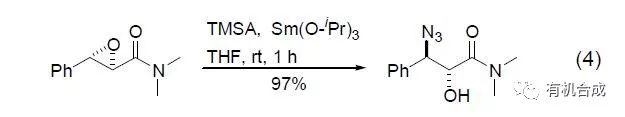
由于 TMSA 中的叠氮基具有1,3-偶极结构,所以很容易与缺电子炔烃发生[3+2]成环反应,生成三氮唑的衍生物 (式5)[10]。文献报道,使用CuI 为催化剂可以提高炔烃的反应活性[11]。如果反应底物为氰基的话,则生成四氮唑的衍生物[12~14]。该反应需要催化剂的存在下才能进行,许多路易斯酸金属催化剂可以用于该目的。有时金属叠氮化物不能够进行的反应,TMSA 可能会给出很好的结果 (式6)[12]。
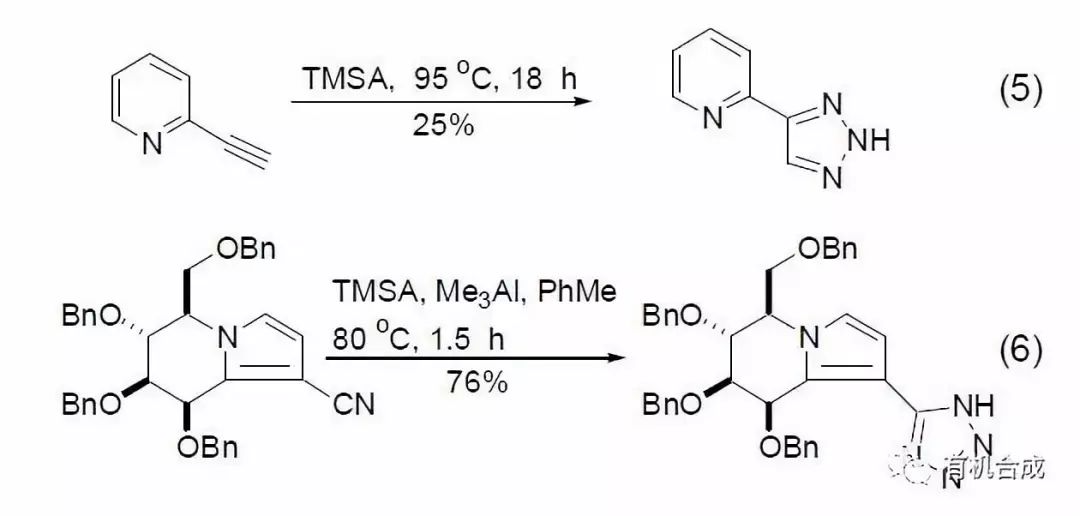
参考文献
1. Nishiyama, K.; Yamaguchi, T. Synthesis, 1988, 106.
2. Lu, J.; Jayaprakash, K. N.; Schlueter, U.; Fraser-Reid, B. J. Am. Chem. Soc., 2004, 126, 7540.
3. Miller, D. R.; Swenson, D. C.; Gillan, E. G. J. Am. Chem. Soc., 2004, 126, 5372.
4. Ohlsson, J.; Larsson, A.; Haataja, S.; Alajaeaeski, J.; Stenlund, P.; Pinkner, J. S.; et al. Org. Biomol. Chem., 2005, 3, 886.
5. Pratt, M. R.; Bertozzi, C. R. J. Am. Chem. Soc., 2003, 125, 6149.
6. Bodine, K. D.; Gin, D. Y.; Gin, M. S. J. Am. Chem. Soc., 2004, 126, 1638.
7. Trost, B. M.; Yang, H.; Probst, G. D. J. Am. Chem. Soc., 2004, 126, 48.
8. Tosaki, S.-y.; Tsuji, R.; Ohshima, T.; Shibasaki, M. J. Am. Chem. Soc., 2005, 127, 2147.
9. Martinez, Luis E.; Leighton, James L.; Carsten, Douglas H.; Jacobsen, Eric N. J. Am. Chem. Soc., 1995, 117, 5897.
10. Roppe, J.; Smith, N. D.; Huang, D.; Tehrani, L.; Wang, B.; Anderson, J.; Brodkin, J. et al. J. Med. Chem., 2004, 47,4645.
11. Jin, T.; Kamijo, S.; Yamamoto, Y. Eur. J. Org. Chem., 2004, 3789.
12. Terinek, M.; Vasella, A. Helv. Chim. Acta, 2003, 86, 3482.
13. Amantini, D.; Beleggia, R.; Fringuelli, F.; Pizzo, F.; Vaccaro, L. J. Org. Chem., 2004, 69, 2896.
14. Schulz, M. J.; Coats, S. J.; Hlasta, D. J. Org. Lett., 2004, 6, 3265.
本文转自:《现代有机合成试剂——性质、制备和反应》,胡跃飞等编著




