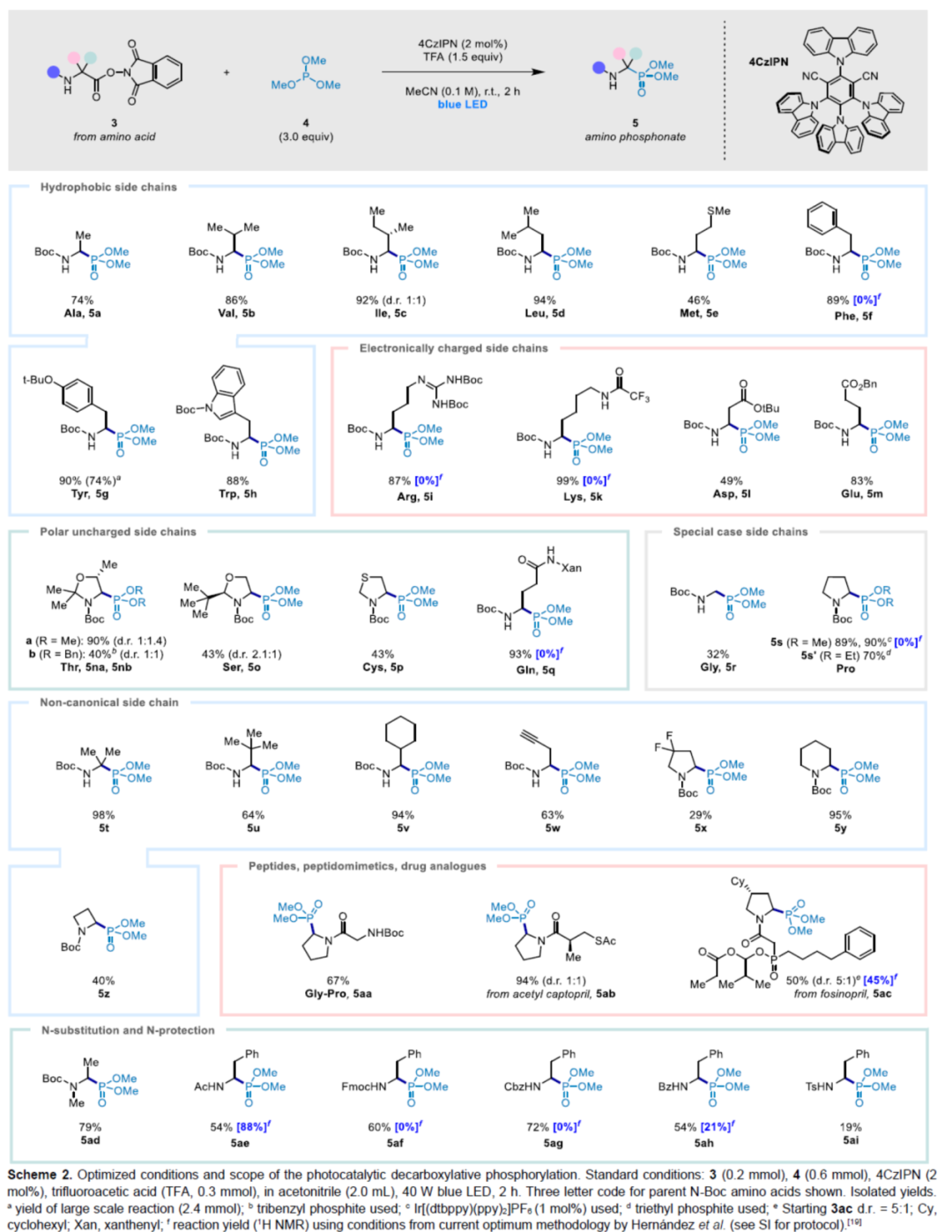
有机合成中常见光催化剂的应用
过去的十几年里,光化学反应的研究报道呈爆发式增长。过渡金属光敏剂配合物类催化剂和有机高共轭催化剂等光氧化还原催化剂广泛应用于各种有机反应,除了经典的光催化的反应(如Barton亚硝酸酯光解反应,Curtius 重排,Diels-Alder反应,脱羧卤代反应,de Mayo反应等),原来过渡金属催化偶联反应也可以在光催化条件下进行,而且相比经典条件,光催化的反应条件更加温和。另外像Pinacol偶联反应这种一百多年前发现的经典反应,化学家也开发出来光催化的反应条件【J. Am. Chem. Soc., 2013, 135, 17735】。光化学反应已成为构建化学键的强有力方法。
在有机光化学领域,光催化剂发挥着非常重要的作用。光化学反应一般是通过产生自由基进行的,简单的有机分子的自由基的产生通常需要短波长的紫外照射,氧化还原反应或加热等条件。光催化研究领域开发了过渡金属配合物类催化剂和有机高共轭催化剂,这些光催化剂能够在可见光波长范围内被激发,相比于有机小分子,对于光的吸收有更高的效率。
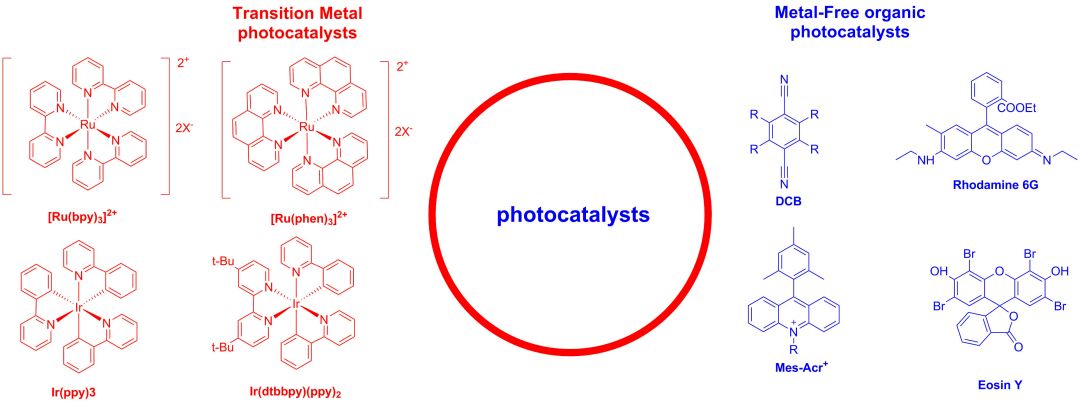
在有机合成中使用的几种最常见的光催化剂如上图所示,主要分为两类一种是过渡金属配合物光催化剂和非金属有机光催化剂。这一系列催化剂的结构都有着高度共轭体系,但也还有各自的特点,包括简单的芳香共轭基团、中性和带电体系、官能团化的有机染料和能够通过配体改变性质的过渡金属络合物。
相关机理
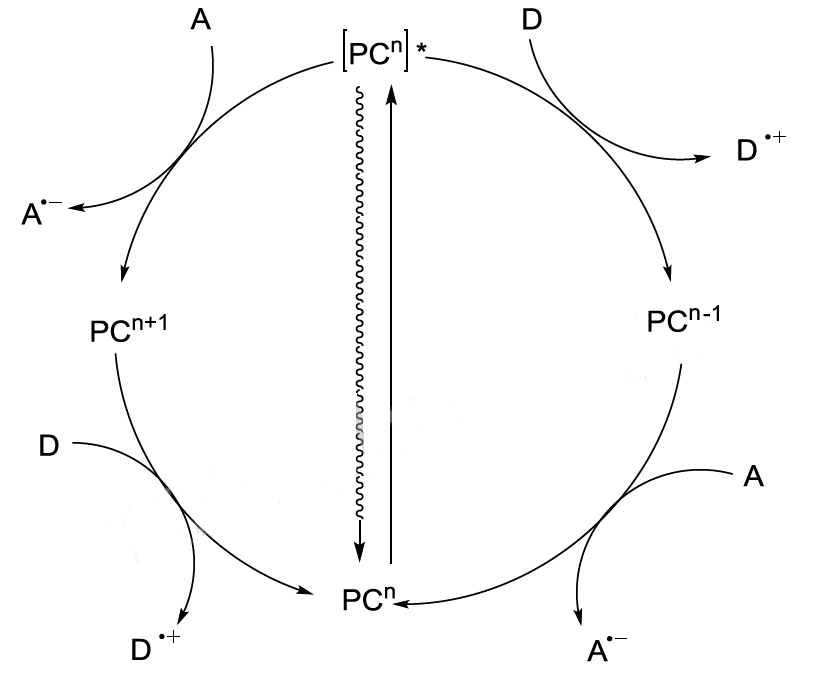
目前这些不同结构的光催化剂对反应底物的活化机理主要有三种,即单电子转移,氢原子夺取或能量转移。其中最常见机理就是光催化的单电子转移机理,光催化剂吸收光子进入电子激发态,导致其拥有很强的氧化还原性。其可以快速将电子转移到缺电子受体A,或接受富电子供体D的电子,反应循环包括氧化和还原两种路径,最终的结果是产生一对包含氧化供体(D•+)和还原受体(A•−)的反应性自由基离子。
反应实例
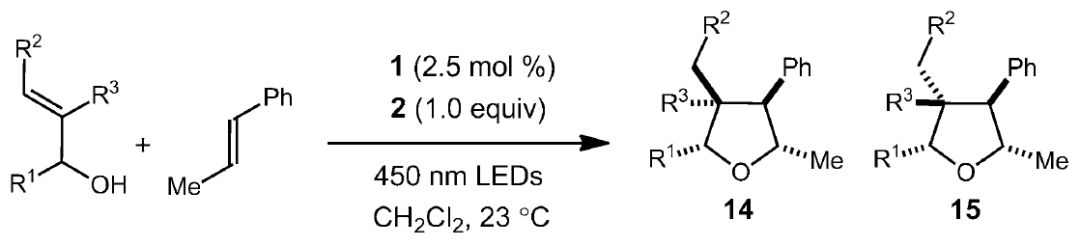
光照条件下,Mes-Acr+ClO4-作为光催化,PhCH(CN)2作为H供体,烯基醇和烯烃进行极性-自由基-交叉环加成反应。
【Angew. Chem. Int. Ed. 2013, 52, 3967 –3971】
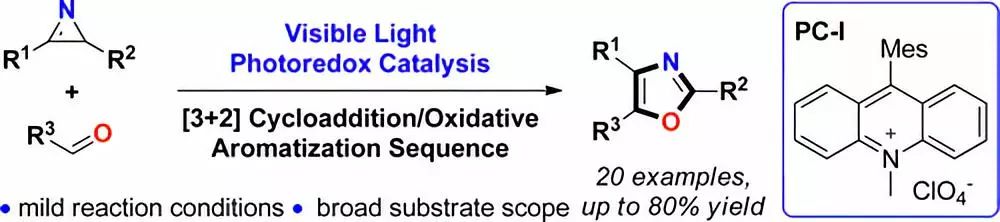
光照条件下,Mes-Acr+ClO4-催化 2H-azirines 和醛进行[3+2]环加成/氧化芳基化合成2,4,5-三取代恶唑。
【Org. Lett., 2015, 17, 4070–4073】
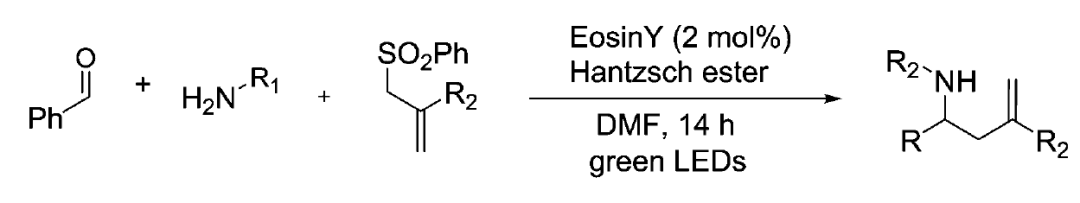
绿光LED照射下,Eosin Y催化的三组分还原偶联反应。
【Chem. Commun., 2016, 52, 14434-14437】
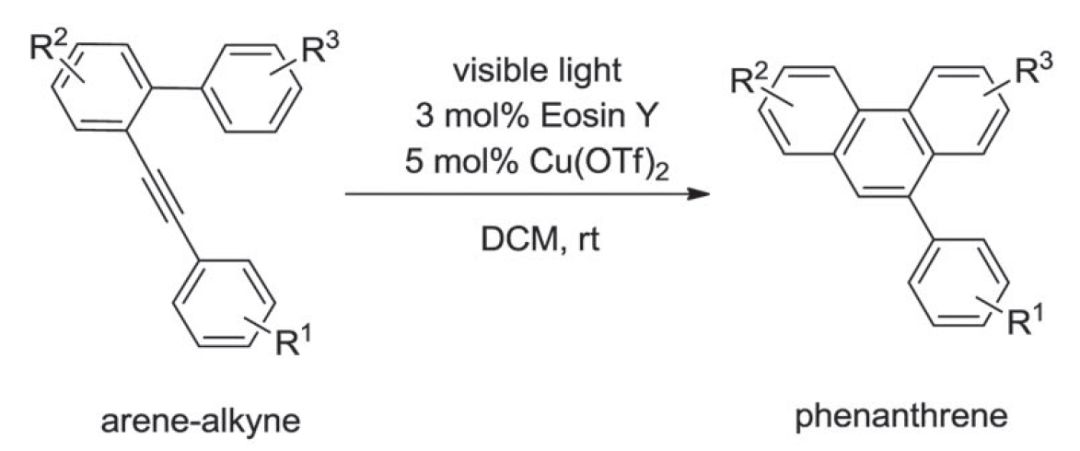
可见光照下,Eosin Y和Cu(OTf)2共催化芳基炔关环的反应。
【Chem. Commun., 2016, 52, 9909-9912】
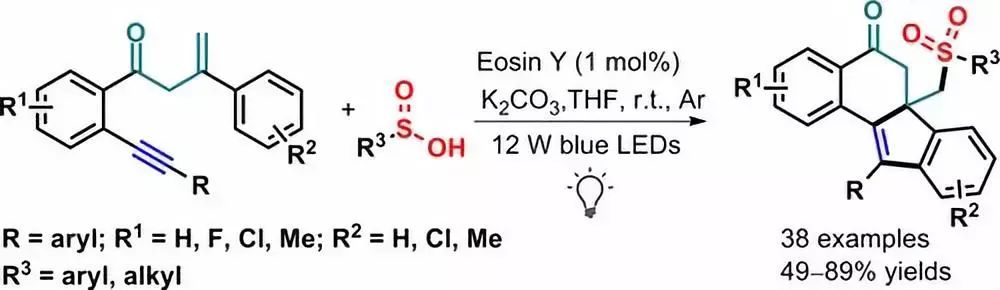
光照条件下,Eosin Y催化1,7-烯炔和亚磺酸进行二环化反应得到砜官能团化的苯并[α]芴-5-酮。
【Advanced Synthesis and Catalysis, 2017, 359, 2229-2234】
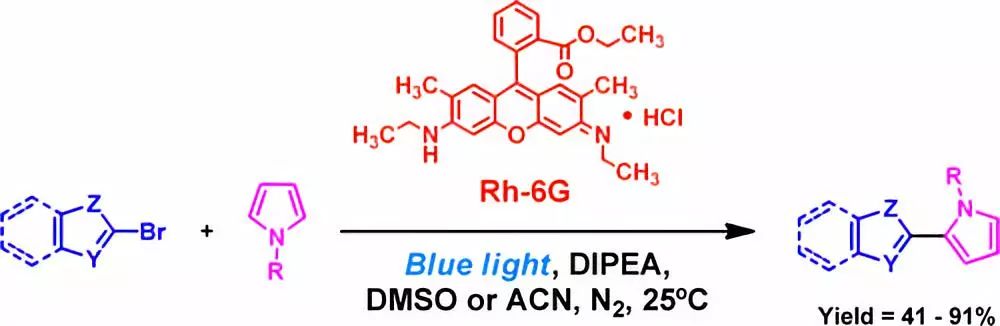
光照条件下,Rh-6G催化杂环溴代或氯代芳烃形成杂环芳烃自由基,接着和吡咯反应得到联杂环芳基化合物。
【ACS Catal., 2016, 6, 6780–6784】
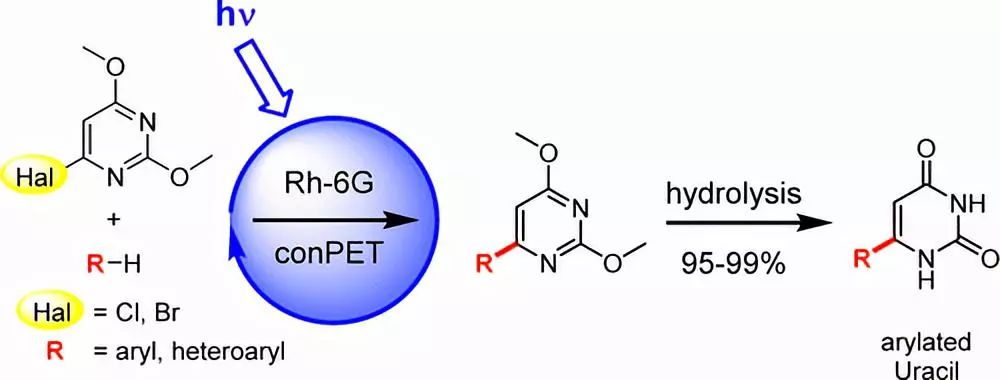
光照条件下,Rh-6G催化下通过光诱导的电子转移机理,在室温条件下卤代核酸碱基前体和C-H活化的芳环或芳杂环进行还原交叉偶联。
【J. Org. Chem. 2017, 82, 3552−3560】
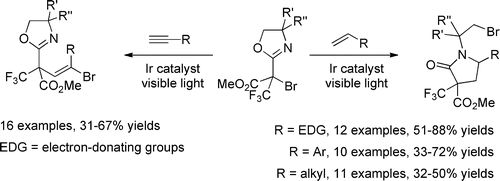
可见光照下,Ir(ppy)2(dtbbpy)(PF6)或fac-Ir(ppy)3催化三氟甲基叔溴代烃和富电子烯烃反应得到含有三氟甲基季碳的γ-丁内酰胺。此反应是一个非常好的得到三氟甲基季碳的方法。炔烃在fac-Ir(ppy)3也可以进行电子转移自由基加成反应。
【J. Org. Chem. 2016, 81, 7051−7063】
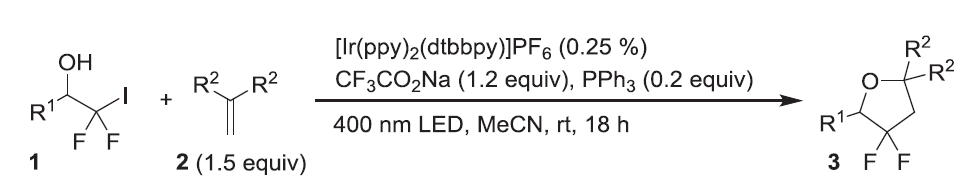
光照条件下,[Ir(ppy)2(dtbbpy)]PF6催化二氟碘甲基醇和1,1-二芳基乙烯关环得到3,3-二氟四氢呋喃。
【Tetrahedron 2018, 74, 7136-7142】
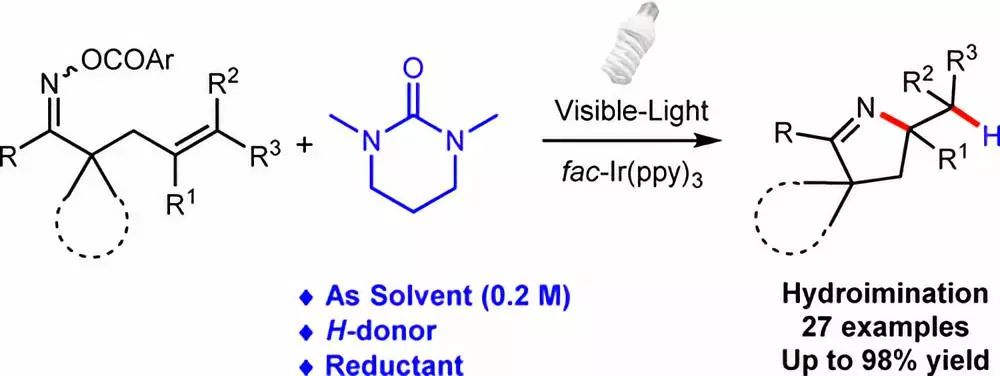
在可见光条件下,fac-Ir(ppy)3催化非活性烯烃进行氢亚胺化关环得到3,4-吡咯啉的反应。DMPU在反应中既作为催化剂再生的还原剂也作为H供体。
【Adv. Synth. Catal. 2018, 360, 1262–1266】
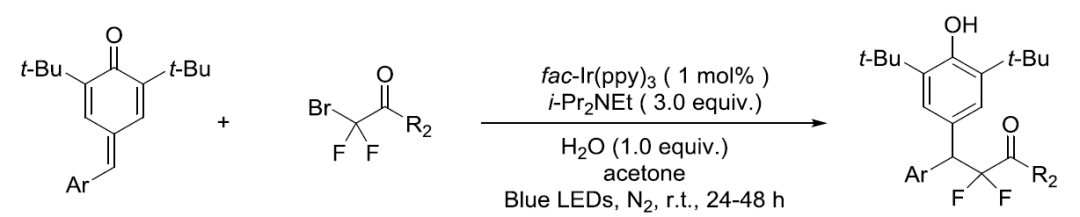
光照条件下,para-quinone methides (p-QMs)首先与*fac-Ir(ppy)3作用形成二芳基自由基,接着和二氟烷基自由基进行自由基自由基交叉偶联反应。
【Chem. Commun., 2018, 54, 3993--3996】
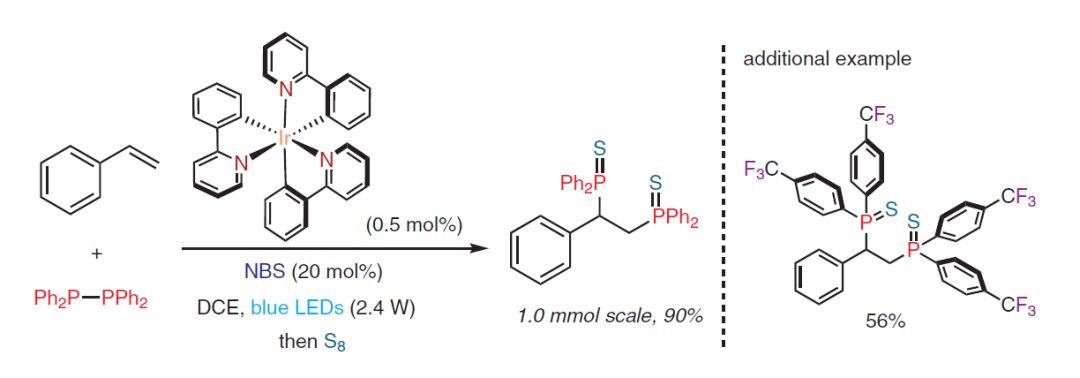
光照条件下,Ir(ppy)3催化苯乙烯进行二膦基化反应。
【Synthesis 2018, 50, 3402–3407】
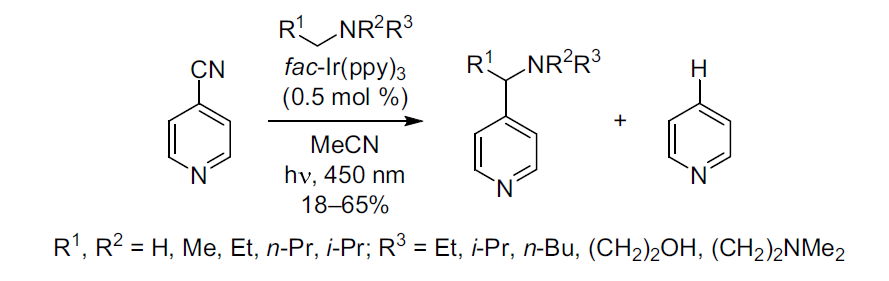
光照条件下,fac-Ir(ppy)3催化4-氰基吡啶和脂肪叔胺分别形成自由基,两个自由基偶联生成α-吡啶-4-基叔胺类化合物。
【Chemistry of Heterocyclic Compounds, 2019, 55(1), 90–92】
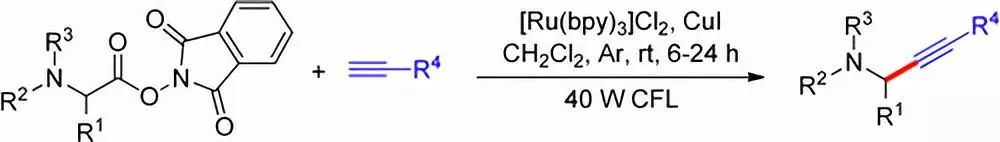
室温下,[Ru(bpy)3]Cl2/CuI催化的脱羧炔基化反应。
【Org. Lett. 2017, 19, 1016−1019】
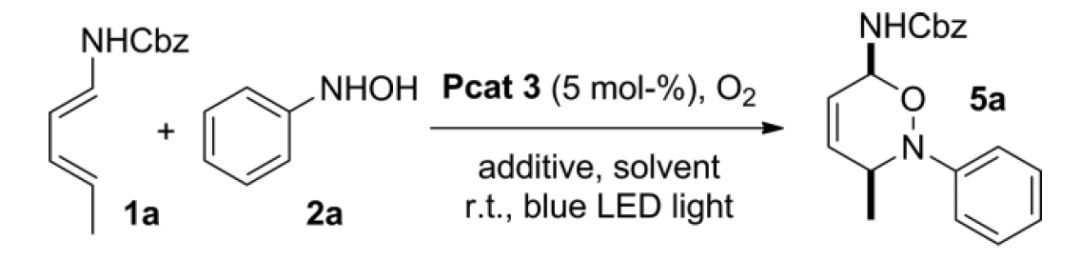
光照条件下,Ru(bpy)3Cl2作为氧化还原催化剂,将羟胺氧化为亚硝基化合物,接着进行,亚硝基-Diels–Alder反应。
【Eur. J. Org. Chem. 2017, 2095–2098】
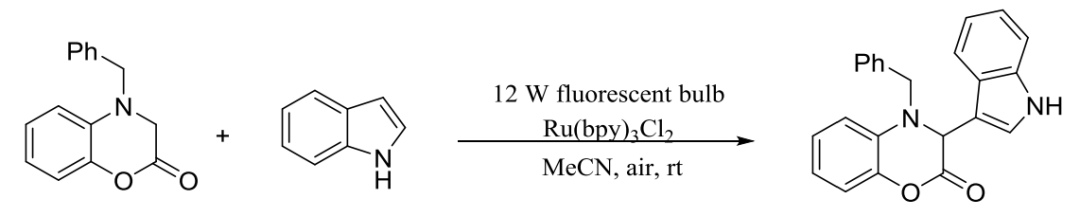
光照条件下,在Ru(bpy)3Cl2催化下,氧气作为氧化剂苯并恶嗪-2-酮和各种富电子芳环化合物进行氧化交叉脱氢偶联反应。
【Eur. J. Org. Chem. 2018, 525–531】
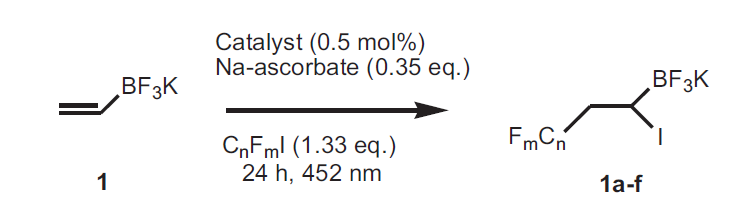
可见光照下,[Ru(bpy)3]Cl2或 [Ru(bpy)3](PF6)2催化全氟烷基碘代物对烯基三氟硼酸钾进行原子转移的自由基加成反应。
【Tetrahedron Letters, 2018, 2700–2703】
光照条件下,Ru(bpy)3Cl2催化烯基苯基硝酮,进行分子内的偶极环加成反应。
【Org. Lett., 2019, 1388–1392】
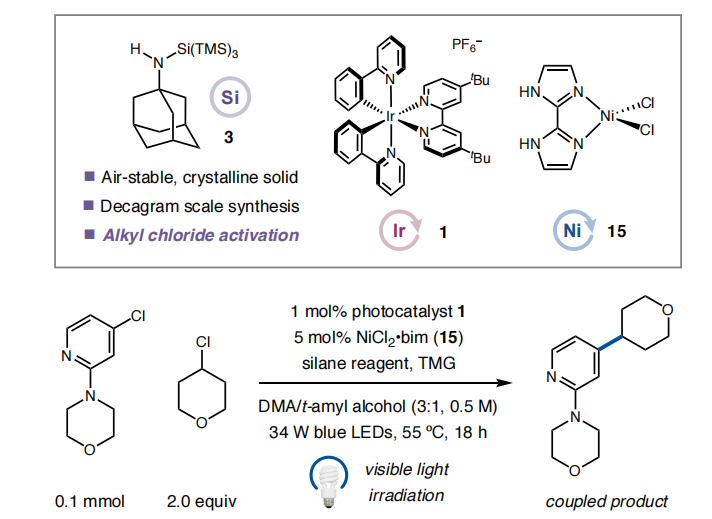
美国普林斯顿大学(Princeton University)的David W. C. MacMillan教授团队,在他们早期研究的基础上,又发展了一种在Ni/光氧化还原双催化体系下,在蓝色LED光照条件下,55℃实现低活性的氯代烷烃和氯代芳烃的还原偶联反应。作者设计了一种新型的硅烷试剂1-金刚烷氨基取代的三(三甲基硅基)硅烷3,可以克服很高的C-Cl键解离能攫取低活性氯代烷烃的氯原子,由此实现其与氯代芳香烃的还原交叉偶联。
【J. Am. Chem. Soc. 2020, 142, 11691–11697】。
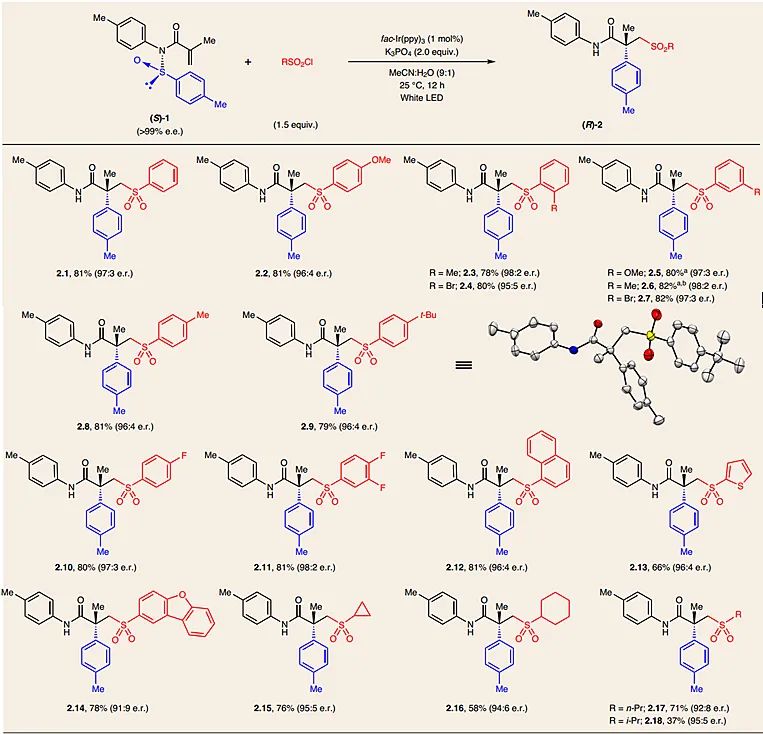
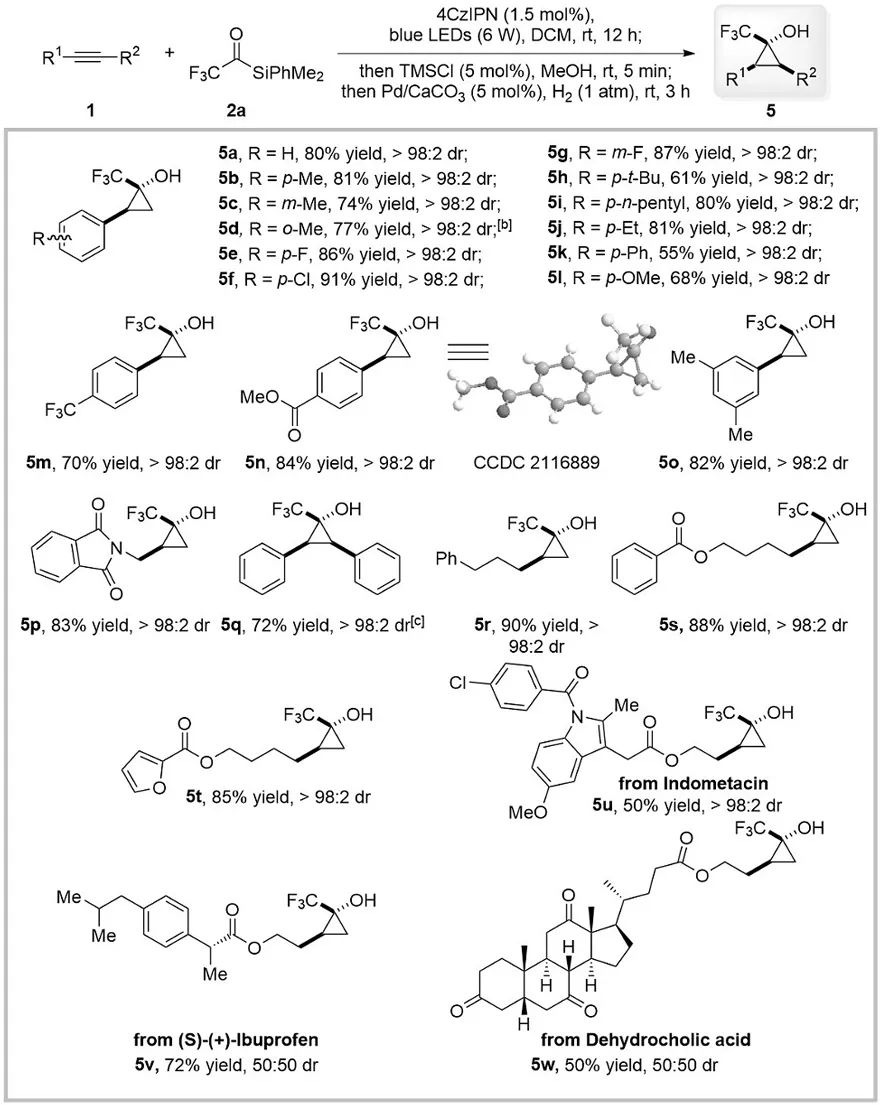
武汉大学沈晓课题组首次提出了利用三氟甲基酰基硅烷产生双亲的donor-acceptor卡宾与炔烃的[2+1]环化反应来制备环丙烯醇类化合物。
【Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202115334】
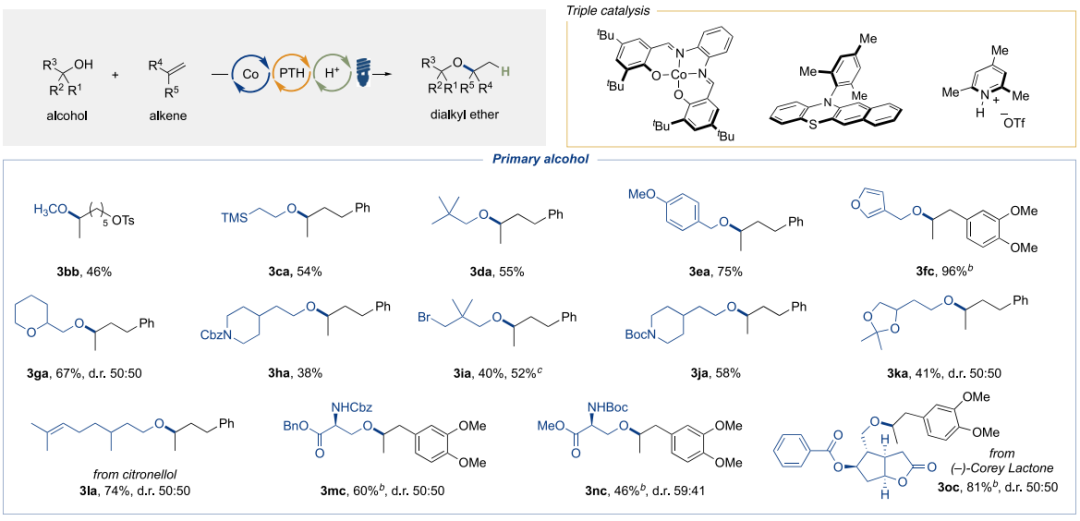
近期,Masanari Nakagawa等人报道了一种光氧化还原/Co/Brønsted酸三重催化体系下,在可见光照射下实现符合马氏规则的氢烷氧化反应。此反应可以制备各种高附加值的醚,伯,仲,叔醇都可顺利反应,可以实现常规条件下很难制备得到的醚。通过三种催化剂对质子和电子的精确控制,可以避免使用传统方法中所需的强酸和外部还原剂/氧化剂,因此此反应条件温和,官能团耐受度高。
【J. Am. Chem. Soc. 2022, 144, 7953−7959】