【Org. Lett.】中南大学阳华/郑雨/陈凯课题组: 可见光诱导钯催化烯丙位C-H烷基化反应

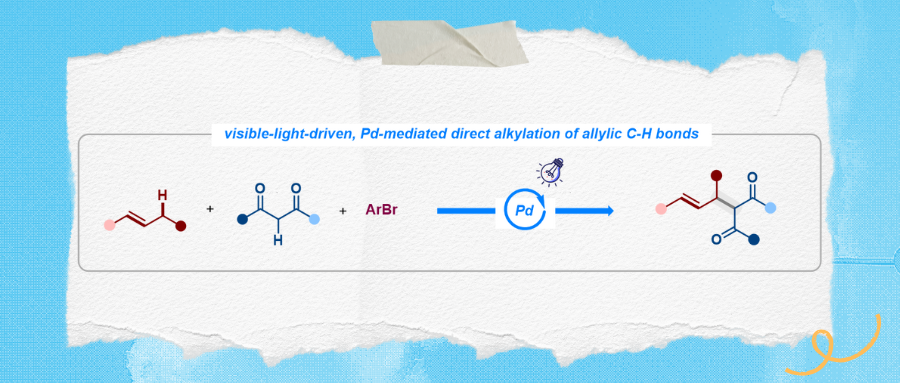
在合成化学中,快速构建具有特定官能团的碳骨架是一项关键任务。其中,带有活泼离去基团的烯丙基底物因其在广泛C-C键形成反应中的重要作用,已成为有机合成转化的核心工具。尤其值得注意的是,钯催化的Tsuji-Trost反应,凭借其高度的区域选择性和立体选择性,代表了烯丙基取代反应中最通用的策略。尽管我们充分认可这一强大转化的功效,但通过乙酸酯或碳酸酯对烯烃烯丙位进行预官能化以获得活化底物的过程本身并非易事,且反应后会产生化学计量的废弃物。因此,直接利用未活化烯烃的策略正受到越来越多的关注。与之相比,龚等人成功开发了基于氧化策略的烯丙基C-H键直接官能化方法。可以预见,尽管通过烯丙基C-H键直接官能化实现C-C键构建的反应仍有待进一步发展,但该方法必将对经典途径形成有力补充,并在多样性导向的合成中扮演重要角色。
光诱导钯催化已成为过渡金属光催化领域的研究热点,其近期进展带来了前所未有的突破。相较于传统钯催化模式,光照的引入不仅实现了钯对烷基卤化物的高效活化,更赋予了反应中间体独特的自由基特性,为新型合成策略开辟了新途径。在此背景下,基于光诱导钯催化的烯丙位直接C-H官能团化,展现出广阔的应用前景(图1 a)。
令人鼓舞的是,Gevorgyan团队近期报道了一项突破:他们利用芳基溴作为氢原子转移(HAT)试剂,成功实现了光诱导钯催化下的烯丙位C–H键胺化、磺酰化和氧化反应。该研究的突出意义在于,其有效实现了将重要的1,3-二羰基结构引入烯丙位。这类结构因兼具多功能性和高效性,在药物开发、材料设计和绿色合成中备受青睐,其生成的碳骨架广泛存在于众多生物活性分子(如α-生育酚、cohulupone和泛醌)中(图1 b)。此项工作基于我们团队先前在分子内钯催化氢原子转移反应方面的研究基础。我们设想,通过结合溴苯介导的HAT过程与光诱导钯催化下的碳亲核取代反应,应能实现烯烃的直接烯丙基C-H烷基化。这一策略的关键优势在于,它绕过了传统方法中需要预引入离去基团的繁琐步骤(图1 c)。
近日,中南大学阳华/郑雨/陈凯课题组在该领域取得突破,报道了一种可见光诱导的钯介导的烯丙位C-H烷基化反应,通过溴苯与光钯协同催化的作用,跳过了离去基团的预组装步骤,高效合成了烯丙基烷基化产物。
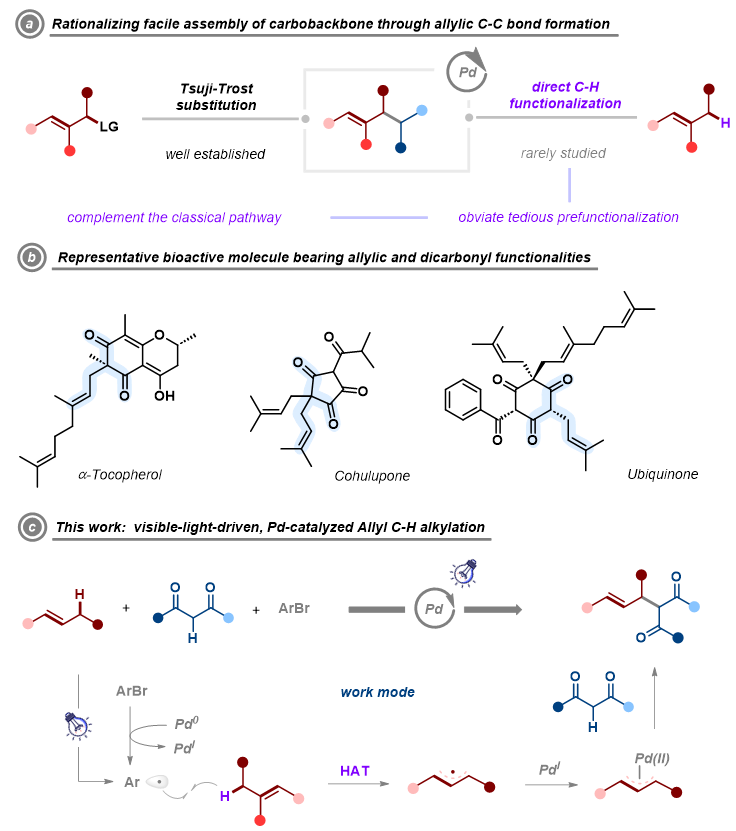
图1. 研究背景及本课题的设计思路(来源:Organic Letters)
为了验证我们的理论框架,我们开始使用丁-1-烯基苯(1a)和丙二酸二乙酯(2a)作为模型底物进行研究。在双30W蓝色LED的照射下,以1.1'-联萘-2.2'-二苯基膦(L1)为配体,Cs2CO3为碱,三氟甲苯为溶剂,对Pd(0)和Pd(II)催化剂进行了初步筛选。当使用Pd(PPh3)4作为催化剂时,以30%的收率获得了产物3。尽管其他钯催化剂被证明是反应性的,但它们的收率较低。随后对膦配体的筛选未能改善结果。配体优化后,溶剂评估表明,强极性溶剂,包括二甲亚砜(DMSO)、N,N-二甲基乙酰胺(DMA)和N,N-三甲基甲酰胺(DMF),具有良好的收率,而DMSO被确定为最佳溶剂。将浓度降低到0.075M并将1a的负载量增加到2.5当量,将收率提高到73%。对1a/2a或可见光波长的当量比的进一步调整并没有提高效率。值得注意的是,对照实验证实了钯催化剂、碱、芳基溴化物和光的必要性。因此,为后续研究建立了优化条件(图2)。
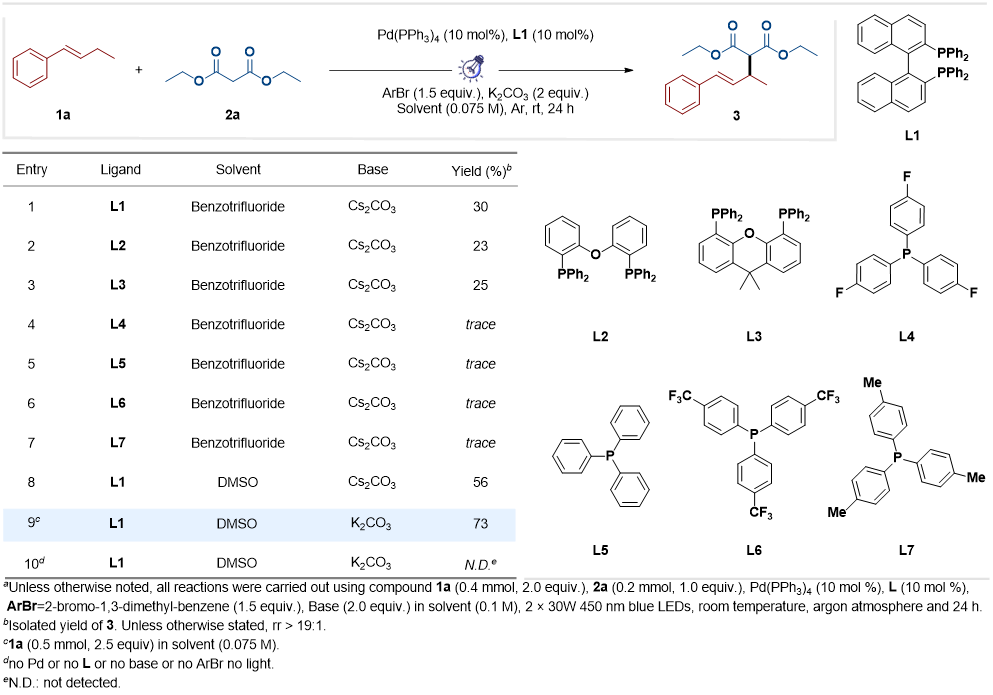
图2. 条件筛选(来源:Organic Letters)
在确定优化条件后,我们测试了该方法的适用性。最初,研究了丙二酸衍生物的范围。带有不同取代基的对称丙二酸酯以27%-61%的收率得到产物4-10。同样,不对称丙二酸酯以35%-51%的收率提供了相应的产物11-14。亲核位点碳原子上带有官能团的丙二酸酯也表现出良好反应性,以27%-45%的收率得到目标产物15-17。此外,该方案对β-酮化合物的反应性适中,分别以38%和31%的收率得到产物18和19。在此基础上,我们使用丙二酸二乙酯(2a)作为偶联剂研究了烯丙基化合物的范围。值得注意的是,该反应对苯环上的供电子和吸电子取代基容忍性较好,以36%-52%的收率得到产物20-25。碳链长度的变化(延长或缩短)也被证明是可行的,以39%和40%的收率得到相应的产品26和27。有趣的是,底物1e和1f产生了相同的产物27,但产率不同(分别为37%和40%)。此外,具有杂环和脂肪环的烯丙基化合物表现出增强的反应性,以42%-56%的收率得到产物25、28和29(图3)。
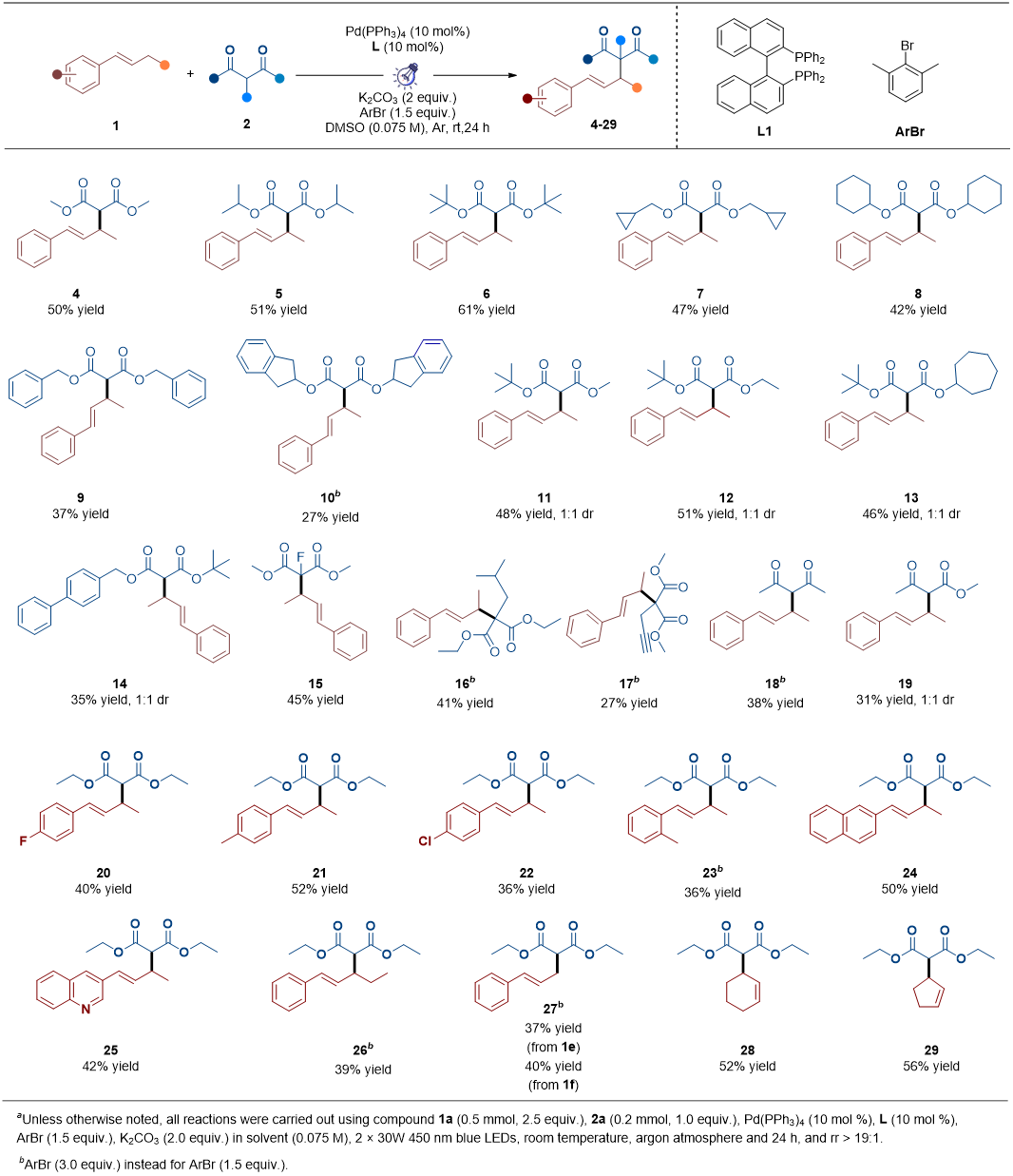
图3. 底物拓展(来源:Organic Letters)
此外,还证明了来源于药物和天然产物的各种复合丙二酸酯和烯丙基底物的后期功能化。胆固醇衍生的不对称丙二酸酯反应干净,以36%产率得到产物30。以烯丙基为特征的药物分子(如茴香脑、丁香酚)经过有效转化,得到31和32,产率为50-62%。为了验证方法的工业化应用前景,标准反应放大到2 mmol规模上进行,最后以47%的收率得到产物。随后使用Pd/C催化氢化以85%的收率得到产物。还通过水解得到丙二酸34(产率83%),硼氢化钠还原得到二醇35(产率73%);其羟基能够进一步多样化反应。为了阐明反应机理,进行了自由基捕获实验。2,2,6,6-四甲基哌啶-1-氧基(TEMPO)的自由基捕获完全支持自由基介导的途径。此外,开灯/关灯实验排除了自由基链机制(图4)。
根据机理研究和之前的报告,提出了一种可能的反应机制(图4d)。最初,Pd(0)催化剂配合物的光激发产生激发态物种Pd(0)*。Pd(0)*然后还原芳基溴,得到Pd(I)Br和苯基。随后,苯基和烯烃1a之间的氢原子转移(HAT)产生烯丙基和苯。烯丙基自由基与Pd(I)Br结合形成稳定的σ-烯丙基Pd(II)络合物A。最后,A被脱质子化物质2a(与K2CO3形成)进行亲核取代,产生产物3和KBr,同时Pd(0)催化剂络合物再生,从而完成催化循环。
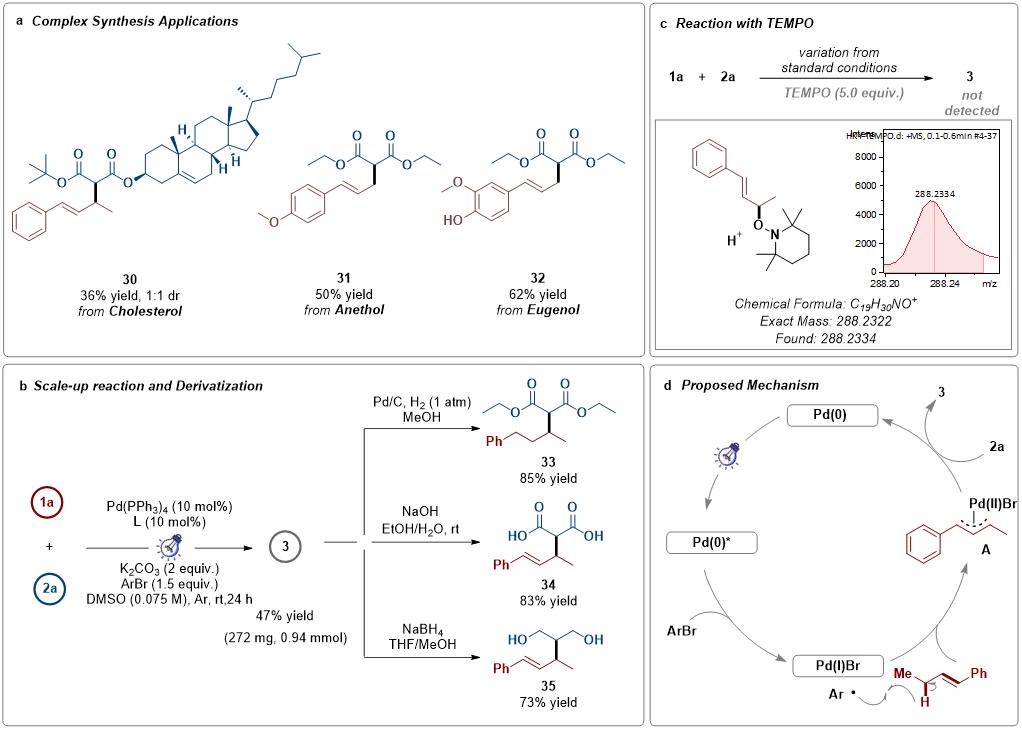
图4. 放大合成、衍生化实验、自由基捕获实验和可能的反应机理
(来源:Organic Letters)
总之,我们报告了一种用于烯丙基直接C-H烷基化的策略。采用芳基溴作为氢原子转移(HAT)试剂的光诱导Pd/BINAP催化体系,该方法能够轻松构建烯丙基C-C键。此外,该方案显示了广泛的底物范围,可容纳各种芳香族和脂肪族丙二酸酯,并且证明对部分β-酮类化合物也是有效的。这种模块化合成策略为进一步探索钯催化的烯丙基C-H官能化提供了一个多功能平台。
该工作近期发表在Org. Lett.(DOI: 10.1021/acs.orglett.5c03515)上,中南大学化学化工学院阳华教授、郑雨讲师为论文共同通讯作者,论文第一作者是中南大学2024级硕士研究生黄鲲宇与博士研究生陆伟东同学。(论文作者:Kun-Yu Huang, Wei-Dong Lu, Xiao-Qing Chen, Kai Chen, Yu Zheng,* Hua Yang*)。
该研究工作得到了国家自然科学基金、湖南省自然科学基金以及中南大学研究生自主探索创新项目等的资助。
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




