【Nat. Commun.】法国鲁昂大学Thomas Poisson团队:电化学合成联烯基硅烷和联烯基硼酸酯
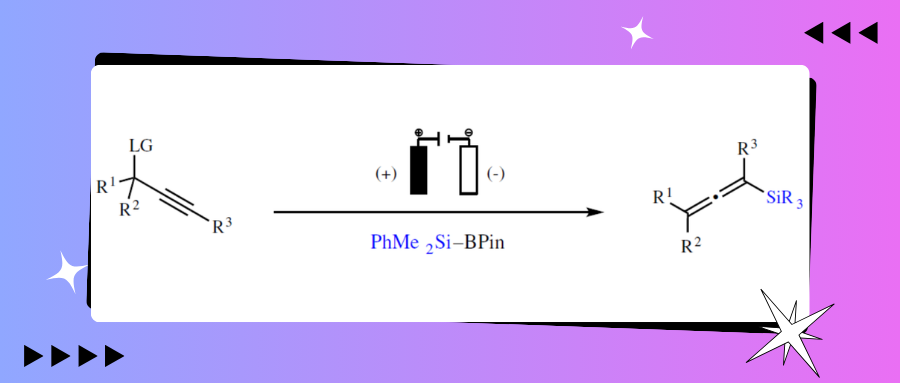
联烯基硅烷和联烯基硼酸酯是有机合成中的重要的砌块。然而,其合成过程通常需要依赖过渡金属或高活性试剂的参与。因此,开发可持续的合成方法备受关注。近日,法国鲁昂大学Thomas Poisson团队开发了一种联烯基硅烷和联烯基硼酸酯的电化学合成方法。同时,该策略无需使用催化剂,具有反应条件温和、底物范围广泛、官能团耐受性出色等特点。机理研究表明,反应涉及硅基和硼基自由基参与氧化的过程。相关研究成果发表在Nat. Commun.上。
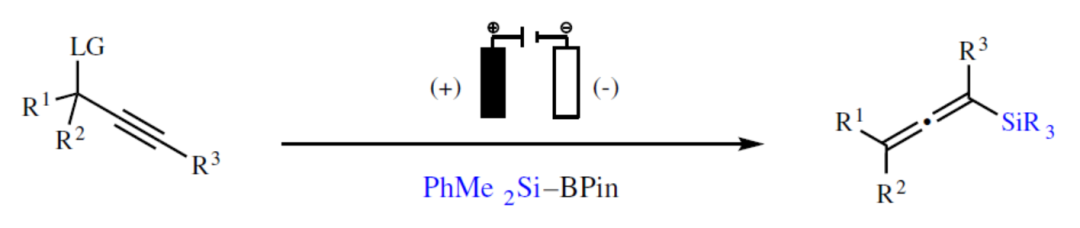
(图片来源::Nat. Commun.)
联烯基单元是一类重要的骨架,广泛存在于各类天然产物与生物活性分子等中。同时,联烯基单元也是一类重要的砌块,可进行多种官能团化反应。其中,联烯基硅烷是一类重要的多功能合成中间体,可作为炔丙基阴离子(propargylic anion)替代物。目前,对于联烯基硅烷的合成方法主要依赖于过渡金属(Cu、Ni、Rh和Pd)催化炔丙基衍生物的硅基化反应(Fig. 1, Eq. (1).)。作为补充,通过碳金属化或直接金属化生成的金属化联烯的亲电硅基化反应,为构建该骨架结构提供了一种直接途径(Fig. 1, Eq. (2))。同时,硅基化乙烯酮的Wittig反应则是另一种方法(Fig. 1, Eq. (3))。此外,以硅基化底物为起始原料,通过过渡金属催化,也可生成相应的联烯基单元(Fig. 1, Eq. (4))。然而,上述的方法常需使用过渡金属催化剂、化学计量量的强碱或苛刻的反应条件。因此,仍需开发一种更温和、更可持续的反应条件来构建此类化合物。基于前期对于有机电合成的持续研究,近日,法国鲁昂大学Thomas Poisson团队开发了一种电化学合成联烯基硅烷和联烯基硼酸酯的方法,避免了上述过渡金属催化剂的使用,具有温和的反应条件、广泛的底物范围、良好的官能团耐受性等特点。
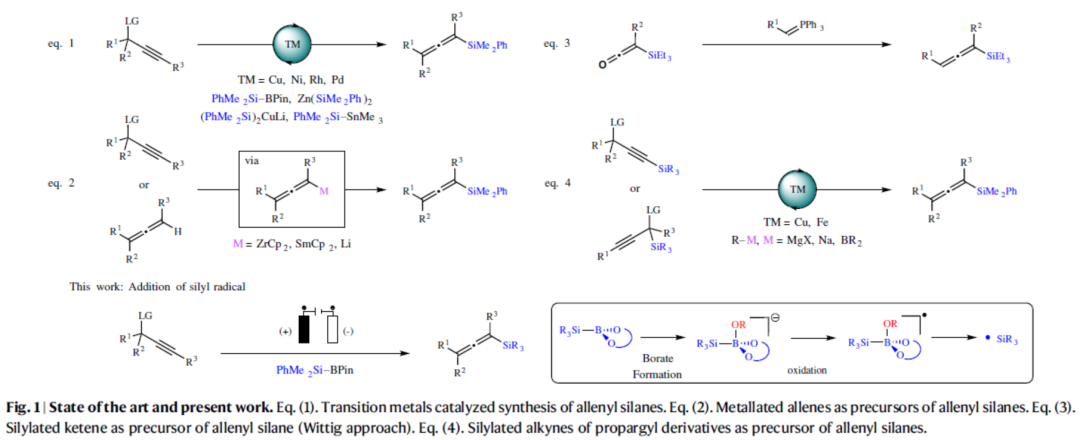
(Fig. 1,图片来源:Nat. Commun.)
首先,作者以乙酸炔丙酯衍生物(I)与Suginome试剂(PhMe2Si–BPin)作为模型底物,对反应条件进行了大量的筛选(Table 1)。筛选结果表明,当以不锈钢(SST)作为正负电极,nBu4NCl作为电解质,电流为30 mA,电势为3 F·mol-1,CH3CN和CH3OH作为混合溶剂,在室温下反应,可以74%的收率得到联烯基硅烷产物1。
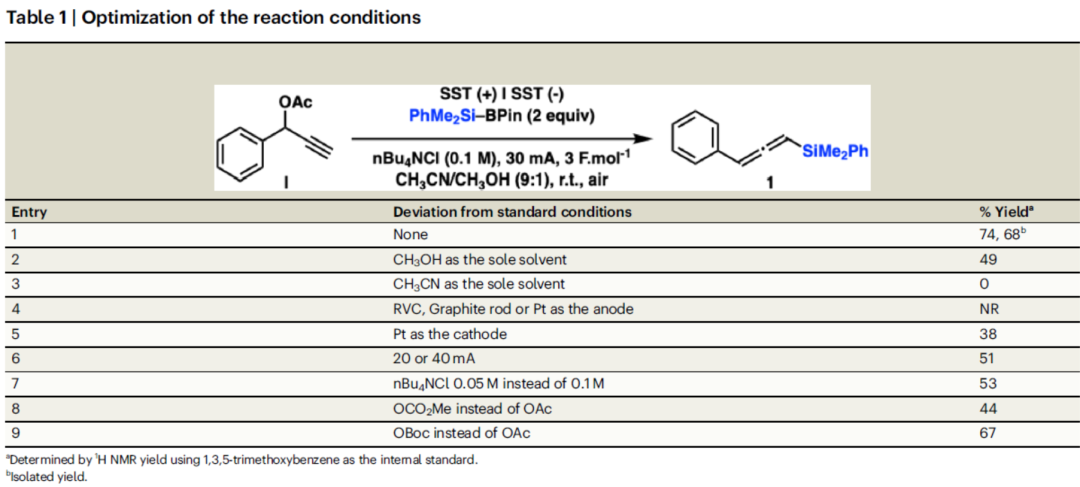
(Table 1,图片来源:Nat. Commun.)
在获得上述最佳反应条件后,作者对合成联烯基硅烷的底物范围进行了扩展(Fig. 2)。首先,当乙酸炔丙酯底物R1或R2为不同电性取代的芳基或杂芳基时,均可顺利进行反应,获得相应二取代联烯基硅烷的产物2-10,收率为20-75%。当乙酸炔丙酯底物R1或R2为烷基与环烷基时,也能够顺利进行反应,获得相应的二取代联烯基硅烷产物11-17,收率为45-78%。其次,当乙酸炔丙酯底物R1或R2分别为芳基/烷基或烷基/烷基时,可获得相应三取代联烯基硅烷产物18-22,收率为62-82%。同时,环状乙酸炔丙酯衍生物,也是合适的底物,可获得相应环烷基取代联烯基硅烷产物23-25,收率为58-70%。值得注意的是,该策略还可用于复杂分子的后期衍生化,如脱氢表雄酮与孕烯醇酮,获得相应的衍生物26-28,收率为79-95%。然而,芳基上含有氰基取代的底物、空间位阻更大的芴酮衍生物以及非末端炔烃,均未能有效反应。
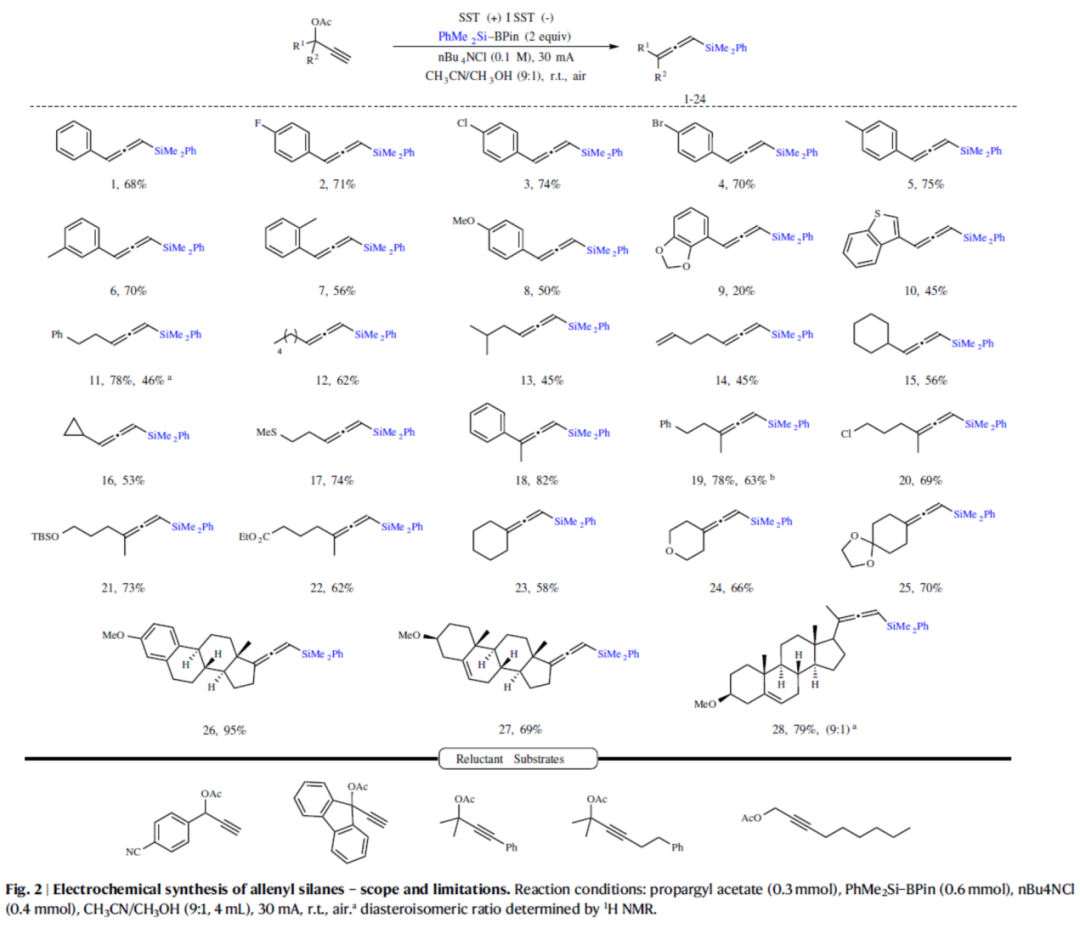
(Fig. 2,图片来源:Nat. Commun.)
紧接着,作者对合成四取代联烯基硼烷的反应条件进行了筛选(Table 2)。筛选结果表明,以炔丙基碳酸酯(II)与B2Pin2作为底物,不锈钢(SST)作为正负电极,NaOCH3作为添加剂,Et4NBF4作为电解质,电流为25 mA,电势为3 F·mol-1,快速交替极性(rAP)为150 ms,CH3OH作为溶剂,在室温下反应,可以56%的收率得到四取代联烯基硼烷产物29。
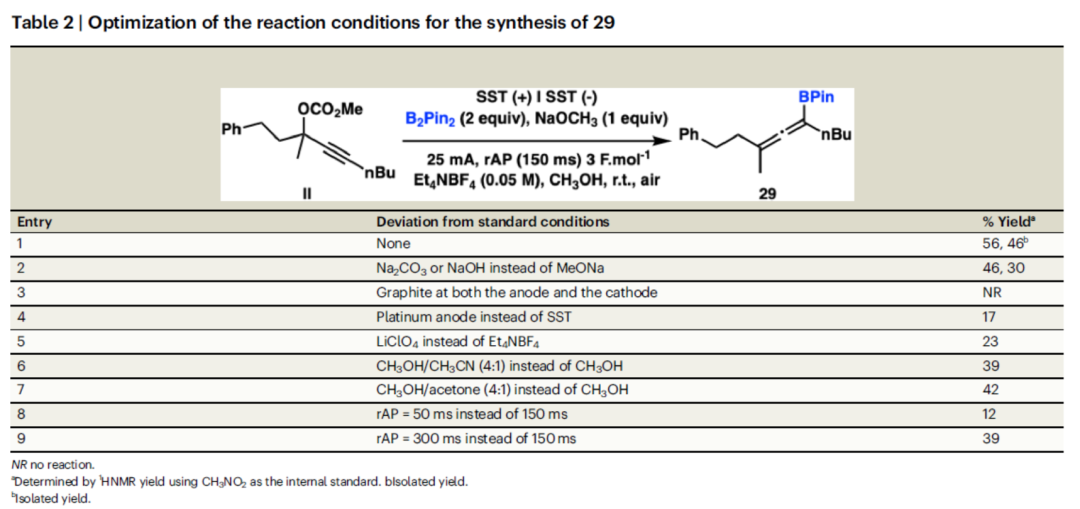
(Table 2,图片来源:Nat. Commun.)
随后,作者对合成四取代联烯基硼烷的底物范围进行了扩展(Fig. 3)。首先,当炔丙基碳酸酯底物中的R3为各种烷基与环烷基时,均可顺利进行反应,获得相应烯丙基硼烷产物29-34,收率为20-52%。其次,当炔丙基碳酸酯底物中的R1与R2为相同的甲基与丙基时,也能够顺利进行反应,获得相应烯丙基硼烷产物35-39,收率为12-50%。此外,当炔丙基碳酸酯底物中R1与R2为两种不同的烷基时,反应效率较差,如40和41,低产率主要是由于烯丙基硼烷在反应介质中的稳定性较差导致。
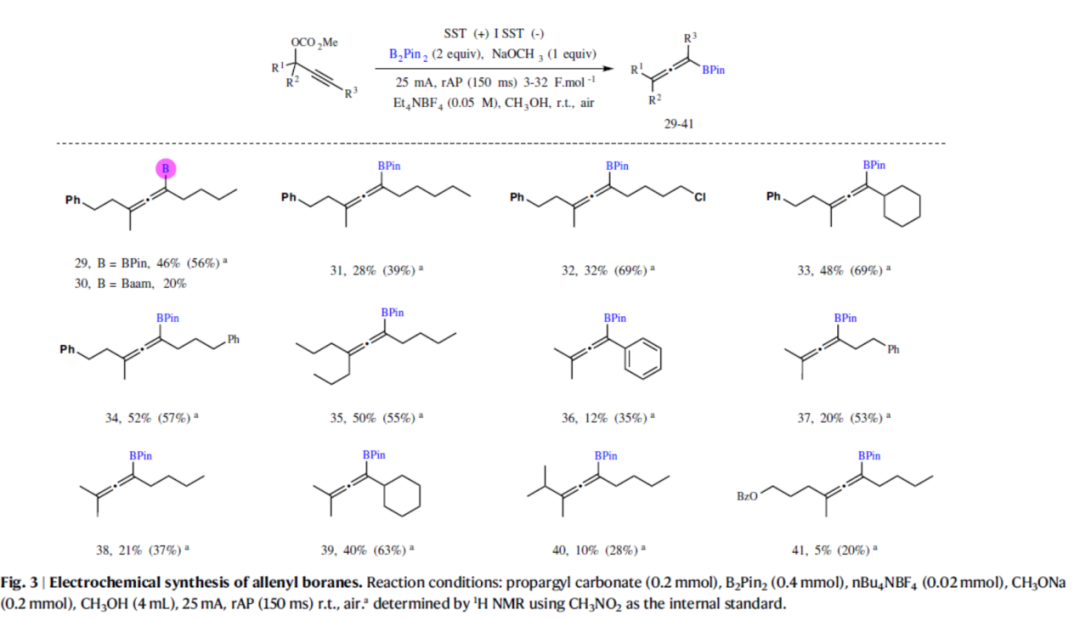
(Fig. 3,图片来源:Nat. Commun.)
此外,作者还对反应的机理进行了研究(Fig. 4)。立体保留实验结果表明,反应具有对映专一性,并揭示了以对映体富集的手性炔丙基乙酸酯为原料可能实现对映体富集联烯的构建(Fig. 4A)。自由基捕获实验结果表明,反应涉及硅基自由基的生成(Fig. 4B)。CV实验结果表明,排除了在上述条件下丙炔基衍生物的初始还原。同时,B2Pin2与甲醇盐原位形成的硼酸盐物种可能发生不可逆的氧化过程,可生成硼基自由基(Fig. 4C)。基于上述的研究以及相关文献的查阅,作者提出了一种合理的反应机理(Fig. 4D)。首先,B2Pin2与阴极还原MeOH溶剂生成的甲氧基负离子反应,形成相应的硼酸酯配合物A。其次,配合物A氧化后生成中间体B,继而分解生成硼基自由基C。硼基自由基C与炔丙基衍生物反应,形成瞬态乙烯基自由基D,其可能通过两种不同的途径生成目标的联烯产物。在Path a中,C-O键的β-断裂可生成联烯产物和相应的MeOCOO•,其具有非常缓慢的脱羧速率,可在阴极还原形成相应的阴离子。该阴离子可能会迅速释放二氧化碳,生成甲氧基负离子。在Path b中,通过β-(磷酸氧基)烷基自由基断裂过程,可生成自由基阳离子E、甲氧基负离子和CO2(由MeOCO2-产生)。自由基阳离子E可在阴极进行还原,从而获得目标的联烯产物。
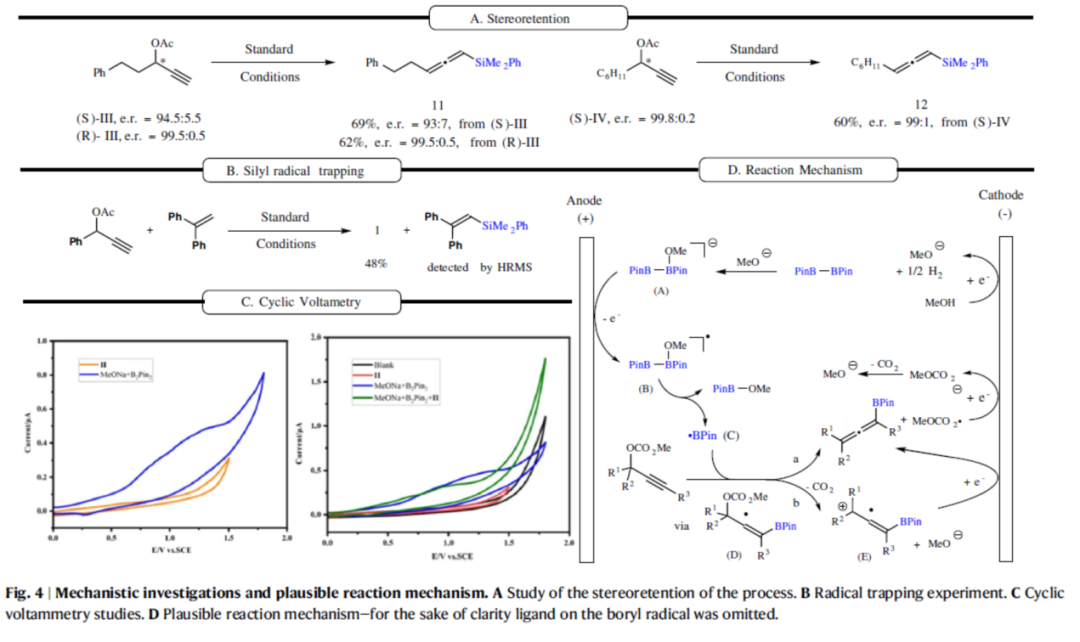
(Fig. 4,图片来源:Nat. Commun.)
最后,作者对反应的实用性进行了研究(Fig. 5)。首先,联烯化合物11经铜催化区域选择性硼氢化反应,可以40%的收率得到乙烯硼酸酯42,Z:E为2:1。联烯化合物19与苯甲醛反应,可以55%的收率得到具有炔丙基季碳中心的烯基硅烷43。其次,联烯化合物11与19经去硅基化反应,可分别获得末端无取代的联烯化合物44(收率为40%)和45(收率为49%)。此外,联烯化合物33还可进行Suzuki偶联反应、羟甲基化反应和氧化反应,获得相应的衍生物46-48,收率为45-97%。
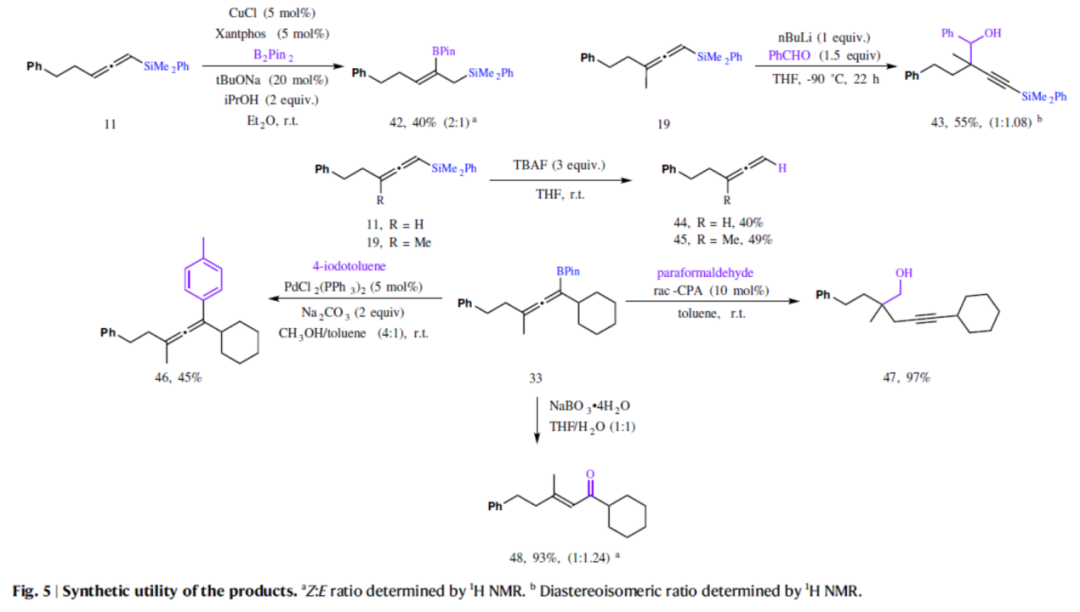
(Fig. 5,图片来源:Nat. Commun.)
法国鲁昂大学Thomas Poisson团队开发了一种温和无催化剂的电化学合成法,合成了一系列联烯基硅烷和联烯基硼酸酯衍生物。同时,该策略避免了使用敏感试剂或昂贵的过渡金属催化剂,具有反应条件温和、底物范围广泛、官能团耐受性出色等特点。机理研究表明,反应可能通过瞬态硼酸酯氧化生成的硅基或硼基自由基,对炔丙基底物进行加成而实现。
论文信息
Electrochemical synthesis of allenyl silanes and allenyl boronic esters
Tingting Feng, Tony Biremond, Philippe Jubault, Thomas Poisson
Nat. Commun.
声明:本文仅用于学术文章转载分享,不做盈利使用,如有侵权,请及时联系小编删除。




